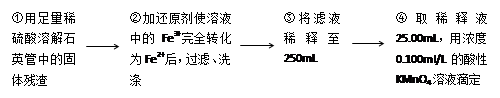-
下图是某实验室测定黄铁矿(主要成分为FeS2)中硫元素的质量分数的装置:
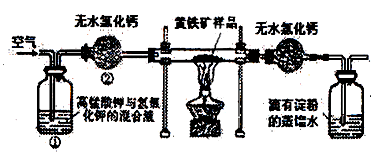
实验时有如下操作:
A.连接好全部仪器,并检查其气密性
B.称取研细的黄铁矿样品
C.将样品小心放硬质试管中部
D.以均匀的速度不断鼓入空气
E.将试管中样品加热到800℃~850℃
F.用标准碘溶液滴定含淀粉的SO2水溶液
(1)装置①的作用是__________________。装置②的作用是 _________________________。
(2)I2跟SO2水溶液反应的离子方程式为 __________________________。
(3)根据___________________________现象判断滴定已达到终点。
(4)有同学认为用上述装置测出的黄铁矿中硫元素的质量分数会偏低,其原因可能是_____(只需举出一种可能)。
(5)完成下列计算:若取6g样品在空气中充分灼烧,将吸收了SO2气体的淀粉溶液用0.1mol/L的标准碘溶液滴定,完全反应消耗溶液体积600mL,则样品中硫元素的质量分数为(假设杂质不参加反应) _____________________。
-
(14分)工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:实验原理是
A.连接全部仪器,使其成为如图装置,并检查装置的气密性。
B.称取研细的辉铜矿样品1.000g。
C. 将称量好的样品小心地放入硬质玻璃管中。
D.以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2=SO2 +2Cu。
F.移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
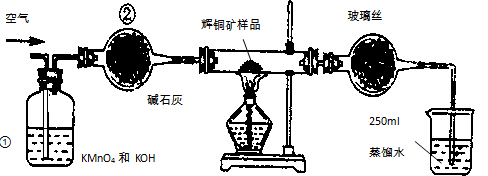
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是_________。
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
| | | |
(4)本方案设计中有一个明显的缺陷影响了测定结果(不属于操作失误),你认为是__________(写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6.25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系: c2 (H+) ·c(S2-) = 1.0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________________。
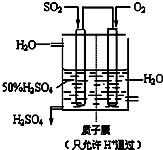
(6)某人设想以下图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式______.
-
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
A. 连接全部仪器,使其成为如图装置,并检查装置的气密性。
B. 称取研细的辉铜矿样品1.000g。
C. 将称量好的样品小心地放入硬质玻璃管中。
D. 以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2=SO2 +2Cu。
F. 移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
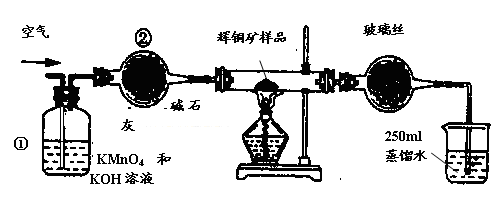
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为 ,当产生______________________________ _的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是_________。
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
| | | |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是 (写一种既可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系: c2 (H+) ·c(S2-) = 1 . 0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中c(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________。
-
实验题(17分)工业上可用下列仪器组装一套装置来测定黄铁矿中硫的质量分数(忽悠SO2、H2SO3与氧气的反应)。
实验的正确操作步骤如下:
A、连接好装置,并检查装置的气密性
B、称取研细的黄铁矿样品
C、将2.0g样品小心地放入硬质玻璃管中。
D、以1L/min的速率不断鼓入空气。
E、将硬质玻璃管中的黄铁矿样品加热到800℃~850℃。
F、用300ml的饱和碘水吸收SO2 ,发生的反应是:I2+SO2+2H2O=H2SO4+2HI
G、吸收液用CCl4萃取,分离得到上层无色溶液
H、取20.00ml 吸收液,用标准0.2000 mol·L-1的NaOH溶液滴定。(填“上”、“下”)层溶液进行后续实验。
试回答:
(1) 步骤G中所有主要仪器是 、应取
(2)装置⑤的作用是 ;
(3) 装置连接顺序是 (填编号)。
(4) 步骤H中滴定时应选用________作指示剂,可以根据________现象判断滴定已达到终点。
(5) 假定黄铁矿中的硫在操作E中已全部转化为SO2,并全部饱和碘水完全吸收。滴定得到的数据如表所示:
| 滴定次数 | 待测液的体积/mL | 标准溶液NaOH(aq)体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 第一次 | 20.00mL | 0.00 | 20.48 |
| 第二次 | 20.00mL | 0.22 | 22.15 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
则该黄铁矿样品中硫元素的质量分数为 ________。(保留小数点后1位)
-
某化学兴趣小组以黄铁矿(主要成分为FeS2)为原料进行如下实验探究。为测定黄铁矿中硫元素的质量分数,将m1g该黄铁矿样品放入如图所示装置中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品。
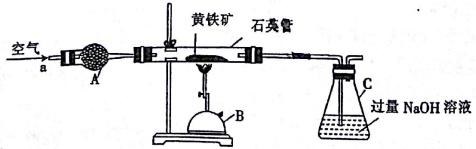
(1)仪器B的名称是________________。
(2)仪器A的作用是______________,锥形瓶C中NaOH溶液的作用是______________。
(3)反应结束后将锥形瓶C中的溶液进行如下处理:

①操作Ⅱ是洗涤、烘干、称重,其中洗涤的具体方法为______________________。
②上述流程中生成固体反应的离子方程式为__________________。
③经过分析,向m2g固体中加入过量稀盐酸时,无明显现象,则该黄铁矿中硫元素的质量分数为____(用含m1、m2的代数式表示)。
-
(15分)工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
A.连接好仪器,使其成为如图装置,并检查装置的气密性。
B.称取研细的辉铜矿样品1.000g。
C.将称量好的样品小心地放入硬质玻璃管中。
D.以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2 SO2 +2Cu。
SO2 +2Cu。
F.移取25.00mL含SO2的水溶液于250mL锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
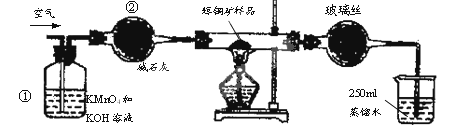
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为 ,当产生_______________________________的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是________。
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
| | | |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是 (写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系:c2 (H+)·(S2-) = 1 . 0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为1 mol/L,应调节溶液的c(H十)为__________________。
-
某化学兴趣小组测定硫铁矿(主要成分FeS2)矿样中硫元素的质量分数,进行如下实验:将m1g样品放入如图所示装置C中,打开K1关闭K2,从a处不断通入空气,高温灼烧石英管中的样品。
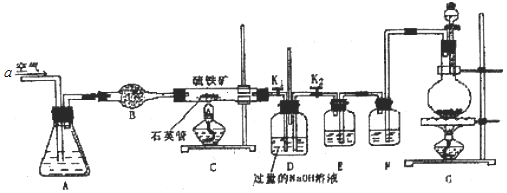
请回答下列问题:
(1)装置B的名称为_____;a处不断通入空气的目的是_____。
(2)装置A的作用是_____。
(3)反应结束后,关闭K1打开K2,向烧瓶中加入液体,点燃G处酒精灯,使烧瓶中反应发生,操作流程如图。
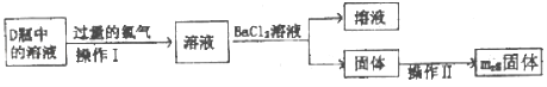
①操作I所得溶液中所含的溶质有_____。
②操作Ⅱ是洗涤、烘干、称重,检验固体是否洗净的方法是_____。
③该硫铁矿中硫元素的质量分数为_____(用含m1、m2的代数式表示)
(4)取煅烧后的熔渣(含有Fe2O3、FeO),欲验证其中存在FeO,应选用的试剂是_____。
-
中国是钢铁生产大国,也是铁矿石消费大国。某铁矿石主要成分为 和
和 ,实验室为测定
,实验室为测定 和
和 的物质的量比,利用下图所示装置进行实验。
的物质的量比,利用下图所示装置进行实验。
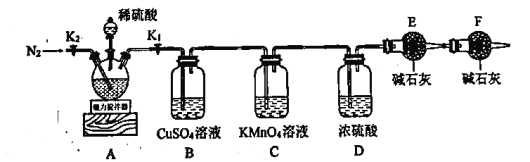
实验步骤如下:
Ⅰ.按图示连接仪器,检查装置气密性后加入药品;
Ⅱ.打开 、
、 ,通入一段时间氮气,关闭
,通入一段时间氮气,关闭 、
、 ,取下干燥管称量其质量(
,取下干燥管称量其质量( )后再连接好装置;
)后再连接好装置;
Ⅲ.打开 和分液漏斗活塞,向三颈烧瓶中慢慢滴加足量已经除去
和分液漏斗活塞,向三颈烧瓶中慢慢滴加足量已经除去 的稀硫酸(其它杂质与稀硫酸不反应,且无还原性物质),待反应完成后,打开
的稀硫酸(其它杂质与稀硫酸不反应,且无还原性物质),待反应完成后,打开 通入一段时间氮气;
通入一段时间氮气;
Ⅳ.关闭 、
、 ,取下三颈烧瓶过滤、洗涤,将滤液与洗涤液合并成100mL溶液备用;
,取下三颈烧瓶过滤、洗涤,将滤液与洗涤液合并成100mL溶液备用;
Ⅴ.取下上述步骤ⅱ中的干燥管并称量其质量( );
);
Ⅵ.取配制好的滤液25mL于锥形瓶中,用 溶液滴定。
溶液滴定。
回答下列问题:
(1)步骤Ⅱ中需要称重的干燥管是_________(填“E”或“F”)。
(2)实验过程中发现B中有黑色沉淀生成,写出装置A中 与稀硫酸反应的化学方程式__________________。
与稀硫酸反应的化学方程式__________________。
(3)C装置的作用是_________;若撤去装置F,则测得的 的含量会_________(填“偏大”“偏小”或“无影响”)。
的含量会_________(填“偏大”“偏小”或“无影响”)。
(4)下列关于步骤Ⅳ的叙述正确的是_________(填标号)。
A.滤渣中含有还原产物单质硫
B.过滤过程中玻璃棒起到引流和搅拌的作用
C.过滤操作要迅速,否则会使测得的 的含量偏低
的含量偏低
D.检验沉淀是否洗涤干净,可向滤液中加入氯化钡溶液,观察是否有白色沉淀生成
(5)步骤Ⅵ中发生反应的离子方程式为_________,到达滴定终点的现象是_________。
(6)若上述实验中 ,步骤Ⅵ消耗
,步骤Ⅵ消耗 溶液45mL,则该矿石样品中
溶液45mL,则该矿石样品中 _________。
_________。
-
黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取硫酸的主要原料。某化学学习小组对某黄铁矿石进行如下实验探究。
[实验一]测定硫元素的含量。
Ⅰ、将m1 g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
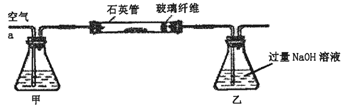
Ⅱ、反应结束后,将乙瓶中的溶液进行如下处理:

 [实验二]测定铁元素的含量。
[实验二]测定铁元素的含量。
III、测定铁元素含量的实验步骤如图所示。
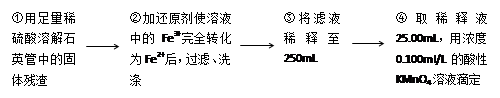
问题讨论:
(1)I中,甲瓶内所盛试剂是____溶液。乙瓶内发生反应的离子方程式为____。
(2)II中,乙瓶加入H2O2溶液时反应的离子方程式为_____________________。
(3)该黄铁矿中硫元素的质量分数为_______________________。
(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有____________________________________________。
(5)III的步骤④中,表示滴定已达终点的现象是________
(6)Ⅲ的步骤④进行了三次平行实验,测得消耗KMnO4溶液体积分别为24.98mL、24.80mL、25.02mL(KMnO4被还原为Mn2+)。根据上述数据,可计算出该黄铁矿样品铁元素的质量分数为。
-
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究.
【实验一】:测定硫元素的含量
I.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体.写出石英管中发生反应的化学方程式为:______ 2Fe2O3+8SO2