-
已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,1570C时开始分【解析】
(1)探究草酸的酸性
250C H2C2O4 K1 = 5.4 x 10-2,K2 = 5. 4 x 10 -5 ;H2CO3 K1=4.5x10-7 K2= 4.7X10-11
下列化学方程式可能正确的是________
A. H2C2O4 +CO32-=HCO3- +HC2O4- B. HC2O4- +CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32- D. H2C2O4 +CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物
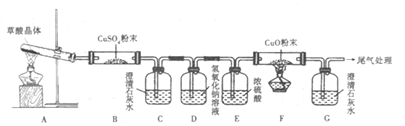
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:_______,证明有CO气体生成的现象是:_____________________
②写出H2C2O4分解的化学方程式_____________________
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加人4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液, 再向乙试管中加人一粒黄豆大的MnSO4固体,摇匀。填写下表:
| 反应现象 | ______________ |
| 实验结论 | ______________ |
| 试管中发送反应的离子方程式 | ______________ |
(4)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.OOmL于锥形瓶中=再向瓶 中加人足量稀H2SO4 ,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.OOmL0
①高锰酸钾溶液应装在_______滴定管中。(填“酸 式”或“碱 式”)
②滴定至终点时的实验现象是:______________。
③Na2C2O4的纯度是:______________
-
(12分)乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,在100℃开始升华,157℃时开始分解。
(1)探究草酸的酸性
①已知:25℃ H2C2O4 K1=5.4×102 ,K2=5.4×105;H2CO3 K1=4.5×107 K2= 4.7×1011
下列化学方程式正确的是
A.H2C2O4+CO32 = HCO3+HC2O4 B.HC2O4+CO32 = HCO3+C2O42
C.H2C2O4+CO32 = C2O42+H2O+CO2 D.2C2O42+CO2+H2O = 2HC2O4+CO32
②向1L 0.02mol/L H2C2O4溶液中滴加1L 0.01mol/L NaOH溶液。混合溶液中c(H+)>c(OH-),下列说法中正确的是 。
A.c(H2C2O4)>c(HC2O4)
B.c(Na+)+c(H+)=2 c(C2O42)+ c(HC2O4)+c(OH-)
C.c(OH-)= c(H+)+2c(H2C2O4)+c(HC2O4)
D.c(H2C2O4)+c(C2O42)+c(HC2O4)=0.02mol/L
(2)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度。
实验步骤:准确称取1gNa2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中。再向瓶中加入足量稀H2SO4 ,用0.016mol/L高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
①高锰酸钾溶液应装在 滴定管中。(填“酸式”或“碱式”)
②滴定至终点时的实验现象是: 。
③下列操作可能使测量结果偏高的是
A.盛装的Na2C2O4的滴定管没润洗
B.盛装高锰酸钾溶液的滴定管滴定前尖嘴处有气泡,滴定后气泡消失
C.读数时滴定前仰视,滴定后俯视
D.锥形瓶中残留少量水
④计算Na2C2O4的纯度
-
(16分)已知:乙二酸(HOOC-COOH,可简写为H2C2O4),俗称草酸,157℃时开始分解。
(1)探究草酸的酸性
25℃ H2C2O4 K1 = 5.4×10-2,K2 = 5.4×10-5 ;H2CO3 K1=4.5×10-7 K2= 4.7×10-11
下列化学方程式可能正确的是 。
A.H2C2O4 + CO32- = HCO3- + HC2O4-
B.HC2O4- + CO32- = HCO3- + C2O42-
C.2C2O42- + CO2 + H2O = 2HC2O4- + CO32-
D.H2C2O4 + CO32- = C2O42- + H2O +CO2↑
(2)探究草酸分解产物
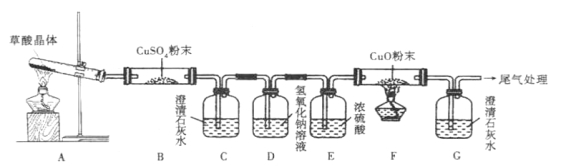
实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用是 ,证明有CO气体生成的现象是 。
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.01mol/L KMnO4酸性溶液2mL 0.1mol/L H2C2O4溶液, 再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀。填写下表:
(4)用酸性KMnO4溶液滴定Na2C2O4,求算Na2C2O4的纯度
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
① 高锰酸钾溶液应装在_______滴定管中。(填“酸式”或“碱式”)
② Na2C2O4的纯度是______________。
-
已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,157℃时开始分解.
(1)探究草酸的酸性
25℃H2C2O4 K1=5.4×10-2,K2=5.4×10-5;H2CO3K1=4.5×10-7,K2=4.7×10-11
下列化学方程式可能正确的是________.
A.H2C2O4+CO32-=HCO3-+HC2O4-B.HC2O4-+CO32-=HCO3-+C2O42-
C.2C2O42-+CO2+H2O=2HC2O4-+CO32-D.H2C2O4+CO32-+=C2O42-+H2O+CO2↑
(2)探究草酸分解产物
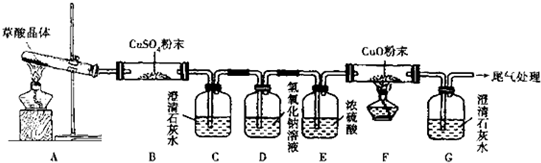
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:________,证明有CO气体生成的现象是:________.
②写出H2C2O4分解的化学方程式:________.
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mL 0.0lmol/LKMnO4酸性溶液和2mL0.1moL/L H2C2O4溶液,再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀.填写下表:
| 反应现象 | ________ |
| 实验结论 | ________ |
| 试管中发生反应的离子方程式 | ________ |
(4)用酸性KmnO4溶液滴定Na2C2O4,求算Na2C2O4的纯度
实验步骤:准确称取2.0g Na2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中.再向瓶中加入足量稀H2SO4,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL.
①高锰酸钾溶液应装在________滴定管中.(填“酸式”或“碱式”)
②滴定至终点时的实验现象是:________.
③Na2C2O4的纯度是:________.
-
已知乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.某校研究性学习小组为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为______.
(2)向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有______(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
______ MnO4-+______ H2C2O4+______ H+=______ Mn2++______ CO2↑+______ H2O
(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):
实验发现,装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红,
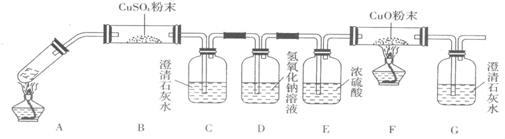
据此,乙二酸分解的产物为______.上述装置中,D的作用是______. 装置F中发生反应的化学方程式为:______ Cu+CO2
-
(16分)某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,草酸在常温下呈无色晶体状,其晶体的熔化温度低于草酸的分解温度,且易升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为____________________________________。
(2)取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
①该实验说明草酸具有________(填“氧化”或“还原”)性,该反应的反应速率先慢后快的主要原因可能是_______ _ ______。
②请配平该反应的离子方程式:______MnO4-+____H2C2O4+____ ===____Mn2++____CO2↑+____。
(3)为了探究草酸的不稳定性,某同学设计了如下实验装置:
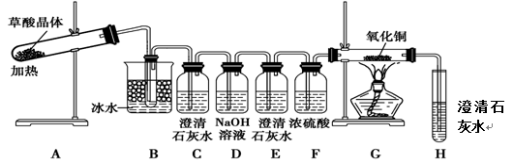
①C、H装置均变浑浊,E处无现象,G玻璃管里黑色变红色,写出A中反应的化学方程式: 。
②上述装置中,B装置的作用是 。 D的作用是 。从环境保护角度来看,该方案的不足之处是 。
(4)该小组同学将2.52 g草酸晶体(H2C2O4·2H2O)加入到100 mL 0.2 mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,形成的溶液中各离子的浓度由大到小的顺序为_______________(用离子符号表示)。
-
某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为___________________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
_____MnO4-+_____H2C2O4+____H+ = ____Mn2++_____CO2+____H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
上述装置中,D的作用是______。乙二酸分解的化学方程式为__________。
(4)该小组同学将2.52g草酸晶体(H2C2O4·2 H2O)加入到100mL0.2mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是_______(用文字简单描述)。
(5)以上溶液中各离子的浓度由大到小的顺序为:_________(用离子符号表示)。
-
某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC—COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为____________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现紫红色逐渐褪去,说明乙二酸具有_______(填:“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:__MnO4-+__H2C2O4+__H+=__Mn2++__CO2↑+__H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):
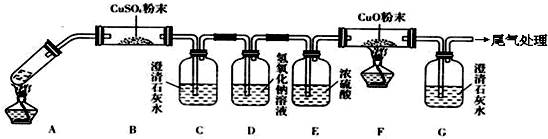
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:上述装置中,D的作用是____________________。乙二酸分解的化学方程式为________________。
(4)该小组同学将2.52g草酸晶体(H2C2O4·2H2O)加入到100mL 0.2mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是___________________。
(5)Na2C2O4溶液中离子的浓度由大到小的顺序为:__________________。
(6)设计实验证明草酸的酸性比碳酸强:__________________ 。
-
某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为______;
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有______(填“氧化性”、“还原性”或“酸性”);②请配平该反应的离子方程式:
______ MnO4-+______ H2C2O4+______ H+=______ Mn2++______ CO2↑+______H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):
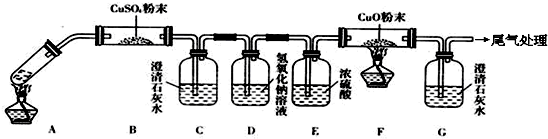
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红.据此回答:
①上述装置中,D的作用是______,
②乙二酸分解的化学方程式为______ H2O+CO↑+CO2↑
-
某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为___________________________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有_____________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:
____ MnO4–+ ____ H2C2O4+ ____ H+  ____ Mn2++ ____CO2↑ + ____ H2O
____ Mn2++ ____CO2↑ + ____ H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(注:忽略草酸的升华,且夹持装置未标出):
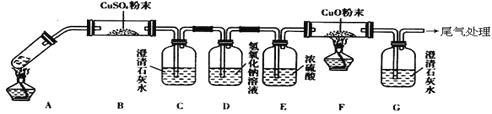
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末由黑色变为红色。据此回答:
上述装置中,D的作用是__________________.乙二酸分解的化学方程式为______________________________________.
(4)该小组同学将2.52 g草酸晶体(H2C2O4·2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是______________________(用文字简单表述)。
(5)以上溶液中各离子的浓度由大到小的顺序为_________(用离子符号表示)。








