-
某化学兴趣小组同学探索某些溶液的酸碱性。25℃时他们分别测得CH3COOH和(NH4)2SO4两种溶液的pH都为4,并对结果作了以下四种分析。则其中正确的是 ( )
A.(NH4)2SO4溶液呈酸性是因为NH4+电离出H+
B.因为醋酸是弱酸,所以醋酸促进了水的电离
C.CH3COOH和(NH4)2SO4溶液中水电离出来的H+的物质的量浓度相等
D.CH3COOH和(NH4)2SO4两水溶液呈酸性的原因不同
高二化学选择题困难题查看答案及解析
-
某化学兴趣小组同学探索某些溶液的酸碱性。25℃时他们分别测得CH3COOH和(NH4)2SO4两种溶液的pH都为4,并对结果作了以下四种分析。则其中正确的是
A.(NH4)2SO4溶液呈酸性,是因为NH4+电离出H+
B.因为醋酸是弱酸,所以醋酸溶液中水的电离平衡被促进了
C.CH3COOH和(NH4)2SO4溶液中水的电离出来的H+的物质的量浓度相同
D.CH3COOH和(NH4)2SO4两水溶液呈酸性的原因不同
高二化学选择题简单题查看答案及解析
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证 NaOH的碱性大于 NH3·H2O,继而可以验证 Na 的金属性大于 N,你认为此设计是否合理? 并说明理由:_____________________。
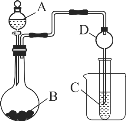
II.根据下图所示装置图回答以下问题。
(1)利用如图装置可以验证元素的非金属性的变化规律。图中 A 装置名称是____________,干燥管 D的作用是______________。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为_____________________。
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3 进而证明非金属性: N>C>Si,从以下所 给物质中选出甲同学设计的实验所用到物质:
①稀 HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置 A、C中所选试剂分别为______________(填序号);能说明酸性 H2CO3>H2SiO3的实验现象是________________________________________________________________________。
高二化学实验题中等难度题查看答案及解析
-
下列物质的溶液呈碱性的是
A. Na2CO3 B. Na2SO4 C. NH4NO3 D. CH3COOH
高二化学选择题简单题查看答案及解析
-
某化学兴趣小组的同学利用酸碱滴定法测定某变质烧碱样品(含Na2CO3杂质)中 NaOH 的质量分数。实验步骤如下:
(I)迅速地称取烧碱样品0.50 g,溶解后配制成100 mL溶液,备用。
(II)将0.1000 mol·L−1HCl标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取 20.00mL 样品溶液于锥形瓶中,滴加 2 滴酚酞;以HCl 标准溶液滴定至第一终点,记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用 HCl 标准溶液滴定至第二终点,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如下:
实验序号
1
2
3
V0/ mL
0.00
0.00
0.00
V1/ mL
22.22
22.18
22.20
V2/ mL
23.72
23.68
23.70
(1)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和__。酸式滴定管用蒸馏水洗净后、装入标准溶液并调零之前,应进行的操作是__。
(2)溶液中的H2CO3、
、
的物质的量分数随 pH 的变化如图所示:
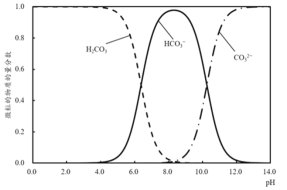
酚酞和甲基橙指示剂的变色pH范围及对应颜色见表。
酚酞
无色
pH < 8.0
粉红
pH 8.0~9.8
红
pH > 9.8
甲基橙
红
pH < 3.1
橙
pH 3.1~4.4
黄
pH > 4.4
①滴定至第一终点时,溶液中含碳微粒的主要存在形式为__。
②滴定至第一终点的过程中,发生反应的离子方程式为__。
③已知:pKa1= −lgKa1,结合图像可知,H2CO3的pKa1约为__。
a.5.0 b.6.4 c.8.0 d.10.3
(3)下列有关滴定的说法正确的是__。
a.滴定至第一终点时,溶液中 c(H+)+c(Na+) = 2c(
) + c(
) + c(OH−)
b.滴定至第一终点时,溶液中 n(Cl−) +n(
) + n(
) + n(H2CO3) =n(Na+)
c.判断滴定至第二终点的现象是溶液由黄色变为橙色
d.记录酸式滴定管读数V1时,俯视标准液液面,会导致测得的NaOH质量分数偏低
(4)样品中NaOH的质量分数
(NaOH) =__%(计算结果保留小数点后 1 位)
高二化学实验题困难题查看答案及解析
-
某校化学兴趣小组的同学对含有少量Na2SO4的NaOH样品中NaOH的含量进行测定。回答下列问题:
(1)甲同学运用沉淀法测定样品中NaOH的含量。该同学选用的药品有样品、蒸馏水、MgCl2溶液,需要测定的实验数据有__________。
(2)乙同学运用中和滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品5.0000 g,全部溶于水配制成1000.0 mL溶液。用碱式滴定管量取20.00 mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测。滴定管在使用前除洗涤外,还应____________________________________。
②用浓度为0.100 0 mol·L-1的盐酸标准溶液进行滴定。开始滴定前的一步操作是________。
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时测定pH应每滴一滴测一次。
④滴定过程中,锥形瓶中溶液的pH变化如下:
V(HCl)/mL
0.00
12.00
18.00
22.00
23.00
23.96
24.00
24.04
25.00
26.00
30.00
pH
13.1
12.6
12.2
11.7
11.4
9.9
7.0
4.0
2.7
2.4
1.9
请在坐标图中绘制出上述中和滴定的曲线。______________

⑤如表所示是几种酸碱指示剂的变色范围,根据你所作的中和滴定曲线分析,上述中和滴定中应选用的指示剂是________。
指示剂
变色范围(pH)
颜色
酸
碱
甲基橙
3.1~4.4
红
黄
石蕊
5.0~8.0
红
蓝
酚酞
8.2~10.0
无
红
⑥样品中,NaOH的质量百分含量为____________。
高二化学实验题中等难度题查看答案及解析
-
(10分)N2在化工生产、农业、医疗、航天航空等领域用途广泛。现提供以下装置(连接仪器略去):
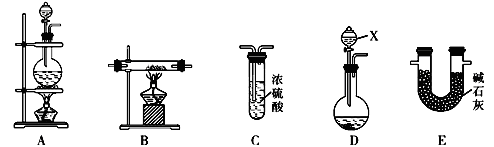
(1)某化学兴趣小组甲同学欲用加热NaNO2和NH4Cl的浓溶液制得N2,应该选择的发生装置是 ,在添加药品、制取气体前必须进行的操作是 。
(2)在加热条件下,用NH3还原CuO可制得N2,同时获得铜粉,此反应的化学反应方程式是 。
(3)乙同学利用②中反应原理制备干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料。按气流从左到右的连接顺序是D→E→B→C,其中装置D中仪器X的名称是 。装置C中试剂的作用是 。
高二化学填空题困难题查看答案及解析
-
A、B、C、D、E五种物分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①0.001 mol/L的A溶液pH=3;
②B溶液和D溶液显碱性,等浓度两者PH关系B< D;
③E是弱电解质。回答下列问题:
(1)D是____________溶液,判断理由是______________________。
(2)用水稀释0.1 mol·L-1 B时,溶液中随着水量的增加而减小的是________(填写序号)。
①
②
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
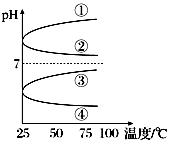
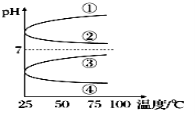
(3)将等体积、等物质的量浓度B和C的溶液混合,升高温度(溶质不会分解)溶液pH随温度变化为图中的________曲线(填写序号)。
(4)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
高二化学简答题困难题查看答案及解析
-
A、B、C、D、E五种物质分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①0.001 mol/L的A溶液pH=3;
②B溶液和D溶液显碱性,等浓度两者PH关系B< D;
③E是弱电解质。回答下列问题:
(1)D是____________溶液。
(2)用水稀释0.1 mol·L-1 B时,溶液中随着水量的增加而减小的是________(填写序号)。
①c(B)/c(OH-)
②c(OH-)/c(H+)
③c(H+)和c(OH-)的乘积
④OH-的物质的量
(3)将等体积、等物质的量浓度B和C的溶液混合,升高温度(溶质不会分解)溶液pH随温度变化为图中的________曲线(填写序号)。
(4)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌的物质的量A=E ④反应过程的平均速
率E>A
⑤A溶液里有锌剩余 ⑥E溶液里有锌剩余
高二化学填空题简单题查看答案及解析
-
某校化学兴趣小组的同学运用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
(1)用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视着____。滴定终点的现象是____________。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_____(填写序号)
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则滴定终点的读数为____mL。
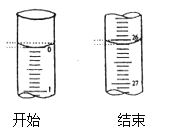
(4)某学生根据三次实验分别记录有关数据如下:
滴定次数
待测氢氧化钠溶液的体积/mL
0.1000mol/L盐酸的体积(mL)
滴定前刻度
滴定后刻度
第1次
20.00
0.00
26.01
第2次
20.00
1.56
30.30
第3次
20.00
0.22
26.21
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)__
高二化学实验题中等难度题查看答案及解析