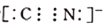-
某废水中含有CN-和Cr2O72- 等离子,需经污水处理达标后小能排放,污水处理拟采用下列流程进行处理:
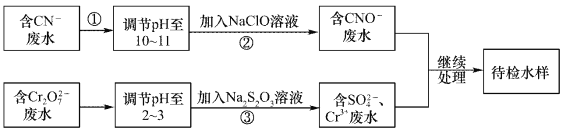
回答下列问题:
(1)步骤②中,CN- 被ClO-氧化为CNO-的离子方程式为____________。
(2)步骤③的反应的离了方程式为S2O32-+Cr2O72-+H+→SO42-+Cr3++H2O(未配平),每消耗0.4mol Cr2O72-时,反应中S2O32-失去_________mol电子。
(3)含Cr 3+废水可以加入熟石灰进一步处理,目的是___________________。
【答案】 CN-+ClO- = CNO-+Cl- 2.4 调节废水pH,使其转化为Cr(OH)3沉淀除去
【解析】(1)步骤②中,CN- 被ClO-氧化为CNO-,因为是在碱性环境中,所以ClO-只能被还原为Cl-,因此反应的离子方程式为CN-+ClO- = CNO-+Cl-;(2)根据方程式可知,在反应中Cr元素的化合价从+6价降低到+3价,得到3个电子,所以0.4 mol Cr2O72-转化为Cr3+时转移电子的物质的量=0.4mol×(6-3)×2=2.4mol;(3)熟石灰是强碱,溶于水显碱性,所以含Cr3+废水中加入熟石灰进一步处理的目的是调节废水pH,使其转化为Cr(OH)3沉淀除去。
【题型】综合题
【结束】
30
用湿法制磷酸的副产品氟硅酸(H2SiF6)生成无水氟化氢的工艺如图所示:
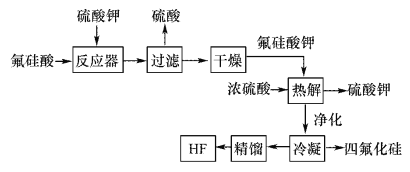
已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于酒精。
(1)写出反应器中的化学方程式:________________。
(2)在实验室过滤操作中所用的玻璃仪器有_____________,在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是:____________。
(3)该流程中哪些物质可以循环使用:_____________。(用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6,试写出该反应的化学方程式:__________________。
-
某废水中含有CN-和Cr2O72- 等离子,需经污水处理达标后小能排放,污水处理拟采用下列流程进行处理:
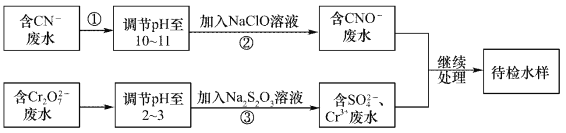
回答下列问题:
(1)步骤②中,CN- 被ClO-氧化为CNO-的离子方程式为____________。
(2)步骤③的反应的离了方程式为S2O32-+Cr2O72-+H+→SO42-+Cr3++H2O(未配平),每消耗0.4mol Cr2O72-时,反应中S2O32-失去_________mol电子。
(3)含Cr 3+废水可以加入熟石灰进一步处理,目的是___________________。
【答案】 CN-+ClO- = CNO-+Cl- 2.4 调节废水pH,使其转化为Cr(OH)3沉淀除去
【解析】(1)步骤②中,CN- 被ClO-氧化为CNO-,因为是在碱性环境中,所以ClO-只能被还原为Cl-,因此反应的离子方程式为CN-+ClO- = CNO-+Cl-;(2)根据方程式可知,在反应中Cr元素的化合价从+6价降低到+3价,得到3个电子,所以0.4 mol Cr2O72-转化为Cr3+时转移电子的物质的量=0.4mol×(6-3)×2=2.4mol;(3)熟石灰是强碱,溶于水显碱性,所以含Cr3+废水中加入熟石灰进一步处理的目的是调节废水pH,使其转化为Cr(OH)3沉淀除去。
【题型】综合题
【结束】
30
用湿法制磷酸的副产品氟硅酸(H2SiF6)生成无水氟化氢的工艺如图所示:
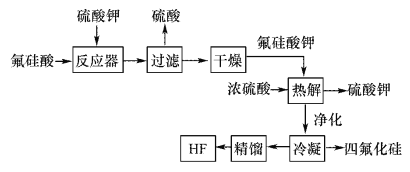
已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于酒精。
(1)写出反应器中的化学方程式:________________。
(2)在实验室过滤操作中所用的玻璃仪器有_____________,在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是:____________。
(3)该流程中哪些物质可以循环使用:_____________。(用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6,试写出该反应的化学方程式:__________________。
-
化学工业中会产生大带含铬废水,需进行无害化处理检测达标后才能排放。
(1)工业常用NaHSO3还原法处理,方法如下:向酸性废水中加入NaHSO3使Cr2O72- 还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
① 写出NaHSO3与Cr2O72-反应的离子方程式:__________________________________。
②已知25℃时Ksp[Cr(OH)3]=6.4×10-31。若除去废水中Cr3+,使其浓度小于1×10-5 mol•L-1,此时溶液中的c(H+)<_________mol•L-1
(2)废水中铬元素总浓度的测定方法如下:向一定量含Cr2O72-和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O72-与I-完全反应后生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:Cr3+ 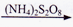 Cr2O72-
Cr2O72-  I2
I2  S4O62-
S4O62-
① 上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会________(选填“偏大”、“偏小”或“不变”)。
②准确移取含Cr2O72-和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000 mol•L-1的Na2S2O3标准溶液13.50 mL。计算该废水中铬元素总浓度(以mg·L-1表示),写出计算过程。_____________________________________________________
-
工业废水中常含有一定量的Cr2O72﹣和CrO42﹣,它们会对人类及生态系统产生很大的伤害,必须进行处理,常用的处理方法为还原沉淀法.
该法的工艺流程为CrO42- Cr2O72-
Cr2O72- Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
①第①步的反应是否为氧化还原反应 (填“是”或“否”)
②第②步中,还原1molCr2O72﹣离子,需要 mol的FeSO4•7H2O.
③写出第③步反应的离子方程式 .
-
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理.该法的工艺流程为:
CrO42- Cr2O72-
Cr2O72- Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+⇌Cr2O72-(橙色)+H2O
(1)若平衡时溶液呈强酸性,则溶液显________色
(2)能说明第①步反应达平衡状态的是________.
A.Cr2O72-和CrO42-的浓度相同 B.溶液的颜色不变
C.CrO42-的消耗速率是Cr2O72-生成速率的2倍 D.溶液的pH值不变
(3)第②步中,还原0.01mol Cr2O72-离子,需要________mol的FeSO4•7H2O.
(4)Cr(OH)3在水溶液中有两种电离方式,并存在以下平衡:
H++CrO2-(亮绿色)+H2O⇌Cr(OH)3(s)⇌Cr3+(紫色)+3OH-
下列有关说法中正确的是________
a、加酸平衡向右移动,生成Cr3+;加碱平衡向左移动,生成CrO2-
b、在一定条件下存在反应:Cr(OH)3+OH-→CrO2-+2H2O;Cr(OH)3+3H+→Cr3++3H2O
c、Cr3+盐溶液中加入NaOH溶液,先产生沉淀,后沉淀消失,溶液变成无色
d、Cr(OH)3(固)在水中存在三个平衡.
-
某工厂排放的废水中含有氰化物,可在碱性条件下对氰化物进行净化处理:2CN-+8OH- +5C12=2CO2+N2+10Cl-+4H2O。下列分析中错误的是( )
A.当反应消耗0.2 mol CN-时,反应中转移电子的物质的量是1 mol
B.还原性:CN->Cl-
C.CN-的电子式为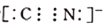
D.该反应中氧化剂和还原剂的物质的量之比是2∶5
-
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确是
A. 阳极反应为Fe-2e-=Fe2+
B. 电解过程中溶液pH不会变化
C. 过程中有Fe(OH)3沉淀生成
D. 电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原
-
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图,下列说法不正确的是
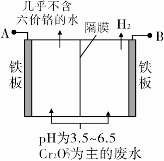
A.A接电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原
-
某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品。具体流程如下:
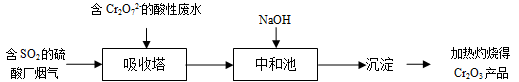
已知吸收塔中反应后的铬元素以Cr3+形式存在,下列说法中正确的是
A、吸收塔中的硫元素可能以单质形式存在
B、中和池中只发生生成沉淀的复分解反应
C、在中和池中加入盐酸酸化的BaCl2溶液,可能产生白色沉淀
D、由题意分析得到,沉淀可能是Cr(OH)6
-
某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品。具体流程如下:
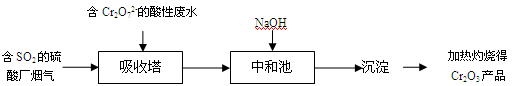
已知吸收塔中反应后的铬元素以Cr3+形式存在,下列说法中正确的是
A.吸收塔中的硫元素可能以单质形式存在
B.中和池中只发生生成沉淀的复分解反应
C.在中和池中加入盐酸酸化的BaCl2溶液,可能产生白色沉淀
D.由题意分析得到,沉淀可能是Cr(OH)6




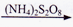 Cr2O72-
Cr2O72-