-
某粗盐主要成分为氯化钠,杂质为不溶性泥沙和Mg2+、Ca2+、和SO42- 。某校化学兴趣小组探究食盐的精制过程.以该粗盐为原料,通过如下几个实验步骤,可制得纯净的食盐固体。
①过滤②蒸发③加入稍过量的Na2CO3溶液④滴入稀盐酸至无气泡产生⑤溶解⑥加入稍过量的NaOH溶液⑦加入稍过量的BaCl2溶液。
(1)第⑤中用到的仪器有:______________.
(2)第①步操作中得到沉淀的成分有:泥沙、BaSO4 、Ma(OH)2、______________、_____________;
洗涤沉淀的正确方法是_________________。
(3)正确的操作顺序是__________________。
(4)写出第④ 步中涉及到的两个化学反应方程式是:___________________,__________________.
高一化学实验题困难题查看答案及解析
-
某粗盐主要成分为氯化钠,杂质为不溶性泥沙和可溶性的MgCl2、CaCl2和Na2SO4。某校化学兴趣小组欲探究食盐的精制过程,以该粗盐为原料,设计方案流程如下:
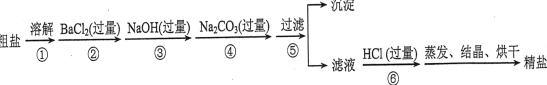
试回答下列问题:
(1)在第①步和第⑤步中都要用到玻璃棒,它们的主要作用分别是 、 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中的 、 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、 。
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是 。
(5)写出第②、③步涉及的两个化学反应的离子方程式: 、 。
高一化学实验题困难题查看答案及解析
-
某粗盐主要成分为氯化钠,杂质为不溶性泥沙和可溶性的MgCl2、CaCl2和Na2SO4.某校化学兴趣小组欲探究食盐的精制过程,以该粗盐为原料,设计方案流程如下:

试回答下列问题:
(1)在第①步和第⑤步中都要用到玻璃棒,它们的主要作用分别是________、________.
(2)第②步操作的目的是除去粗盐中的________ (填化学式,下同),第⑥步操作的目的是除去滤液中的________、________.
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、________、________(填化学式)
(4)在第⑨步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是________.写出第⑥步涉及的两个化学反应的离子方程式:________、________.高一化学填空题中等难度题查看答案及解析
-
(11分)电解法制烧碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42- 杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
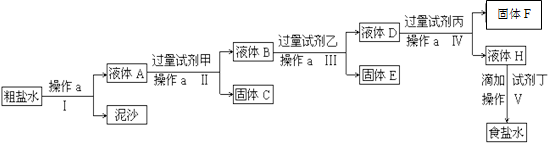
请回答以下问题:
(1)操作a的名称是____________。
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。试剂乙为________,固体F为。
(3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________、_________________。
高一化学填空题简单题查看答案及解析
-
(一)电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:

请回答以下问题:
(1)操作a的名称是______________,所用玻璃仪器有_________________;
(2)在第Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为(填化学式)_______________溶液;
(3)写出固体H所含物质的化学式_________________________________;
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式____________________________________________。
(二)某次实验需用0.4 mol·L-1 NaOH溶液500 mL。若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏低的是__________,对实验结果没有影响的是________(填字母代号)。
A.所用的NaOH中混有少量Na2O
B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
高一化学实验题中等难度题查看答案及解析
-
(8分)电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
 请回答以下问题:
请回答以下问题:(1)操作a的名称是_______,所用玻璃仪器有_____________;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为(填化学式)___溶液;
(3)写出固体H所含物质的化学式_____________;
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式
_______________________;_______________________。
高一化学填空题简单题查看答案及解析
-
电解法制烧碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42- 杂质,不符合电解要求,因此必须经过精制.某校实验小组精制粗盐水的实验过程如下:

请回答以下问题:
(1)操作a的名称是________.
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液.试剂乙为________,固体F为________.
(3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________、________.高一化学填空题中等难度题查看答案及解析
-
电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42—杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
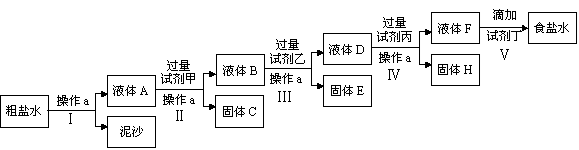
请回答以下问题:
(1)操作a的名称是_______,所用玻璃仪器有____________、玻璃棒、烧杯;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为(填化学式)____溶液;
(3)写出固体H所含物质的化学式_____________;
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式: _______________________;_______________________。
高一化学选择题中等难度题查看答案及解析
-
电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、SO42-等杂质,不符合电解要求,因此必须经过精制。某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步骤1:去一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调节盐水的pH;
步骤3:将得到的溶液蒸发、结晶、烘干即得精盐;请回答以下问题:
(1)上述实验中的过滤操作需要烧杯、__________、__________等玻璃仪器。
(2)步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的合理顺序为:______________________________。
(3)步骤2中,加入Na2CO3时主要发生反应的离子方程式为:______________________________。
高一化学实验题中等难度题查看答案及解析
-
海水中有取之不尽的化学资源,从海水中可提取多种化工原料。如图是某工厂综合利用海水资源的示意图。
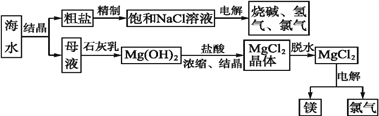
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得饱和NaCl溶液。精制过程中所用试剂有a、BaCl2溶液、b、Na2CO3溶液、c、 NaOH溶液、d、盐酸。加入试剂顺序正确的是____________;
A、a.b.c.d B、c.b.a.d C、b.a.d.c D、a.c.b.d
(2)写出电解饱和食盐水方程式________________________________________,产生的Cl2和烧碱反应能生成____________(填商品名称),反应方程式________。
(3)海水中提取食盐后的母液中含有K+、Na+、Mg2+等。从离子反应的角度考虑,向母液中加入石灰乳的作用是_________________________。
(4)电解熔融的氯化镁所得的镁蒸气冷却后即为固体镁,可以冷却镁蒸气的气体氛围为_____。
A.H2 B.CO2 C.空气 D.Ar
高一化学综合题中等难度题查看答案及解析