-
工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体。

下列说法错误的是
A.步骤a中还需要加入适量的氧气和水
B.保温去铁后过滤,铁元素主要以+2价的沉淀形式被过滤出去
C.蒸发浓缩的过程中加入适当的硝酸,目的是抑制硝酸铜的水解
D.硝酸铜溶液中离子浓度大小:
-
工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体。

下列说法错误的是
A.步骤a中还需要加入适量的氧气和水
B.保温去铁后过滤,铁元素主要以+2价的沉淀形式被过滤出去
C.蒸发浓缩的过程中加入适当的硝酸,目的是抑制硝酸铜的水解
D.硝酸铜溶液中离子浓度大小:
-
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
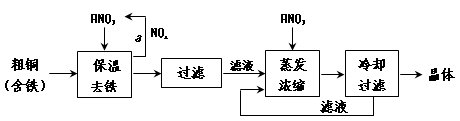
①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 。
(3)图-2是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。
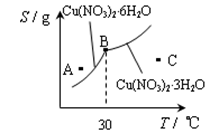
a. A点时的溶液为不饱和溶液
b. B点时两种晶体可以共存
c. 按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d. 若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
-
(选修—化学与技术)(15分)
(1)工业上以粗铜为原料采取如图1所示流程制备硝酸铜晶体:

①在步骤a中,还需要通入氧气和水,其目的是________。
②在保温去铁的过程中,为使Fe3+沉淀完全,根据下表数据,溶液的pH值应保持在________范围。调节pH值时,可以向溶液中加入的试剂是( )
(a) NaOH溶液 (b) 氨水 (c) Cu(OH)2 (d) CuO
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
③在操作Ⅰ之前,对滤液用HNO3调节pH值至1,其目的是(结合离子方程式说明)________。
④从滤液中制取硝酸铜晶体的操作Ⅰ的具体步骤是________。
(2)图2是某小组学生查阅资料后所绘出的硝酸铜晶体[Cu(NO3)2 nH2O]的溶解度曲线(温度在300C左右对应不同的晶体),下列说法正确的是( )
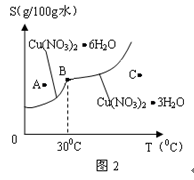
(a) A点时的溶液为不饱和溶液
(b) B点时两种晶体可以共存
(c)按上述流程最终得到的晶体一定是Cu(NO3)2 3H2O
(d) 若将C点时的溶液降温至300C以下,可以析出Cu(NO3)2 6H2O晶体
-
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
①在步骤a中,还需要通入氧气和水,其目的是______.
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在______范围.
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
Fe3+
Cu2+ | 1.9
4.7 | 3.2
6.7 |
不用加水的方法调节溶液pH的原因是______.
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)______.
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是______.
(3)图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2•nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是______(填字母).
a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2•3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2•6H2O晶体
(4)某些共价化合物(如H2O、NH3、N2O4等)在液态时有微弱的导电性,主要是因为发生了电离,如:2NH3 NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应.液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是______;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是______.
NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应.液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是______;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是______.
-
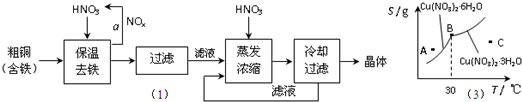
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
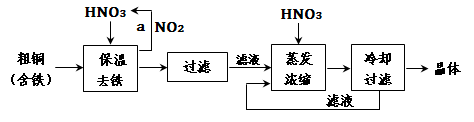
①在步骤a中,还需要通入氧气和水,其目的是________.
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在________范围。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是________。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)________。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是________。
(3)在硝酸铜溶液中,各种离子浓度由大到小的顺序是________。
-
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
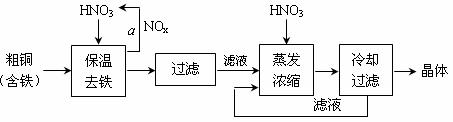
①在步骤a中,还需要通入氧气和水,其目的是 ________ 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 ________ 范围。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是 ________ 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明) 。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 ________ 。
 (3)下图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2·nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。
(3)下图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2·nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。
a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d.若将C点时的溶液降温至 30℃以下,可能析出Cu(NO3)2·6H2O晶体
(4)某些共价化合物(如H2O、NH3、N2O4等)在液态时有微弱的导电性,主要是因为发生了电离,如:2NH3 NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是________;
NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是________;
Cu与液态N2O4反应制得无水硝酸铜的化学方程式是 ________ 。
-
硝酸铜是常用的一种无机化学试剂
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:

①在步骤a中,还需要通入氧气和水,其目的是__________
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO调节溶液的pH,根据下表数据,溶液的pH应保持在_________范围

③在滤液蒸发浓缩步骤中,适当加入稀硝酸的作用是__________________________
(2)某研究学习小组将一定质量的硝酸铜晶体【Cu(NO3)2•6H O】放在坩埚中加热,在不同温度阶段进行质量分析,绘制出剩余固体质量分数与温度关系如下图所示。据图回答下列问题:
O】放在坩埚中加热,在不同温度阶段进行质量分析,绘制出剩余固体质量分数与温度关系如下图所示。据图回答下列问题:
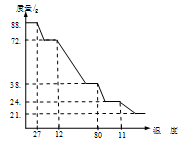
①当温度27℃<T<120℃时,反应的化学方程式为________②剩余固体质量为38.4g时,固体成分为【Cu(NO3)2•2Cu(OH)2】,当温度120℃<T<800℃时,反应的化学方程式为________ (此温度下,HNO 也分解)③当剩余固体质量为21.6g时,固体的化学式为_____________________
也分解)③当剩余固体质量为21.6g时,固体的化学式为_____________________
(3)制备无水硝酸铜的方法之一是用Cu与液态N O
O 反应,反应过程中有无色气体放出,遇到空气变红棕色。反应的化学方程式是_________________
反应,反应过程中有无色气体放出,遇到空气变红棕色。反应的化学方程式是_________________
-
以硫铁矿(主要成分为 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下所示:
)的工艺流程如下所示:
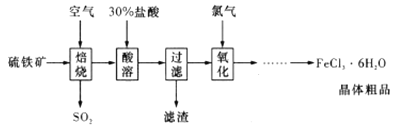
下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的 应回收利用
应回收利用
C. 通入氯气的目的是氧化
D. 用 制取无水
制取无水 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
-
以硫铁矿(主要成分为 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下所示:
)的工艺流程如下所示:
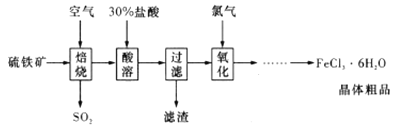
下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的 应回收利用
应回收利用
C. 通入氯气的目的是氧化
D. 用 制取无水
制取无水 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热













