-
有甲、乙两位同学根据所学化学知识,设计了由铜和硫酸为原料制取硫酸铜的两种方案:①铜与浓硫酸加热直接反应,即Cu→CuS04
②将铜加到热的稀硫酸中并通入空气来制备硫酸铜,即由Cu→CuO→CuSO4,
试回答:
(1)、写出方案①的化学反应方程式________
这两种方案,你认为哪一种方案比较合理?________。(答编号),理由是
________
(2)、实验室采用方案①取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲、乙两位同学为了验证其中灰白色沉淀的主要成分,设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌
实验现象:_____________________________________________
实验结论:所得灰白色固体的化学式为________________
直到最后反应完毕,发现试管中还有铜片剩余。可两位同学仍然认为试管中还有硫酸剩余,他们这样认为的理由是________________________
高一化学实验题困难题查看答案及解析
-
甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即
方案②:由
请回答下列问题:
(1)“方案①”中铜和浓硫酸反应的化学方程式是______________________。
该反应体现了浓硫酸的__________性和____________性。
(2)这两种方案,你认为哪一种方案更合理?_______(答编号)。理由是____________。
高一化学选择题中等难度题查看答案及解析
-
科学探究的基本程序包括形成问题、建立假设、设计研究方案、检验假设、表达或交流结果等.请根据课本中的《活动与探究》相关知识回答问题.
某同学欲用下图装置可用来探究浓硫酸与木炭粉的加热条件下反应产生的所有气体产物,填写下列空白: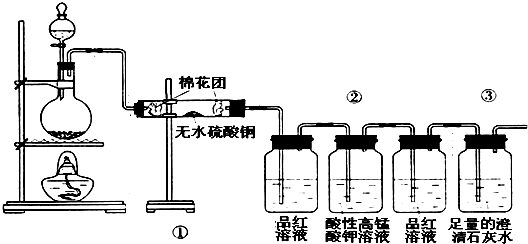
(1)写出木炭粉与浓硫酸反应的化学方程式________
②中3个洗气瓶的现象依次为________、________、________
(2)如果将仪器的连接顺序变为①、③、②,则不能检出的物质是________.
(3)如果将仪器的连接顺序变为②、③、①,则不能检出的物质是________.
(4)如果将仪器的连接顺序变为②、①、③:则不能检出的物质是________.高一化学填空题中等难度题查看答案及解析
-
硫酸铜的制备实验是化学实验教学中一个必做实验,某学习小组设计了如下两个实验方案:
实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
(1)根据上述实验和反应,比较浓硫酸与稀硫酸的性质,浓硫酸具有 。
(2)该反应的化学方程式为 。
实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,其反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
(3)Fe2(SO4)3的作用是 。
(4)得到的混合液可以用下列四种物质中的 调节溶液的pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B. CuO C. CuCO3 D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:
实 验 (一)
实 验 (二)
主要优点
操作简便
(1)原料充分转化为产品
(2)没有有害气体排放
主要缺点
高一化学实验题极难题查看答案及解析
-
为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了如下图所示的实验装置。
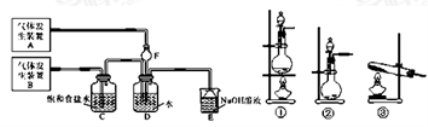
(1)该化学兴趣小组同学为制取Cl2和SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。在此实验中,F仪器的作用是:______________;发生装置B应选择三种装置中的___________(填序号)。
(2)D装置中主要反应的离子方程式为__________________。
(3)为验证通入D装置中过量的气体是Cl2还是SO2气体,兴趣小组的同学准备了以下试剂:①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液 ⑤酸性高锰酸钾溶液。
A.若Cl2过量:取适量D中溶液滴加至盛有______(选填一个序号)试剂的试管内,再加入_____(选填一个序号)试剂,发生的现象是:____________________;
B.若SO2过量:取适量D中溶液滴加至盛有______(选填一个序号)试剂的试管内,发生的现象是:____________________。
高一化学实验题简单题查看答案及解析
-
为了探究Cl2、SO2同时通入H2O中发生飞反应,某化学兴趣小组同学设计了如下图所示的实验装置。
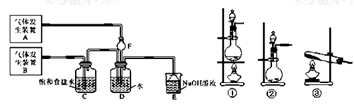
(1)该化学兴趣小组同学为制取Cl2和SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。在此实验中,F仪器的作用是:______________;发生装置B应选择三种装置中的___________(填序号)。
(2)D装置中主要反应的离子方程式为__________________。
(3)为验证通入D装置中过量的气体是Cl2还是SO2气体,兴趣小组的同学准备了以下试剂:
①氯化铁溶液
②氯化亚铁溶液
③硫氰化钾溶液
④品红溶液
⑤酸性高锰酸钾溶液。
A.若Cl2过量:取适量D中溶液滴加至盛有______(选填一个序号)试剂的试管内,再加入_____(选填一个序号)试剂,发生的现象是:____________________;
B.若SO2过量:取适量D中溶液滴加至盛有______(选填一个序号)试剂的试管内,发生的现象是:____________________。
高一化学实验题简单题查看答案及解析
-
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
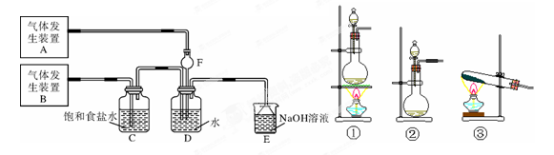
(1)该组同学为了制取Cl2,SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。在此实验中,发生装置B应选择三种装置中的___________(选填序号),F的作用是_____________。
(2)D装置中主要反应的离子方程式为__________________________。
(3)为检验通入D装置中的Cl2是否过量,该组同学取适量D溶液滴加至盛有少量紫色石蕊的试管中,若出现___________现象,则Cl2过量,此时E中发生的离子反应方程式为______________________,若D中出现__________________实验现象,则氯气不过量。
高一化学实验题困难题查看答案及解析
-
某化学兴趣小组在实验室以铜和浓硫酸为原料,采用两种方法制取胆矾。制备方法如下:
方法一:将铜屑放入浓硫酸中加热
(1)写出该反应的化学方程式______________。
(2)浓硫酸试剂瓶上贴的标签应该是______________(填字母选项)。
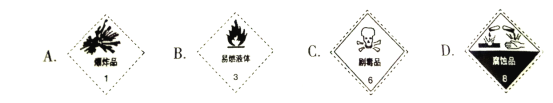
(3)通过上述反应后,经过一系列操作,若最终得到胆矾晶体25.0g,则被还原的H2SO4的物质的量为____________mol。
方法二:将铜屑置入稀硫酸中,加热并不断鼓入空气,该反应的化学方程式为:2Cu+ H2SO4+O2
2 CuSO4+2H2O
(4)写出该反应的离子方程式:____________________________。
(5)上述反应中氧化剂和还原剂的物质的量之比为___________。
(6)充分反应后,将制得的硫酸铜溶液经过蒸发浓缩、___________,过滤,即可得到胆矾晶体。
(7)对比两种方法,方法二相对于方法一有两个明显的优点:
①制取等质量的胆矾消耗的硫酸的量少;
②__________________________________________________
高一化学实验题中等难度题查看答案及解析
-
Cu在加热条件下能与浓硫酸反应(反应Ⅰ),但工业上制取CuSO4却不是直接用浓硫酸与铜反应,而是将铜丝浸入稀硫酸中并不断由容器的下部吹入细小的空气泡(反应Ⅱ)。
(1)写出反应Ⅰ、Ⅱ的化学方程式___、___。
(2)试分析反应Ⅱ的制备办法的优点___。
高一化学填空题中等难度题查看答案及解析
-
(1)现有废铜屑和废硫酸,请从原料的利用率和环保的角度分析,设计一个制取胆矾的合理方案,只用化学方程式说明
第一步:________
第二步:________
第三步:过滤,加热浓缩,冷却结晶________
(2)有人建议用铜和稀硫酸混合在加热的条件下不断通入空气以制得硫酸铜溶液,请写出该反应的化学方程式________.高一化学填空题中等难度题查看答案及解析