-
(I)下图是工业生产硝酸铵的流程。

(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是________(填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式:________
(II)某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(3)该反应的离子方程式为___________________________________________________。
(4)提出合理假设。该实验中反应速率明显加快的原因可能是_____________________。
A.反应放热导致温度升高 B.压强增大
C.生成物有催化作用 D.反应物接触面积增大
(5)初步探究。测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
结合实验目的和表中数据,你得出的结论是__________________________________。
(6)进一步探究。查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:
| 实验 编号 | 铜片 质量/g | 0.1mol·L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | _______ | _______ | 实验①和②探究_________的影响;实验①和③探究亚硝酸根的影响。 |
| ② | 5 | 20 | 0.5 | 0 |
| ③ | 5 | 20 | 0 | 0.5 |
-
下图是工业生产硝酸铵的流程。

(1)吸收塔C中通入空气的目的是________ 。
A、B、C、D四个容器中的反应,属于氧化还原反应的是________(填字母)。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H= -1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
写出氨高温催化氧化的热化学方程式:________,
氨催化氧化反应的化学平衡常数表达式K=________。
(3)已知:N2(g)+3H2(g)  2NH3(g) △H=一92 kJ/mol。为提高氢气的转化率,宜采取的措施有________。(填字母)
2NH3(g) △H=一92 kJ/mol。为提高氢气的转化率,宜采取的措施有________。(填字母)
A.升高温度 B.使用催化剂 C.增大压强
D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为33.33%,此时H2的转化率为________。
-
如图是工业生产硝酸铵的流程示意图.

(1)吸收塔C中通入过量空气的目的是______.A、B、C、D四个容器中的反应,属于氧化还原反应的是______(填字母).
(2)已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g),△H=-1266.8kJ/mol;
N2(g)+O2(g)═2NO(g),△H=+180.5kJ/mol
据此写出氨高温催化氧化的热化学方程式:______.
若上述催化氧化过程转移了5mol电子,则反应的能量变化为______kJ.
(3)在化工研究中,经常要判断反应能否自发进行,若某反应的△H<0,则该反应是否一定能自发进行?______(填“一定”或“不一定”)
(4)已知:N2(g)+3H2(g)⇌2NH3(g),△H=-92kJ/mol.为提高氢气的转化率,宜采取的措施有______(填字母).
A.适当升高温度
B.使用更有效的催化剂
C.增大压强
D.循环利用和不断补充氮气
E.及时分离出氨气
(5)在一定温度和压强下,将H2和N2按3:1的体积比在密闭容器中混合,当反应达到平衡时,测得平衡混合气中NH3的体积分数为20.0%,此时H2的转化率为______(计算结果保留一位小数).
-
 由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:
吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇。 回答下列问题:
(1)写出吸收池中反应的离子方程式________。
(2)从分解池中循环使用的物质是________。
(3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g) 请写出该反应的化学平衡常数表达式K=。
CH3CH2OH(g)+H2O(g) 请写出该反应的化学平衡常数表达式K=。
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH 的平衡常数。则由CO制取CH3CH2OH的优点是________________________,
由CO2制取CH3CH2OH的优点是________________________。(写出一点即可)
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:

根据表中数据分析:
① 温度升高,该反应的平衡常数K值(选填“增大”、“减小”或“不变”)。
② 提高氢碳比 ,对生成乙醇(选填“不利”、“有利”或“无影响”)
,对生成乙醇(选填“不利”、“有利”或“无影响”)
-
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇。回答下列问题:
(1)写出吸收池中反应的离子方程式________。
(2)从分解池中循环使用的物质是________。
(3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
写出该反应的化学平衡常数表达式 K=。
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH 的平衡常数。则由CO制取CH3CH2OH的优点是使原料有较大的转化率 ,由CO2制取CH3CH2OH的优点是________。(写出一点即可)
| 
|
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:
根据表中数据分析:
①温度升高,该反应的平衡常数K值________(选填“增大”、“减小”或“不变”);
②提高氢碳n(H2)/n(CO2)比,对生成乙醇________(选填“不利”、“有利”或“无影响”)。
-
下图是工业海水提溴的部分流程,下列有关说法正确的是
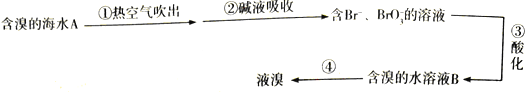
A. “吹出”采用热空气而不是常温空气的原因是热空气氧化性强
B. 碱液吸收所发生的化学反应中氧化剂与还原剂之比为1 : 5
C. 第③ 步中“酸化”要用强氧化性的酸,如硝酸
D. 含溴的水溶液B中的单质溴浓度比A中的大
-
由碳的氧化物直接合成乙醇燃料已进入大规模生产.如图是由二氧化碳合成乙醇的技术流程:

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇. 回答下列问题:
(1)写出吸收池中反应的离子方程式________.
(2)从分解池中循环使用的物质是________.
(3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g)⇌CH3CH2OH(g)+H2O(g) 请写出该反应的化学平衡常数表达式K=________.
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH 的平衡常数.则由CO制取CH3CH2OH的优点是________,
由CO2制取CH3CH2OH的优点是________.(写出一点即可)
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:
温度(K)
CO2转化率(%)
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
根据表中数据分析:
①温度升高,该反应的平衡常数K值________(选填“增大”、“减小”或“不变”).
②提高氢碳比 ,对生成乙醇________(选填“不利”、“有利”或“无影响”)
,对生成乙醇________(选填“不利”、“有利”或“无影响”)
-
(16分)氨、硝酸、硝酸铵、硝酸铜是重要的化工产品。工业合成氨与制备硝酸一般可连续生产,流程如下:

请回答下列问题:
(1)吸收塔中通入空气的作用是 。
下列可以代替硝酸镁加入到蒸馏塔中的是 。
A.浓硫酸 B.氯化钙 C.生石灰 D.硝酸亚铁
(2)制硝酸尾气中的氮氧化物常用尿素[CO(NH2)2]作为吸收剂,其主要的反应为:NO、NO2混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2 和N2,请写出反应的化学方程式 、 。
(3)在氧化炉里,催化剂存在时氨气和氧气反应:
4NH3 + 5O2 4NO + 6H2O 4NH3 + 3O2
4NO + 6H2O 4NH3 + 3O2 2N2+ 6H2O
2N2+ 6H2O
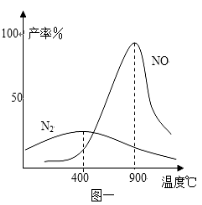
在不同温度时生成产物如图一所示。在氧化炉里,反应温度通常控制在800℃~900℃的理由是 。
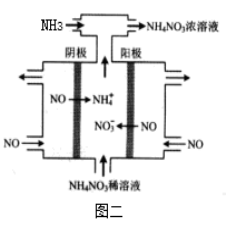
(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为 ,需补充氨气的理由是 。
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2·3H2O,摩尔质量为242g/mol)。已知:25℃、1.01×105 Pa时,在密闭容器发生反应:2NO2 N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100 mol/L。
N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100 mol/L。
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00 L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105 Pa),理论上生成光谱纯硝酸铜晶体的质量为________ g。
-
氨、硝酸、硝酸铵、硝酸铜是重要的化工产品.工业合成氨与制备硝酸一般可连续生产,流程如图1:请回答下列问题
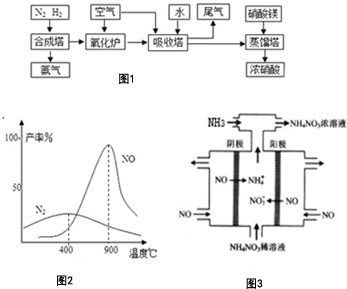
(1)吸收塔中通入空气的作用是 .
下列可以代替硝酸镁加入到蒸馏塔中的是 .
A.浓硫酸 B.氯化钙 C.生石灰 D.硝酸亚铁
(2)制硝酸尾气中的氮氧化物常用尿素[CO(NH2)2]作为吸收剂,其主要的反应为:NO、NO2混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2和N2,请写出反应的化学方程式 、 .
(3)在氧化炉里,催化剂存在时氨气和氧气反应:4NH3+5O2⇌4NO+6H2O 4NH3+302⇌2N2+6H2O 在不同温度时生成产物如图一所示.在氧化炉里,反应温度通常控制在800℃~900℃的理由是 .
(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为 ,需补充氨气的理由是 .
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2•3H2O,摩尔质量为242g/mol).已知:25℃、1.01×105Pa时,在密闭容器发生反应:2NO2⇌N2O4,达到平衡时,c(NO2)=0.0400mol/L,c(N2O4)=0.0100mol/L.
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105Pa),理论上生成光谱纯硝酸铜晶体的质量为 g.
-
如图是工业利用菱镁矿(主要含MgCO3,还含有Al2O3、FeCO3杂质)制取氯化镁的工艺流程。
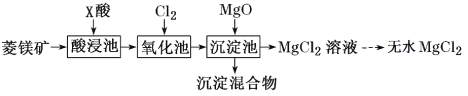
下列说法不正确的是( )
A.酸浸池中加入的X酸是硝酸
B.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
C.沉淀混合物为Fe(OH)3和Al(OH)3
D.在工业上常利用电解熔融氯化镁的方法制取金属镁












