-
已知:①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220kJ·mol-1
②断裂1 mol H2(g)中的H—H键需要吸收436 kJ的能量,断裂1mol O2(g)中的共价键需要吸收496kJ的能量,生成H2O(g)中的1 mol H—O键能放出462 kJ的能量。则下列说法正确的是
A. 断裂1 mol H2O(l)中化学键形成H、O原子的过程中需吸收的能量为924 kJ
B. a的值为-130
C. 2H2(g)+O2(g)=2H2O(g) ΔH =-(220+2a)kJ·mol-1
D. 加入某一催化剂能同等程度降低ΔH1、ΔH2的大小
高二化学选择题中等难度题查看答案及解析
-
已知C(s)+H2O(g)═CO(g)+H2(g)△H=akJ•mol﹣1
2C(s)+O2(g)═2CO(g)△H=﹣220kJ•mol﹣1
H﹣H、O=O和O﹣H键的键能分别为436、496和462kJ•mol﹣1,则a为( )
A.﹣332 B.﹣118 C.+350 D.+130
高二化学选择题中等难度题查看答案及解析
-
已知C(s)+H2O(g)
CO(g)+H2(g) ΔH=AkJ·mol-1
2C(s)+O2(g)
2CO(g) ΔH=-220 kJ·mol-1
H—H、O
O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则A为
A.-332 B.-118 C.+350 D.+130
高二化学选择题中等难度题查看答案及解析
-
已知C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g)
ΔH=-220kJ·mol-1
H—H、O=O和O—H键的键能分别为436kJ·mol
-1、496kJ·mol-1和462 kJ·mol-1,则a为( )
A.+130 B.-118 C.+350 D.-332
高二化学选择题中等难度题查看答案及解析
-
已知:C(s)+H2O (g)=CO(g)+H2(g) ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH= -220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
A.-332 B.-118 C.+350 D.+130
高二化学选择题中等难度题查看答案及解析
-
已知:C(s)+H2O(g) =CO(g)+H2(g)ΔH=akJ·mol-1
2C(s)+O2(g) =2CO(g) ΔH=-220 kJ·mol-1
H—H、O=O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为( )
A. -332 B. -118 C. +350 D. +130
高二化学选择题困难题查看答案及解析
-
在密闭容器中进行反应①Fe(s)+CO2(g)
FeO(s)+CO(g) ΔH1=akJ·mol-1
反应②2CO(g)+O2(g)
2CO2(g) △H2=b kJ·mol-1
反应③2Fe(s)+O2(g)
2FeO(s) △H3
(1)△H3=_____________________________(用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K=_________________________,已知500℃时反应①的平衡常数K=1.0,在此温度下2 L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为_____________________________,CO的平衡浓度为_____________________________。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a_____0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有_____________________________(填序号)。
A.缩小反应器体积 B.再通入CO2 C.升高温度 D.使用合适的催化剂
(4)在密闭容器中,对于反应:2SO2(g)+O2(g)
2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量为_____________,其转化率为____________。
高二化学填空题中等难度题查看答案及解析
-
在密闭容器中进行反应①Fe(s)+CO2(g)
FeO(s)+CO(g) ΔH1=akJ·mol一1
反应②2CO(g)+O2(g)
2CO2(g) △H2=b kJ·mol-1
反应③2Fe(s)+O2(g)
2FeO(s) △H3
(1) △H3= (用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K= ,已知500℃时反应①的平衡常数K=1.0,在此温度下2 L密闭容器中进行反应①,Fe和CO2的起始量均为2.0 mol,达到平衡时CO2的转化率为 ,CO的平衡浓度为 。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有 (填序号)。
A.缩小容器的体积 B.再通入CO2
C.升高温度 D.使用合适的催化剂
(4)下列图像符合反应①的是 (填序号)(图中V是速率、φ为混合物中CO含量,T为温度)。
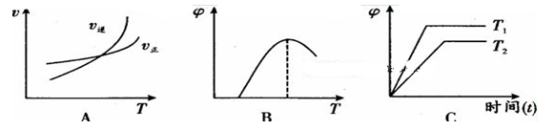
高二化学填空题极难题查看答案及解析
-
已知C(s)+H2O(g)=CO(g)+H2(g) △H=akJ·mol-1 2C(s)+O2(g)=2CO(g) △H=-220kJ·mol-1,H—H、O=O和O—H键的键能分别为436、496、462 kJ·mol-1,则a为
A.-332 B.-118 C.+350 D.+130
高二化学选择题简单题查看答案及解析
-
在25℃、101KPa时,已知反应:①2C(s)+O2(g)=2CO(g) △H=-akJ/mol ②稀溶液中,H+(aq)+OH-(aq)=H2O(1) △H=-bkJ/mol (a、b 均大于0),下列结论正确的是
A. ①的反应热为a kJ/mol
B. 碳的燃烧热大于a/2 kJ/mol
C. 稀硫酸与稀NaOH溶液反应的中和热为-b kJ/mol
D. 稀醋酸与稀NaOH溶液反应生成1mol水,放出b kJ热量
高二化学单选题中等难度题查看答案及解析