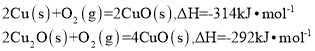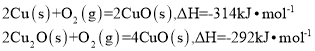-
Cu2O主要用于制造船底防污漆,它是一种鲜红色粉末,几乎不溶于水,在湿空气中逐渐氧化成黑色氧化铜。用含NaOH的Na2SO3溶液还原CuSO4制备Cu2O的工艺流程如下:
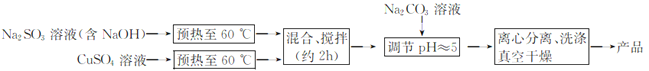
回答下列问题:
(1)流程中涉及的化学反应主要包括:
Ⅰ.Cu2++2OH-=Cu(OH)2↓;Ⅱ.生成CuOH;Ⅲ.2CuOH=Cu2O+H2O。
写出第Ⅱ步反应的离子方程式: ______________________________。
(2)其他反应条件相同时,测得反应时间和溶液的pH对Cu2O产率的影响如下图所示:
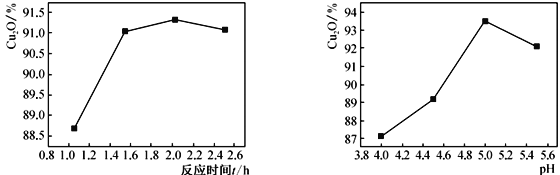
①反应时间超过2h时,Cu2O产率开始降低其原因是____________________________。
②pH<5时,Cu2O产率随pH减小而减小,产品中铜含量增加明显,其原因是______________________(用离子方程式说明)。
(3)为测定产品中Cu2O的含量,称取3.96 g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,至终点时消耗50mL标准液。
①滴定时应选用______(填“酸式”或“碱式”)滴定管,滴定终点的现象是______________________。
②产品与硫酸酸化的Fe2(SO4)3溶液反应的离子方程式为________________________________。
③假定杂质不参与反应,产品中Cu2O的质量分数为_______________。
-
Cu2O是一种鲜红色粉末状固体,几乎不溶于水,在酸性溶液中歧化为二价铜和铜单质。可用于制造船底防污漆等。某校合作学习小组的同学设计实验验证其某些性质及其胶体的制法。回答下列问题:
(1)甲组同学检验H2还原CuO所得的红色粉末中是否有Cu2O。取反应产物少许加入试管中,加入足量的试剂X并搅拌,若发现溶液变蓝且仍有剩余固体,则试剂X可选用_____(填序号)。
A.FeCl3溶液 B.硝酸 C.稀硫酸 d.H2O2酸性溶液
(2)乙组同学在两支试管中分别加入少量Cu2O,一支中加入稀硝酸,固体溶解同时产生NO气体,Cu2O表现_______________性;另一支加入硫酸酸化的KMnO4溶液,溶液紫色褪去得蓝色溶液,反应的离子方程式为______________。
(3)丙组同学取少量Cu2O与黑色的Cu2S混合加强热,产生大量的气体同时得到红色固体粉末,该反应的化学方程式为____________________。
(4)丁组同学向0.1mol·L-1 的(CH3COO)2Cu溶液中加入0.02mol·L-1的N2H4的水溶液,控制pH=7~8,得到红色透明液体,能说明该分散系属于胶体的简单方法是____________。已知制备过程中有N2放出,制备反应的化学方程式为________________。
-
Cu2O是一种鲜红色粉末状固体,几乎不溶于水,在酸性溶液中歧化为二价铜和铜单质。可用于制造船底防污漆等。某校合作学习小组的同学设计实验验证其某些性质及其胶体的制法。回答下列问题:
(1)甲组同学检验H2还原CuO所得的红色粉末中是否有Cu2O。取反应产物少许加入试管中,加入足量的试剂X并搅拌,若发现溶液变蓝且仍有剩余固体,则试剂X可选用_____(填序号)。
A.FeCl3溶液 B.硝酸 C.稀硫酸 d.H2O2酸性溶液
(2)乙组同学在两支试管中分别加入少量Cu2O,一支中加入稀硝酸,固体溶解同时产生NO气体,Cu2O表现_______________性;另一支加入硫酸酸化的KMnO4溶液,溶液紫色褪去得蓝色溶液,反应的离子方程式为______________。
(3)丙组同学取少量Cu2O与黑色的Cu2S混合加强热,产生大量的气体同时得到红色固体粉末,该反应的化学方程式为____________________。
(4)丁组同学向0.1mol·L-1 的(CH3COO)2Cu溶液中加入0.02mol·L-1的N2H4的水溶液,控制pH=7~8,得到红色透明液体,能说明该分散系属于胶体的简单方法是____________。已知制备过程中有N2放出,制备反应的化学方程式为________________。
-
Cu2O是一种鲜红色粉末状固体,几乎不溶于水,在酸性溶液中歧化为二价铜和铜单质。可用于制造船底防污漆等。某校合作学习小组的同学设计实验验证其某些性质及其胶体的制法。回答下列问题:
(1)甲组同学检验H2还原CuO所得的红色粉末中是否有Cu2O。取反应产物少许加入试管中,加入足量的试剂X并搅拌,若发现溶液变蓝且仍有剩余固体,则试剂X可选用_________(填序号)。
a.FeCl3溶液 b.硝酸 c.稀硫酸 d. H2O2酸性溶液
(2)乙组同学在两支试管中分别加入少量Cu2O,一支中加入稀硝酸,固体溶解同时产生NO气体,Cu2O表现_______________性;另一支加入硫酸酸化的KMnO4溶液,溶液紫色褪去得蓝色溶液,反应的离子方程式为______________。
(3)丙组同学取少量Cu2O与黑色的Cu2S混合加强热,产生大量的气体同时得到红色固体粉末,该反应的化学方程式为____________________。
(4)丁组同学向0.1mol·L-1 的(CH3COO)2Cu溶液中加入0.02mol·L-1的N2H4的水溶液,控制pH=7~8,得到红色透明液体,能说明该分散系属于胶体的简单方法是____________。已知制备过程中有N2放出,制备反应的化学方程式为________________。
-
Cu2O可用于制作船底防污漆,某学习小组探究制备Cu2O的方法。
【查阅资料】
① CuSO4与Na2SO3溶液混合可制备Cu2O。
② Cu2O为砖红色固体;酸性条件下生成Cu2+和Cu。
③ Cu2O和Cu(SO3)23-可以相互转化
(1)配制0.25 mol·L-1CuSO4溶液和0.25 mol·L-1 Na2SO3溶液。测得CuSO4溶液pH=4,Na2SO3溶液pH=9。用离子方程式表示CuSO4溶液pH=4的原因_________________。
(2)完成CuSO4溶液和Na2SO3溶液反应制Cu2O的离子方程式:

【实验探究】
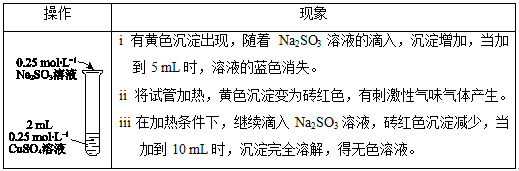
(3)证明ii中砖红色沉淀是Cu2O的实验方案是____________。
(4)经检验i中黄色沉淀含有Cu2SO3,ii中沉淀由黄色变砖红色的化学方程式是___________。
(5)iii中砖红色沉淀消失的原因是____________。
(6)在加热条件下,若向2 mL 0.25 mol·L-1Na2SO3溶液中滴加0.25 mol·L-1CuSO4溶液至过量,预期观察到的现象是____________。
(7)由上述实验得出结论:CuSO4溶液和Na2SO3溶液反应制备Cu2O,应控制的条件是_______、_______。
-
保险粉又称连二亚硫酸钠(Na2S2O4),可用于纺织工业的漂白剂、脱色剂,脱氯剂。Na2S2O4是白色粉末,无味,易溶于水、难溶于乙醇,具有极强的还原性,在空气中易被氧化,在碱性介质中稳定。
Ⅰ.甲酸钠( HCOONa) 法制备过程如下:

(1)连二亚硫酸钠中硫元素的化合价为______________。
(2)实验室用Na2SO3 固体和某酸反应制备SO2气体,制备SO2时所选用的酸,你认为下列最适宜选用的是______________。
A.浓盐酸 B.浓硝酸
C.质量分数为70%的硫酸 D.质量分数为10%的硫酸
(3)步骤①中制备连二亚硫酸钠的化学方程式可表示为____________________________。
(4)上述步骤②中,加入适量乙醇水溶液的作用是______________。
(5)在包装保存“保险粉”时加入少量的Na2CO3固体,目的是_________________________。
(6)①现将0.05mol/L Na2S2O4溶液在空气中放置,其溶液的pH 与时间(t)的关系如图所示。

t1时溶液中只有NaHSO3一种溶质,此时含硫元素的粒子浓度由大到小的顺序为_______________。
②t1~t2段发生化学反应的离子方程式为______________________________。
Ⅱ.电解法制备:工业上用惰性电极电解NaHSO3溶液得到Na2S2O4。过程如图所示
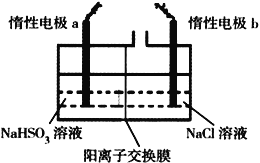
(7) ①产品在_________________(填“阳极”、“阴极”)得到。
②若不加隔膜,则连二亚硫酸钠产率降低,其原因是__________________________________。
-
(14分)铜是一种常见的金属元素,其有多种用途广泛的化合物。
I、氯化亚铜(CuCl)是一种白色粉末,不溶于乙醇,微溶于水,易溶于浓盐酸,露置在空气中迅速被氧化成碱式盐。可用于一氧化碳、乙炔等气体含量的测定。以粗铜(含Cu、Fe)为原料可制备纯净的CuCl,其流程如下:
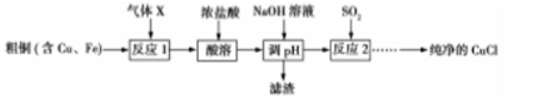
(1)气体X的化学式 ,“酸溶”采用浓盐酸的原因是 。
(2)“酸溶”所得溶液成分分析:c(CuCl2)=5mol·L-1,c(FeCl3)=1 mol·L-1。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=4.8×10-20,当溶液中金属离子的浓度小于10-5 mol·L-1时可认为其沉淀完全,则上述流程中滴加NaOH溶液调节pH,其范围约为 (数值取整数)。
(3)反应2的离子方程式为 。
(4)设计实验提纯析出的CuCl粗晶体: 。
II、纳米氧化亚铜(Cu2O)可用作光电材料,可用电解法制得(如图)。酸性介质中Cu2O不能稳定存在,潮湿的空气中可缓慢被氧化成CuO。
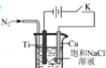
(5)阳极的电极反应式为: 。
(6)电解过程中从烧杯底部通入N2,其可能的作用:
①搅动溶液,使OH-迅速扩散;② 。
-
氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取 ,已知反应:
,已知反应:
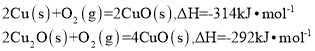
则 的
的 等于
等于
A.  B.
B. 
C.  D.
D. 
-
氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取 ,已知反应:
,已知反应:
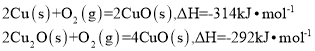
则 的
的 等于
等于
A.  B.
B. 
C.  D.
D. 
-
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校化学实验小组通过实验探究某红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4。
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
(1)若只有Fe2O3,则实验现象是_____________。
(2)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则此过程中的离子反应为:
____________________________。
(3)经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物。实验小组欲测定Cu2O的质量分数。已知Cu2O在空气中加热生成CuO。
测定流程:
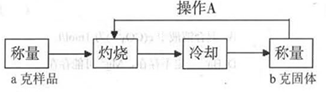
实验中操作A的名称为_____________。
灼烧过程中,所需仪器有:酒精灯、玻璃棒、_____________等(夹持仪器除外)。
(4)写出混合物中Cu2O的质量分数的表达式_____________。
实验小组欲利用红色粉末制取较纯净的胆矾(CuSO4•5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
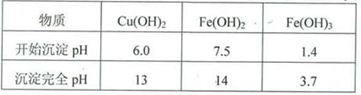
实验室有下列试剂可供选择:A.氯水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
实验小组设计如下实验方案制取胆矾:

(5)用试剂编号表示:试剂l为_____________,试剂2为_____________。
(6)为什么先“氧化”后“调节pH”?pH控制范围为多少?__________________________________