-
工业上常利用含硫废水生产海波Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
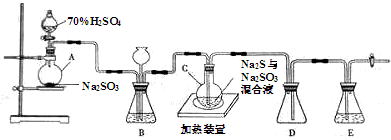
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (Ⅰ)
2H2S+SO2=3S+2H2O (Ⅱ)
S+Na2SO3 Na2S2O3 (Ⅲ)
Na2S2O3 (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若_________,则整个装置气密性良好.装置D的作用是__________,装置E中为__________溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为__________;
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择__________;
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,实验中,为使SO2缓慢进入烧瓶C,采用的操作是__________;已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是__________;反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有__________;
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂(稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液)设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:__________;
已知Na2S2O3•5H2O遇酸易分解:S2O32-+2H+=S↓+SO2↑+H2O,
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液。
-
工业上常用含硫废水生产Na2S2O3•5H2O,实验室可用如图装置(略去部分夹持仪器)模拟生产过程.
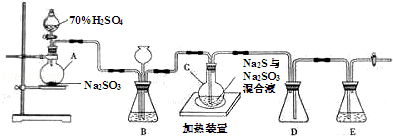
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)  Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)仪器A的名称 ,仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好.装置E中为 溶液.
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 .
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是 .反应后期可用酒精灯适当加热仪器A,实验室用酒精灯加热时必须使用石棉网的仪器还有 .
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(3)反应终止后,仪器C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论 .
已知Na2S2O3•5H2O遇酸易分【解析】
S2O 32﹣+2H+═S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
-
工业上常利用含硫废水生产Na2S2O3·5H2O,实验室用如下装置(略去部分夹持仪器)模拟生成过程。
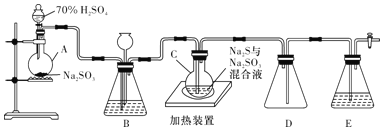
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)═Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)═3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)  Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若____________,则整个装置气密性良好,装理D的作用是___________。装置E中为_________________溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则理论上烧瓶C中Na2S和Na2SO3的物质的量之比为____________。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择__________(填字母代号)。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是___________________。已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是____________________________________。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器有_____________。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:__________________________________。(已知Na2S2O3•5H2O遇酸易分【解析】
S2O32- + 2H+ =S↓+ SO2↑+ H2O)
-
(10分)工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。

(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)装置A中反应的化学方程式为 。
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (I)
2H2S+SO2=3S+2H2O (II)
S+Na2SO3 Na2S2O3 (III)
Na2S2O3 (III)
为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
-
下图是实验室制取Na2S2O3·5H2O的装置图(略去部分夹持仪器)。
已知:Na2SO3 +S Na2S2O3
Na2S2O3

按要求回答下列问题:
(1)仪器A的名称是___________________。
(2)分液漏斗中用70%较浓硫酸的理由是___________________。
(3)装置C中生成S的离子反应方程式是___________________。
(4)E是SO2的尾气处理装置,则装置D的作用是___________________。
-
工业以浓缩海水为原料提取溴的部分过程如下:
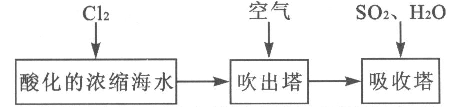
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
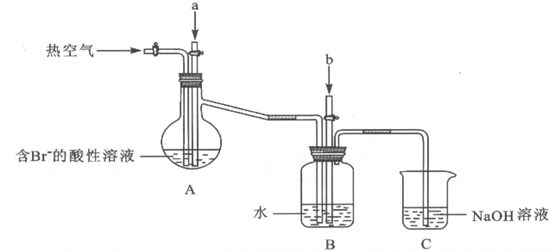
(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)_______________。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是__________________。
(3)反应过程中,B装置中Br2与SO2反应的化学方程式____________________。
(4)C装置的作用是___________________。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用____________________方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是____________________。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是:取出少量溶液,先加入过量新制氯水,再加入KI淀粉溶液,观察溶液是否变蓝色。
该方案是否合理并简述理由:____________________。
-
溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
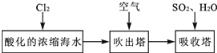
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)
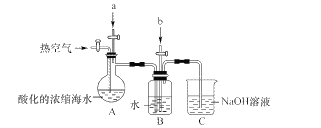
(1)A装置中通入a气体的目的是(用离子方程式表示)____。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是____。
(3)B装置中通入的b气体是____,目的是使溴蒸气转化为氢溴酸以达到富集的目的,试写出该反应的化学方程式____。
(4)C装置的作用是____。
-
溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
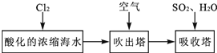
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)
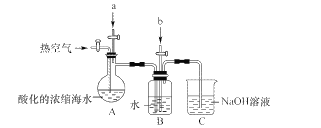
(1)A装置中通入a气体的目的是(用离子方程式表示)____。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是____。
(3)B装置中通入的b气体是____,目的是使溴蒸气转化为氢溴酸以达到富集的目的,试写出该反应的化学方程式____。
(4)C装置的作用是____。
-
(14分)实验室可用如下装置(略去部分夹持仪器)制取SO2并验证其性质。
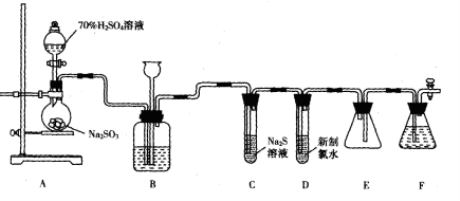
(1)盛装70%H2SO4溶液的仪器名称为_______。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若_______,则整个装置气密性良好。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择_______(填代号)。
a.蒸馏水 b.饱和Na2CO3溶液
c.饱和NaHSO3 溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加人品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案合理的是方案_______(填“I”、“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为__________________________________________.
(5)装置E的作用是_______。装置F中为_______溶液。
-
溴苯是一种化工原料,实验室用苯和液溴合成溴苯的装置示意图如下。(夹持仪器已略去)
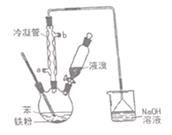
请回答以下问题。
(1)制取溴苯的化学方程式是________,反应过程中烧瓶内有白雾产生,是因为生成_____了气体。
(2)该实验中用到冷凝管,由此猜想生成溴苯的反应属于____________反应(填“放热”或“吸热”);使用冷凝管时,进水口应是____________(填“a”或“b”);烧杯中NaOH溶液的作用是________(答一条即可)。
(3)该实验中将液溴全部加入苯中,充分反应后,为提纯溴苯,进行以下操作:
①继续向烧瓶中加入少量水,然后过滤除去未反应的铁屑,过滤时必须用到的玻璃仪器是烧杯、玻璃棒、____________。
②滤液在经一系列处理,最终得到的粗溴苯中仍含有少量苯,要进一步提纯溴苯,可进行的操作_____(填序号)。
| | 苯 | 溴苯 |
| 沸点/℃ | 80 | 156 |
| 水中溶解度 | 微溶 | 微溶 |
A.重结晶 B.过滤 C.蒸馏

Na2S2O3 (Ⅲ)











