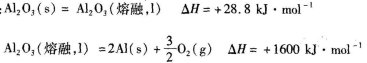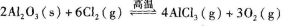-
铝和氢氧化钾都是重要的工业产品,请回答问题:
(1)金属铝的生产是以Al2O3为原料,在熔融状态下进行电解,化学方程式为

电极均由石墨材料做成,电解时不断消耗的电极是____________(填“阴极”或“阳极”),
原因是__________________________ (用化学方程式表示)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命。以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为____________________ 。
(3)铝电池性能优越,Al—Ag2O电池可用作水下动力电源,化学反应为

则负极的电极反应式为______________,正极附近溶液的碱性______(填“增强”、“不变”或“减弱”)。
(4)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
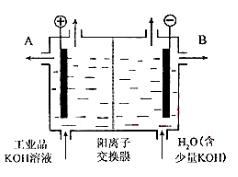
①该电解槽的阳极反应式是 。
②阴极区碱性增强的原因是
③除去杂质后的氢氧化钾溶液从液体出口 (填写“A”或“B”)导出。
-
工业上金属铝的生产是以Al2O3为原料,在熔融状态下进行电解流程如下:2Al2O 3
 4Al+3O2
4Al+3O2
注:冰晶石的作用是使E在较低温度下熔化.
请回答下列问题:
(1)冰品石(Na3AlF6)的作用是______..
(2)铝的最外层电子数______,在周期表中的位置是______.
(3)电解生成的金属铝是在熔融液的______(填“上层”或“下层”).阴极和阳极均由______材料做成;电解时所消耗的电极是______(填“阳极”或“阴极”).
(4)在标准状况下产生67.2L氧气,可得到金属铝______克.
-
下列叙述正确的是
A.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
B.加水稀释溶液,溶液中的所有离子浓度都减小
C.金属铝的生产是以Al2O3为原料,在熔融状态下进行电解
D.NaHCO3溶液中含有少量Na2CO3可以用澄清石灰水除去
-
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.工业上电解熔融Al2O3制备金属铝
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.金属锌与稀硫酸反应制取氢气,粗锌比纯锌反应速率快
D.电解MgCl2饱和溶液,可制得金属镁
-
(14分)用电化学原理研究金属铝具有重要的意义。
(1)已知:
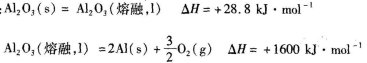
①工业上利用惰性电极电解熔融的Al2O3冶炼铝,每消耗1000kJ电能时,生成27g铝,则电解过程中能量利用率为____。

③利用Al2O3制备无水AlCl3的反应为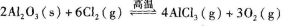
 。反应达平衡时,加入焦炭能使平衡向正反应方向移动,理由是__________.
。反应达平衡时,加入焦炭能使平衡向正反应方向移动,理由是__________.
(2)为了防止钢材腐蚀,常采用电解熔融盐法在钢材表面镀铝。熔融盐中铝元素和氯元素仅以 形式存在。如下图所示:
形式存在。如下图所示:
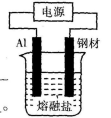
①钢材表面镀铝时,铝应接电源的________极。
②试分析电镀铝时不用氯化铝水溶液作电解液的原因:_______________.
(3)铝一空气-NaOH溶液组成的铝电池性能优越,可用于电动汽车。写出该电池的负极电极反应式______:
(4)铝可用于处理银器表面的黑斑(Ag2S)。将银器置于铝制容器里的食盐水中并与铝接触,形成原电池,可将Ag2S转化为Ag,该过程中食盐水的作用为_______________.
-
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.工业上电解熔融Al2O3制备金属铝
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.金属锌与稀硫酸反应制取氢气,粗锌比纯锌反应速率快
D.电解MgCl2饱和溶液,可制得金属镁
-
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下: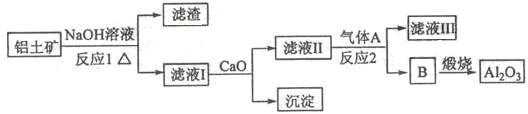
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下: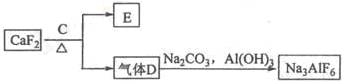
回答下列问题:
(1)写出反应1的化学方程式___________________________ ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为_______________ ;
(3)E可作为建筑材料,化合物C是_____ ,写出由D制备冰晶石的化学方程式 ____________;
(4)电解制铝的化学方程式是 _____________________________________,以石墨为电极,阳极产生的混合气体的成分是 _________________。
-
下列处理方法正确的是
A.为除去污水中的重金属离子Hg2+,向其中加入足量充分反应后过滤
B.为降低能耗,工业电解熔融态的Al2O3制Al时,加入冰晶石
C.为充分利用原料,氯碱工业中,将阳极室的饱和氯化钠溶液电解为水后导出
D.为保护公路两旁的铁护栏,将其与电源的负极相连
-
铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是 。
(2)铝与氢氧化钾溶液反应的离子方程式是 。
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
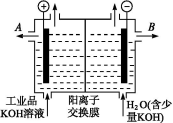
①该电解槽的阳极反应式是 。
②通电开始后,阴极附近溶液pH会增大,请简述原因 。
③除去杂质后的氢氧化钾溶液从溶液出口 (填写“A”或“B”)导出。
-
(16分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为________。
(2)SO42ˉ的立体构型是________,其中S原子的杂化轨道类型是________。
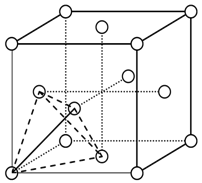
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子外围电子排布式为________。一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为________,该晶体中,原子之间的作用力是________。
(4)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如下图),该晶体储氢后的化学式应为________;假设在另一条件下,氢原子可进入到由Cu原子与Au原子构成的八面体空隙中心,该晶体储氢后的化学式为________。(提示:查找四面体、八面体时,需假设Cu原子与Au原子等同;每个四面体、八面体内只填充一个氢原子)