-
下列处理方法正确的是
A.为除去污水中的重金属离子Hg2+,向其中加入足量充分反应后过滤
B.为降低能耗,工业电解熔融态的Al2O3制Al时,加入冰晶石
C.为充分利用原料,氯碱工业中,将阳极室的饱和氯化钠溶液电解为水后导出
D.为保护公路两旁的铁护栏,将其与电源的负极相连
高二化学选择题简单题查看答案及解析
-
下列关于金属冶炼的说法正确的是
A. 由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al
B. 可以用钠加入氯化镁饱和溶液中制取镁
C. 炼铁高炉中所发生的反应都是放热的,故无需加热
D. 金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A.Al-Mg合金焊接过程中使用的保护气为N2
B.工业上可采用电解熔融NaCl的方法制备金属钠
C.将0.5molN2和1.5molH2充入一密闭容器中充分反应,放出热量19.6KJ,
则该热化学方程式为N2(g) + 3 H2(g)
2NH3(g) △H= —39.2 KJ·mol-1
D.已知:2H2(g) + O2(g)
2H2O(g) △H= —486 KJ·mol-1 ,则H2 的燃烧热△H为—243 KJ·mol-1
高二化学选择题简单题查看答案及解析
-
镁、铝及其化合物在生产生活中具有重要的应用.回答下列问题:
(1)工业上冶炼金属镁是采用惰性电极电解熔融MgCl2的方法,此时阴极的电极反应式为:______;
(2)除去MgCl2溶液中的Fe2+,常加入少量H2O2,使Fe2+氧化为Fe3+,然后加入少量碱性物质至溶液pH=4,此时c(Fe3+)=______mol/L[已知Fe(OH)3的Ksp=4×10﹣38]
(3)工业上冶炼金属铝则是采用惰性电极电解熔融Al2O3的方法,关于为什么不采用电解熔融AlCl3的方法的叙述正确的是______(选择填空):
A.AlCl3是非电解质 B.AlCl3水溶液不导电 C.AlCl3是共价化合物 D.AlCl3熔点太高
(4)用碳棒做电极电解熔融Al2O3时,阳极需要定期更换,其原因是________(用电极反应式和化学方程式回答);
(5)已知:Al2O3(熔融,l)=2Al(s)+3/2O2(g)△H=1600KJmol﹣1工业上利用惰性电极电解熔融Al2O3冶炼铝,每消耗1000kJ电能时,生成27gAl,则电解过程中能量利用率为_______.
(6)明矾的化学式为KAl(SO4)212H2O,它可以作为净水剂,用离子方程式表示其能够净水的原因______;向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH___7(填>、<、=);
(7)若在空气中加热固体MgCl2•6H2O,可水解生成Mg(OH)Cl,写出相关的化学方程式______,所以,为了抑制MgCl2•6H2O在加热时水解,可在干燥的______气流中加热,可得到无水氯化镁.
高二化学综合题中等难度题查看答案及解析
-
工业生产中,降低能耗是重要的节能措施。可以通过合理设计工艺路线,优化工艺条件,从而达到降低能耗的目的。下列措施不能达到降低能耗的目的的是
A. 在N2与H2合成氨工业中,使用催化剂
B. 电解熔融氧化铝制取铝,在氧化铝中加冰晶石
C. 陶瓷烧制时,用煤炭代替瓦斯(主要成分CH4)作燃料
D. 接触法生产H2SO4的过程中,在接触室中采用热交换器
高二化学单选题简单题查看答案及解析
-
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的某试剂充分反应,过滤结晶即可;②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶解,再加入适量的氢氧化镁,充分反应,过滤结晶即可;③为了除上硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为_____________(填化学式)而除去。
(2)①中加入的试剂应该选择_____为宜。
(3)②中除去Fe3+所发生的总反应的离子方程式:______________________________。
(4)下列与方案③相关的叙述中,正确的是__________(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.在pH<4 的溶液中Fe3+一定不能大量存在
C.调节溶液pH=4 可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4 的溶液中
高二化学实验题困难题查看答案及解析
-
对于金属冶炼的工业方法,下列有关说法中正确的是
A.可用电解饱和的MgCl2溶液的方法获得金属镁
B.电解CuSO4溶液精炼金属铜时,用铁做阳极
C.电解熔融Al2O3方法冶炼金属铝时,同时要加入冰晶石作助熔剂
D.工业上常采用活泼金属还原法冶炼金属银
高二化学选择题中等难度题查看答案及解析
-
工业废水中常含有酚类、重金属、氰类、三氯甲烷及砷类等有害物质,必须处理后才可排放。
(1)用FeS除去废水中重金属汞盐的反应为Hg2++FeS
HgS + Fe2+,该反应的平衡常数为K=____________ [填数值,已知:Ksp(FeS)=6.4×10-15,Ksp(HgS)=1.6×10-52]。
(2)处理含CN-废水有惰性电极电解法、NaClO氧化法等。
已知:HCN的Ka=6.3×10-10,沸点为25.7℃,有剧毒。
①电解前需将废水的pH调至10~11,其目的是___________。
②惰性电极电解时,CN-在阳极最终氧化为CO32-、CO2和N2。则1mol CN-在阳极被完全氧化,同时在阴极上产生H2的物质的量为___________(不考虑副反应)。
③电解后期需在废水中加入食盐继续电解,加食盐除可提高电流效率外,还因为___________。
(3)纳米零价铁除去酸性废水中的三氯乙烯、五价砷的原理如下图所示:
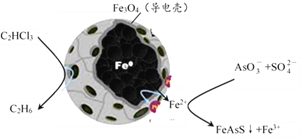
纳米零价铁中Fe为负极, C2HCl3在其表面被还原的电极反应式为___________;在含高浓度SO42-的酸性溶液中脱除砷的化学方程式为___________。
高二化学综合题困难题查看答案及解析
-
下列叙述正确的是( )
A.工业上用电解熔融氯化钠的方法制取钠
B.碳在高温下能还原氧化镁中的镁
C.钠加入氯化镁的饱和溶液中可以制取金属镁
D.电解冶炼铝的原料是氯化铝
高二化学单选题简单题查看答案及解析
-
常温下,以 MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+杂质离子,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀然后过滤除去,下列说法正确的是( )
A. 加入MnS后生成CuS的离子方程式是Cu2++S2﹣=CuS↓
B. 滤渣中含有四种难溶电解质
C. 加入过量MnS的目的是为了使MnS与Cu2+、Pb2+、Cd2+的反应正向移动
D. 若CuS比PbS的Ksp小,则 Cu2+先于Pb2+沉淀
高二化学单选题中等难度题查看答案及解析