-
已知重铬酸钾(K2Cr2O7)具有强氧化性,其还原产物Cr3+在水溶液中呈绿色或蓝绿色。在K2Cr2O7溶液中存在下列平衡:Cr2O72−(橙色) + H2O 2CrO42−(黄色) + 2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是( )
2CrO42−(黄色) + 2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是( )
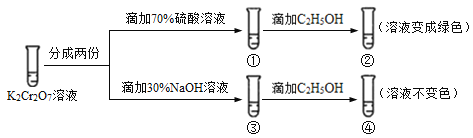
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72−被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
-
已知在K2Cr2O7的溶液中存在着如下平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+,加入下列物质能使溶液变为橙色的是( )
A.氨水 B.硫酸 C.NaOH D.水
-
已知在K2Cr2O7的溶液中存在着如下平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+,加入下列物质能使溶液变为橙色的是( )
A. 氨水 B. 硫酸 C. NaOH D. 水
-
在水溶液中橙色的Cr2O72-与黄色的CrO42-有下列平衡关系:Cr2O72-+H2O 2CrO42-+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
2CrO42-+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
(1)向上述溶液中加入NaOH溶液,溶液呈___色。因为___。
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈__色,因为___。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡___(填“向左移动”或“向右移动”)。
-
Ⅰ.在水溶液中橙色的Cr2O72—与黄色的CrO42—有下列平衡关系:Cr2O72—+H2O 2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。
(1)向上述溶液中加入NaOH溶液,溶液呈________色,因为_________________。
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈_____色,因为________。
Ⅱ.现有浓度均为0.1 mol/L的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)若三种溶液中c(H+)分别为x1 mol/L、x2 mol/L、x3 mol/L,则它们的大小关系为_______。
(2)等体积的以上三种酸分别与过量的NaOH溶液反应,消耗NaOH的物质的量依次为y1 mol、y2 mol、y3 mol,则它们的大小关系为______。
(3)在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况图所示,回答下列问题。
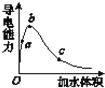
①a、b、c三点醋酸电离程度由大到小的顺序为____;a、b、c三点对应的溶液中c(H+)最大的是_____。
②若实验测得c点处溶液中c(CH3COOH)=0.01 mol·L-1,c(CH3COO-)=0.0001 mol·L-1,则该条件下CH3COOH的电离常数Ka=____。
③在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是(__)。
A.c(H+) B.溶液pH C. D. CH3COOH分子数
D. CH3COOH分子数
-
在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:
Cr2O72- + H2O  2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42- + 2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
⑴向上述溶液中加入NaOH溶液,溶液呈__________色,因为____________________________________。
⑵向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈________色,
因为__________________。
⑶向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡___________, 溶液颜色将_______。
-
(8分)在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系.
Cr2O72-+H2O 2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈________色,因为________。
(2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈________色,
因为________。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡________,溶液颜色将________。
-
(6分)在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系.
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈________色,因为。
(2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈________色,因为________。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡向________方向移动,溶液颜色将________。(填“变深”、“变浅”或“不变”)
-
(6分)在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液, 溶液呈橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液, 溶液呈橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈_______色,平衡________。(填“向左移”或“向右移”,下同。)
(2)再加入过量稀H2SO4,则溶液呈_______色,平衡________。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡_______________,溶液颜色将__________。
-
(6分)在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液, 溶液呈橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液, 溶液呈橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈_______色,平衡________。(填“向左移”或“向右移”,下同。)
(2)再加入过量稀H2SO4,则溶液呈_______色,平衡________。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡_______________,溶液颜色将__________。
2CrO42—+2H+,重铬酸钾(K2Cr2O7)溶于水配成的稀溶液是橙黄色的。

D. CH3COOH分子数
