某市售盐酸试剂瓶标签上的部分信息如下:

(1)该盐酸的物质的量浓度为__________ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)=____mol·L-1。
(3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是____ L。
高一化学计算题简单题
某市售盐酸试剂瓶标签上的部分信息如下:

(1)该盐酸的物质的量浓度为__________ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)=____mol·L-1。
(3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是____ L。
高一化学计算题简单题
某市售盐酸试剂瓶标签上的部分信息如下:

(1)该盐酸的物质的量浓度为__________ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)=____mol·L-1。
(3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是____ L。
高一化学计算题简单题查看答案及解析
某市售盐酸试剂瓶标签上的部分信息如下:
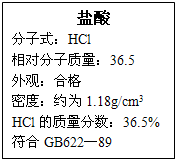
盐酸
分子式:HCl
相对分子质量:36.5
密度约1.18 g·mL-1
HCl的质量分数:36.5%
(1)该盐酸的物质的量浓度c(HCl)=__ mol·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中(HCl)= ___mol·L-1。
(3)取稀释后盐酸溶液100mL,该溶液中所含的氯离子的个数为:N(Cl—)=___NA
(4)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 mol氢气,在标准状况下气体的体积是___L。
高一化学计算题中等难度题查看答案及解析
某市售盐酸试剂瓶标签上的部分信息如下:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度约1.18 g·mL-1 HCl的质量分数:36.5% |
(1)该盐酸的物质的量浓度= ,从中取出100ml,所含HCl的物质的量为 ,所含Cl-的质量为 。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中C(HCl)= ,从中取出10ml,其浓度为 。
(3)取稀释后的盐酸与足量锌粒作用,生成是 。
高一化学填空题困难题查看答案及解析
如图是某市售盐酸试剂瓶标签上的部分数据.则该盐酸的物质的量浓度是( )

A. 3 mol/L B. 8.4 mol/L C. 11.8 mol/L D. 0.5 mol/L
高一化学单选题中等难度题查看答案及解析
如图是某市售盐酸试剂瓶标签上的部分数据.则该盐酸的物质的量浓度是( )

A. 3 mol/L B. 8.4 mol/L C. 11.8 mol/L D. 0.5 mol/L
高一化学选择题中等难度题查看答案及解析
如图是某市售盐酸试剂瓶标签上的部分数据.则该盐酸的物质的量浓度是( )

A. 3 mol/L B. 8.4 mol/L C. 11.8 mol/L D. 0.5 mol/L
高一化学选择题中等难度题查看答案及解析
如图是某市售盐酸试剂瓶标签上的部分数据.则该盐酸的物质的量浓度是( )
A.3 mol/L B.8.4 mol/L C.11.8 mol/L D.0.5 mol/L
高一化学选择题中等难度题查看答案及解析
右图为某浓盐酸试剂瓶标签上的部分内容,请回答下列问题。

(1)该浓盐酸中HCl 的物质的量浓度为 mol/L;
(2)某同学欲用此浓盐酸和蒸馏水配置480mL 浓度为0.4mol/L 的稀盐酸。
①配置稀盐酸时,可供选用的仪器有:
A胶头滴管 B玻璃棒 C烧杯 D药匙 E量筒 F托盘天平 G容量瓶
完成该实验所需的仪器是 (填序号),期中所需G 的规格是 mL;
②操作步骤包括:计算、 、稀释、转移、 、定容、摇匀,此过程中玻璃棒的作用是 、 ;
③实验结束后,发现所配置的溶液浓度偏小,可能的原因是 (填序号)。
A.配置前容量瓶中有少量水
B.定容时仰视观察液面
C.摇匀后液面下降,又加入少量水
高一化学实验题中等难度题查看答案及解析
氯及其化合物在生产、生活中都有重要的应用:
(Ⅰ)现实验室要配置一定物质的量浓度的稀盐酸。
(1)如图是某市售盐酸试剂瓶标签上的部分数据。则该盐酸的物质的量浓度是___ mol·L-1。
(2)某同学用该浓盐酸配制100mL 1mol·L-1的稀盐酸。请回答下列问题:
①通过计算可知,需要用量筒量取浓盐酸 ____ mL。
②使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有_______。
③若配制过程遇下列情况,溶液的物质的量浓度将会:(填“偏高”“偏低”“无影响”)
A.量取的浓盐酸置于烧杯中较长时间后配制______。
B.转移溶液前,洗净的容量瓶内壁附有水珠而未干燥处理___。
C.定容时俯视容量瓶的刻度线_____。
(Ⅱ)实验室使用浓盐酸、二氧化锰共热制氯气,并用氯气和氢氧化钙反应制取少量漂白粉(该反应放热)。已知:MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O;氯气和氢氧化钙在温度较高时会生成副产物氯酸钙。甲、乙、丙三位同学分别设计了三个实验装置如下图所示:
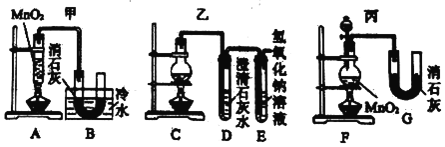
(1)哪位同学的装置能够有效地防止副反应的发生?_____。
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成。从上述甲、乙、丙三套装置中选出合理的部分(按气流从左至右的流向)组装一套较完善的实验装置(填所选部分的字母)_____。
(3)利用(2)中实验装置进行实验,实验中若用12 mol·L-1的浓盐酸200 mL与足量二氧化锰反应,最终生成的次氯酸钙的物质的量总小于0.3 mol,其可能的主要原因是_____(假定各步反应均无反应损耗且无副反应发生)。
(Ⅲ)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气一氯水体系,该体系中Cl2、HClO和ClO-的物质的量分数(a)随pH变化的关系如图所示。
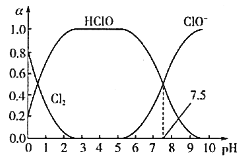
由图分析,欲使氯水的杀菌效果最好,应控制的pH范围是__,当pH=7.5时,氯水中含氯元素的微粒有___。
高一化学综合题中等难度题查看答案及解析

高一化学选择题中等难度题查看答案及解析