过氧化铬的化学式为 CrO5,从其结构发现含有 2 个过氧键,结构如图, 下列说法不正确的是
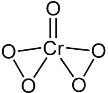
A.CrO5可能具有强氧化性
B.CrO5 溶于水可能放出氧气
C.CrO5 稳定性较低,易分解
D.CrO5 中 Cr 的化合价为+10
高三化学单选题中等难度题
过氧化铬的化学式为 CrO5,从其结构发现含有 2 个过氧键,结构如图, 下列说法不正确的是

A.CrO5可能具有强氧化性
B.CrO5 溶于水可能放出氧气
C.CrO5 稳定性较低,易分解
D.CrO5 中 Cr 的化合价为+10
高三化学单选题中等难度题
过氧化铬的化学式为 CrO5,从其结构发现含有 2 个过氧键,结构如图, 下列说法不正确的是

A.CrO5可能具有强氧化性
B.CrO5 溶于水可能放出氧气
C.CrO5 稳定性较低,易分解
D.CrO5 中 Cr 的化合价为+10
高三化学单选题中等难度题查看答案及解析
已知过氧化铬(CrO5)的结构式如下图所示,过氧化铬不稳定,溶于水生成过氧铬酸;溶于酸生成铬(III)盐(绿色)并放出氧气,反应方程式为:4CrO5+12H+=4Cr3++7O2+6H2O)。下列有关说法正确的是( )
A. CrO5中Cr元素的化合价为+10
B. 过氧化铬中含有极性共价键、非极性共价键和离子键
C. 过氧化铬具有较强的氧化性
D. 上述反应每转移0.2mol电子就能生成2.24LO2
高三化学单选题中等难度题查看答案及解析
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
高三化学填空题中等难度题查看答案及解析
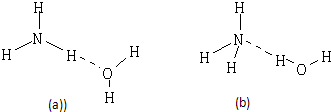
在2020年抗击新型冠状病毒肺炎的战役中,化学品发挥了重要作用,下列说法正确的是
A.银离子是重金属离子,被人体吸收后有害,因此不能用于杀菌
B.过氧乙酸(CH3COOOH)含有过氧键,具有较强的氧化性,因此具有消毒杀菌作用
C.配制84消毒液时,为了提升消毒效果,可以用热水配制
D.酒精是良好的消毒杀菌剂,而且浓度越高消毒效果越好
高三化学单选题简单题查看答案及解析
正确掌握化学用语和化学基本概念是学好化学的基础。下列各项中表达正确的是
A.NaCl的电子式:
B.H2O分子的分子结构模型示意图:(三个原子在同一直线上)
C.CrO5的结构式为 ,该氧化物中Cr为+6价
D.次氯酸的结构式:H-Cl-O
高三化学选择题简单题查看答案及解析
正确掌握化学用语和化学基本概念是学好化学的基础。下列各项中表达正确的是
A.NaCl的电子式:
B.H2O分子的分子结构模型示意图:(三个原子在同一直线上)
C.CrO5的结构式为,该氧化物中Cr为+6价
D.次氯酸的结构式:H-Cl-O
高三化学选择题简单题查看答案及解析
化学与生产、生活、社会密切相关.下列说法中正确的是( )
A.合金材料中可能含有非金属元素
B.钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈
C.二氧化硫和氯水均具有漂白性,可将两者混合使用增强漂白效果
D.氮化硅陶瓷、光导纤维、石英玻璃都属于新型无机非金属材料
高三化学选择题简单题查看答案及解析
(1)青蒿素结构如图,有关叙述正确的是_____(选填序号)。
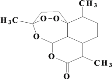
a.化学式为C15H21O5 b.不能与NaOH溶液反应
c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素,其中第2步为还原反应:
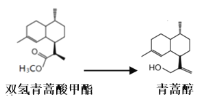
常温下即可反应且略放热,还原剂为LiAlH4。相关物质的性质:
| 物质 | 性质 |
| 双氢青蒿酸甲酯(C16H28O2) | 固体,难溶于水,易溶于有机溶剂。 |
| 青蒿醇(C15H28O) | 固体,难溶于水,易溶于有机溶剂。 |
| 乙醚 | 无色液体,微溶于水;密度0.71g/cm3;沸点34.6℃。 |
| 氢化铝锂 | 固体,溶于乙醚。 与水反应:LiAlH4 + 4H2O →Al(OH)3↓+ LiOH +4H2↑ 可将一分子酯还原成二分子醇,自身生成醇铝、醇锂。 (醇铝、醇锂可与盐酸反应,生成铝盐、锂盐和相应的醇)。 |
某学习小组在实验室用双氢青蒿酸甲酯制取青蒿醇。
(2)反应中使用过量的氢化铝锂,理由是_____________________________________________。为使反应在溶液状态下进行,可用乙醚为溶剂,不用水的理由是____________________。
(3)请设计实验室制备装置(画出草图):____________
(4)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂。从反应混合物中提取青蒿醇的方法是:
①加_______后分液;
②从乙醚层提取青蒿醇。有多种方法,以下是二种方案:
方案一:蒸发结晶。 方案二:蒸馏析出晶体。
a.这2个方案在析出晶体后都应有残留液,原因是___________________________________。
b.请对这2个方案进行比较_______________________________________________________。
高三化学综合题中等难度题查看答案及解析
实验室模拟工业处理含铬废水,操作及现象如图1,反应过程中铬元素的化合价变化如图2。下列说法正确的是( )

已知:深蓝色溶液中生成了CrO5。
A.实验开始至5s,铬元素被氧化
B.实验开始至30s,溶液中生成Cr3+的总反应离子方程式为:Cr2O+3H2O2+8H+=2Cr3++7H2O+3O2↑
C.30s至80s的过程,一定是氧气氧化了Cr3+
D.80s时,溶液中又生成了Cr2O,颜色相比于开始时浅,是水稀释所致
高三化学单选题困难题查看答案及解析
用结构和原理阐释化学反应的类型、限度、速率和历程是重要的化学学科思维。回答下列问题:
(1)用过氧化氢检验Cr(Ⅵ)的反应是Cr2O72-+4H2O2+2H+=2CrO5+5H2O。CrO5结构式为,该反应是否为氧化还原反应?___(填“是”或“否”)。
(2)已知:
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
H2(g)+O2(g)=H2O2(l) △H=-187.8kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) △H=___kJ·mol-1。
(3)一定条件下,H2O2分解时的c(H2O2)随t变化如图所示。已知该反应的瞬时速率可表示为v(H2O2)=k·cn(H2O2),k为速率常数。
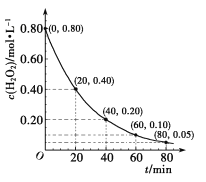
①0-20min内,v(H2O2)=___。
②据图分析,n=___。
③其它条件相同,使用活性更高的催化剂,下列说法正确的是___(填标号)。
A.v(H2O2)增大 B.k增大 C.△H减小 D.Ea(活化能)不变
(4)气体分压pi=p总×xi(物质的量分数)。恒温50℃、恒压101kPa,将足量的CuSO4·5H2O、NaHCO3置于一个密闭容器中,再充入已除去CO2的干燥空气。假设只发生以下反应,达平衡时两者分解的物质的量比为2:1。
CuSO4·5H2O(s)⇌CuSO4·3H2O(s)+2H2O(g) Kp1=36(kPa)2
2NaHCO3(s)⇌Na2CO3(s)+H2O(g)+CO2(g) Kp2
①平衡时=___,Kp2=___。
②平衡后,用总压为101kPa的潮湿空气[其中p(H2O)=8kPa、p(CO2)=0.4kPa]替换容器中的气体,50℃下达到新平衡。容器内CuSO4·5H2O的质量将___(填“增加”“减少”或“不变”,下同),NaHCO3质量将___。
高三化学综合题中等难度题查看答案及解析