向未知浓度的
、
混合溶液逐滴滴加
溶液,混合溶液的电导率(导电能力)如图所示,下列叙述错误的是( )
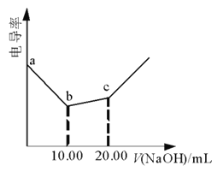
A. 两点水的电离程度:
B.原溶液中
C.是
恰好被
溶液中和的过程
D.点:
高三化学单选题中等难度题
向未知浓度的
、
混合溶液逐滴滴加
溶液,混合溶液的电导率(导电能力)如图所示,下列叙述错误的是( )

A. 两点水的电离程度:
B.原溶液中
C.是
恰好被
溶液中和的过程
D.点:
高三化学单选题中等难度题
向未知浓度的
、
混合溶液逐滴滴加
溶液,混合溶液的电导率(导电能力)如图所示,下列叙述错误的是( )

A. 两点水的电离程度:
B.原溶液中
C.是
恰好被
溶液中和的过程
D.点:
高三化学单选题中等难度题查看答案及解析
已知电解质溶液电导率越大导电能力越强。常温下用溶液分别滴定
浓度均为
的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法错误的是( )。
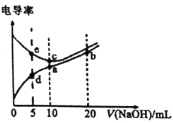
A.c点的混合液pH=7
B.e、d两点溶液混合后的溶液中:
C.b点溶液中:
D.a、b、c三点溶液中水的电离程度:
高三化学单选题困难题查看答案及解析
利用手持技术可测定酸碱滴定过程中溶液的电导率导电能力
和pH的变化,
时向
浓度均为
的盐酸和醋酸的混合溶液中逐滴加入
氨水,滴定过程中电导率和pH变化曲线如图所示,
已知
和
的电离平衡常数均为
。下列说法正确的是
A.a点溶液中,
B.b点溶液中,主要溶质为和HCl
C.c点对应的氨水
D.d点溶液中,
高三化学单选题中等难度题查看答案及解析
电导率可用于衡量电解质溶液导电能力的大小。室温下,用0.1000mol/L氨水滴定10mL浓度均为0.100 mol/L的盐酸和醋酸的混合液,电导率曲线如图所示。下列说法错误的是
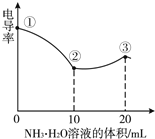
A.①点溶液中c(H+)为0.200 mol/L
B.②点溶液中c(Cl-)>c(NH4+)>c(Ac-)
C.①点溶液中n(所有离子)之和>③点溶液n(所有离子)之和
D.③点后会出现pH=7的点,此点溶液中c(NH4+)=c(Ac-)+c(Cl-)
高三化学多选题中等难度题查看答案及解析
电导率可用于衡量电解质溶液导电能力大小,且电导率越大溶液的导电能力越强。室温下,用的
滴定
浓度均为
和
的混合液,电导率曲线如图所示。下列说法正确的是

A.溶液中
为
B.溶液温度高低为①>②>③
C.点后因离子数目减少使电导率略降低
D.点时溶液中有
高三化学单选题困难题查看答案及解析
常温下用盐酸分别滴定
浓度均为
的NaOH溶液和二甲胺
溶液
在水中电离方式与氨相似
,利电用传感器测得滴定过程中溶液的电导率如图所示。已知电解质溶液电导率越大导电能力越强。
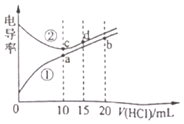
①a、b、c、d四点的水溶液中,由水电离出氢离子浓度大于1.0×10-7 的是______,原因为______。
②化学反应往往伴有热效应,若为绝热体系,a的温度______填“
”,“
”或“
”
点的温度。
高三化学综合题中等难度题查看答案及解析
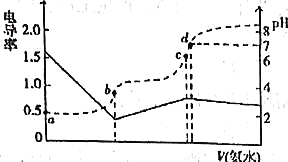
常温下,向10mL0.1mol·的HA溶液中逐滴滴入0.1mol·
的ROH溶液,所得溶液pH及导电能力的变化如图,下列判断正确的是
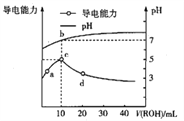
A. ROH在溶液中的电离方程式为
B. c点由电离出的
浓度最小
C. b点存在:
D. 若升高温度,a、d两点pH增大
高三化学单选题困难题查看答案及解析
常温下,向10mL0.1mol·的HA溶液中逐滴滴入0.1mol·
的ROH溶液,所得溶液pH及导电能力的变化如图,下列判断正确的是

A. ROH在溶液中的电离方程式为
B. c点由电离出的
浓度最小
C. b点存在:
D. 若升高温度,a、d两点pH增大
高三化学单选题困难题查看答案及解析
电导率可用于衡量电解质溶液导电能力大小。室温下,用0.100滴定 10.00 mL 浓度均为 0.100 mol/L HCl和CH3COOH的混合溶液,所得曲线如右图所示。下列说法正确的是()
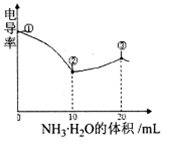
A. ①点溶液中C(H+)为
B. 溶液温度高低为①〉③〉②
C. ③点溶液中有
D. ③点后因离子数目减少使溶液电导率略降低
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析