-
运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)反应ⅠFe(s)+CO2(g)  FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+CO(g) ΔH1,平衡常数为K1;
反应ⅡFe(s)+H2O(g)  FeO(s)+H2(g) ΔH2,平衡常数为K2;
FeO(s)+H2(g) ΔH2,平衡常数为K2;
在不同温度K1、K2值如下表:
| 700 ℃ | 900 ℃ |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
①由表中判断,反应Ⅰ为中ΔH1______ (填“<”或“=”或“>”) 0。
②反应CO2(g)+H2(g)  CO(g)+H2O(g) ΔH平衡常数为K,则K=________(用K1和K2表示)。
CO(g)+H2O(g) ΔH平衡常数为K,则K=________(用K1和K2表示)。
③能判断CO2(g)+H2(g)  CO(g)+H2O(g)达到化学平衡状态的依据是________(填字母)。
CO(g)+H2O(g)达到化学平衡状态的依据是________(填字母)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO)=c(CO2)
E.容器内的气体密度不变 F.混合气体的平均摩尔质量不变。
(2)在不同温度和压强下合成氨,起始时投入氮气和氢气的物质的量分别为1mol、3mol。平衡时混合物中氨的体积分数与温度的关系如图。
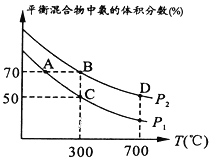
①P1_______P2 (填“>”“=” “<”或“不确定”,)。
②C点H2的转化率为________。
-
运用化学反应原理研究碳、氮、硫的化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车尾气脱硝脱碳主要原理为2NO(g) + 2CO(g) N2(g) + 2CO2(g) ΔH <0。
N2(g) + 2CO2(g) ΔH <0。
①该反应在______(填“低温”或“高温”)下可自发反应。
②一定条件下的密闭容器中,充入10 mol CO和8 mol NO, 发生上述反应,如图为平衡时NO的体积分数与温度、压强的关系。
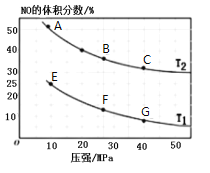
Ⅰ.该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有______(填字母序号)。
a.缩小容器的体积 b.改用高效催化剂
c.升高温度 d.增加CO的浓度
Ⅱ.压强为10 MPa、温度为T1下,若反应进行到30 min达到平衡状态,容器的体积为4L,该温度下平衡常数Kp=______(压强以MPa为单位进行计算,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;保留两位有效数字)。
③氨气易溶于水可电离出 NH4+和 OH-、易液化,液氨也与水一样发生微弱的双聚电离,但比水弱,能溶解一些金属等性质。下列说法中不正确的是_______
a.NH3 可看作比水弱的电解质
b.NH3 的双聚电离可表示为:2NH3 NH4++NH2-
NH4++NH2-
c.NH3 易溶于水是由于与水形成氢键
d.NH3 可与Na 反应: 2NH3+2Na=2NaNH2+H2↑
(2)冶金工业、硝酸工业的废气废液中含氮化合物污染严重,必须处理达标后才能排放。用活性炭处理工厂尾气中的氮氧化物。
①已知:Ⅰ. 4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1=a kJ·mol-1
Ⅱ. 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=b kJ·mol-1
Ⅲ. C(s)+O2(g)=CO2(g) ΔH3=c kJ·mol-1
则反应C(s)+2NO(g)  N2(g)+CO2(g)的ΔH =_____ kJ·mol-1(用a、 b 、c表示)。
N2(g)+CO2(g)的ΔH =_____ kJ·mol-1(用a、 b 、c表示)。
②在容积不变的密闭容器中,一定量的NO与足量的C发生反应:C(s)+2NO(g)  N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是______。
N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图所示,下列说法正确的是______。

a.其他条件不变,容器内压强不再改变时,反应达到平衡状态
b.温度为T2时,若反应体系处于状态D,则此时v正>v逆
c.该反应的Q>0,所以T1、T2、T3对应的平衡常数:K1<K2<K3
d.若状态B、C、D体系的压强分别为p(B)、p(C)、p(D),则p(D)=p(C)>p(B)
③已知某温度时,反应C(s)+2NO(g)  N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。
N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图中画出反应过程中c(NO)随时间t的变化曲线。
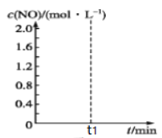 ____________
____________
④工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:__________________。
-
研究碳氧化合物、氮氧化合物、硫氧化合物等大气污染物的处理对缓解环境污染、能源危机具有重要意义。
(1)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g)△H<0。其他条件相同,在甲、乙两种催化剂作用下,相同时间时NO转化率与温度的关系如图。
4N2(g)+6H2O(g)△H<0。其他条件相同,在甲、乙两种催化剂作用下,相同时间时NO转化率与温度的关系如图。
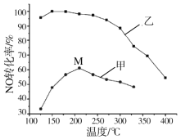
①工业上选择催化剂__________(填“甲”或“乙”)。
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是__________。(写一条即可)。
(2)某研究小组对反应NO2+SO2 SO3+NO△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。
SO3+NO△H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。
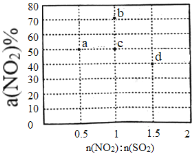
①如果将图中b点的平衡状态改变为c点的平衡状态,应采取的措施是________________。
②图中a、d两点对应的实验温度分别为T1和T2,则T1_______T2(填“>”、“=”或“<”)。
(3)在酸性电解质溶液中,以惰性材料作电极,将CO2转化为丙烯的原理如图所示。
①太阳能电池的正极为_____(填“a”或“b”)。
②生成丙烯的电极反应式是_____________________________。
③当生成标准状况下2.24L丙烯时,右侧溶液中质量减少____g。

-
运用化学反应原理对研究部分单质及其化合物的反应有重要意义。
(1)氨是氮循环过程中的重要物质,是氮肥工业的重要原料。氨的合成是目前普遍使用的人工固氮方法:N2(g)+3H2(g) 2NH3(g)。请回答:
2NH3(g)。请回答:
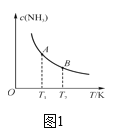
①已知H—H键键能为436kJ·mol-1,N≡N键键能为945 kJ·mol-1,N—H键键能为391 kJ·mol-1。由键能计算消耗1 mol N2时的ΔH=_____。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡____(填“向左”、“向右”或“不”)移动。
②如图中,当温度由T1变化到T2时,KA___(填“>”、“<”或“=”)KB。
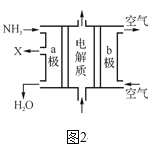
③废氨水可以转化成氨,氨再设计成碱性燃料电池。如图是该燃料电池示意图,产生的X气体可直接排放到大气中。a电极作____(填“正”、“负”、“阴”或“阳”)极,其电极反应式为____。
(2)某温度下在容积固定的密闭容器中,下列反应达到平衡:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
| 起始n(CO)∶n(H2O) | CO转化率 | H2O转化率 |
| 1∶1 | 0.5 | 0.5 |
| 1∶2 | 0.67 | 0.33 |
| 1∶3 | 0.75 | 0.25 |
①该反应的平衡常数为_____。该温度下,向容器中充入1 mol CO、3 mol H2O、2 mol CO2、1.5 mol H2,则起始时该反应速率v(正)______(填“>”、“<”或“=”)v(逆)。
②结合表中数据,判断下列说法正确的是_______(填字母)。
A.增加H2O(g)的量,CO的转化率升高而H2O(g)的转化率降低
B.若CO与H2O(g)的转化率相同,二者的初始投入量一定相同
C.CO和H2O(g)初始物质的量之比等于二者转化率之比
D.当CO与H2O(g)物质的量之比为1∶4时,CO的转化率为0.85
③该温度下,向容器中充入2 mol CO、2 mol H2O,达平衡时放出a kJ热量,则该反应的ΔH=_____。
-
(1)已知1g碳粉在氧气中完全燃烧放出的热量是32.8 kJ,试写出表示碳燃烧热的热化学方程式
(2)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
①合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“正向”、“逆向”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“正向”、“逆向”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”)。
②已知:O2(g)  O2+(g)+e- △H1=+1175.7 kJ·mol—1
O2+(g)+e- △H1=+1175.7 kJ·mol—1
PtF6(g)+e- PtF6-(g) △H2=-771.1 kJ·mol—1
PtF6-(g) △H2=-771.1 kJ·mol—1
O2PtF6(s) O2+(g)+PtF6-(g) △H3=+482.2 kJ·mol—1
O2+(g)+PtF6-(g) △H3=+482.2 kJ·mol—1
则反应O2(g)+PtF6(g)  O2PtF6 (s)的 △H=_____________
O2PtF6 (s)的 △H=_____________
-
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应N2 (g)+3H2(g)=2NH3(g),若在恒温、恒压条件下向平恒体系中通入氩气,则平衡______移动(填“向左”“向右”或“不”);使用催化剂______反应的△H(填“增大”“减小”或“不改变”).
(2)已知:O2 (g)=O2+(g)+e-△H1=1175.7kJ•mol-1
PtF6(g)+e- =PtF6-(g)△H2=-771.1kJ•mol-1
=PtF6-(g)△H2=-771.1kJ•mol-1
O2+PtF6-(S)=O2+ (g)+PtF6-(g)△H3=482.2kJ•mol-1
则反应O2(g)+PtF6(g)=O2+PtF6-(S) 的△H=______ kJ•mol-1.
(3)在25℃下,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式为______.已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20.
(4)在25℃下,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-).则溶液显______性(填“酸”“碱”或“中”);用含a的代数式表示NH3•H2O的电离常数Kb=______.
-
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应,在2L密闭容器中通入2mol的N2和6mol的H2,5min时反应达到平衡,此时容器内的压强变为原来的3/4,0-5min该反应的化学反应速率为V(H2)=______,N2的转化率=______,化学平衡常数K=______.
(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图1:
则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为______.
(3)用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是______(填字母)
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c)
C.平衡常数:K(b)=K(d)
D.正反应速率:v(b)>v(d)
E.平均摩尔质量:M(a)=M(c)
(4)在25℃下,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl¯),则溶液显(______)性(填“酸”“碱”或“中”);用含a的代数式表示NH3•H2O的电离常数Kb=______.
-
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
 (1)合成氨反应反应N2(g)+3H2(g)
(1)合成氨反应反应N2(g)+3H2(g)  2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);,使用催化剂________反应的ΔH(填“增大”“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);,使用催化剂________反应的ΔH(填“增大”“减小”或“不改变”)。
(2)O2 (g)= O+2(g)+e-  H1=+ 1175.7 kJ·mol-1
H1=+ 1175.7 kJ·mol-1
 PtF6(g)+ e-1
PtF6(g)+ e-1  PtF6-(g)
PtF6-(g)  H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6-  H3=+482.2 kJ·mol-1
H3=+482.2 kJ·mol-1
 则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)的
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)的 H=_____________ kJ·mol-1。
H=_____________ kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
 (4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
-
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);使用催化剂反应的△H________(填“增大”“减小”或“不改变”).
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);使用催化剂反应的△H________(填“增大”“减小”或“不改变”).
(2)O2 (g)=O+2(g)+e-△H1=+1175.7kJ•mol-1
PtF6(g)+e-1=PtF6-(g)△H2=-771.1kJ•mol-1
O2+PtF6-(s)=O2+(g)+PtF6-(g)△H3=+482.2kJ•mol-1
则反应O2(g)+PtF6(g)=O2+PtF6-(s)的△H=________kJ•mol-1.
(3)在25℃下,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________,已知25℃时Ksp[Mg(OH)2] = 1.8 × 10-11,KsP[Cu(OH)2] = 2.2 × 10-20
(4)在25℃时,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”),用含a的代数式表示NH3•H2O的电离常数kb=________。
-
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H________(填“增大”、“减小”或“不改变”)。
2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H________(填“增大”、“减小”或“不改变”)。
(2)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出。
首先生成沉淀的离子方程式为__________________
氨水过量后,生成的沉淀会部分溶解,写出溶解沉淀的离子方程式__________________________.
( 已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10-20 )
(3) 在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中
c(NH4+) = c(Cl-)。则溶液显_____ 性(填“酸”、“碱”或“中”),请用含a的代数式表示NH3·H2O的电离常数Kb=________。
(4) 在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则v(o2)=mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,再次达到平衡后, n(SO3)的取值范围为________________。
FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+H2(g) ΔH2,平衡常数为K2;
CO(g)+H2O(g) ΔH平衡常数为K,则K=________(用K1和K2表示)。
CO(g)+H2O(g)达到化学平衡状态的依据是________(填字母)。



 ____________
____________




