-
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
【实验1】铜与浓硫酸反应,实验装置如图所示。

实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置 A 中发生反应的化学方程式为__________。实验中发现在 A 里产生了白色固体,其可能为________。C中NaOH溶液的作用为______
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是______。
(3)停止加热后,在拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是__________________。
【实验2】实验中发现试管A内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图所示的实验
(4)②中检验滤渣是否洗涤干净的实验操作是___________。
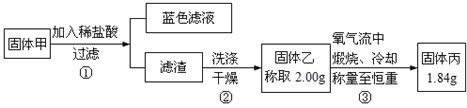
(5)③中在煅烧过程中一定发生的反应的化学方程式为_____________________。
(6)下列对于固体甲的成分的判断中,正确的是(填字母选项)____________。
A.固体甲中,CuS和Cu2S不能同时存在
B.固体甲中,CuO和Cu2O至少有一种
C.固体甲中若没有Cu2O,则一定有Cu2S
D.固体甲中若存在Cu2O,也可能有Cu2S
-
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
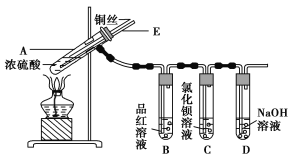
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为____________________________________________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_______________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | ________ | ________ |
写出其SO2表现还原性的离子反应方程式:______________________________________。
(4) 装置D的作用__________________________________________________________ 。
(5)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是_________________________________________________________________。
-
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
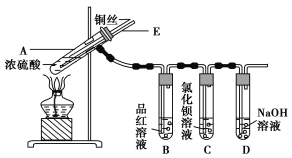
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为____________________________________________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_______________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | ________ | ________ |
写出其SO2表现还原性的离子反应方程式:______________________________________。
(4) 装置D的作用__________________________________________________________ 。
(5)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是_________________________________________________________________。
-
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。

实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液褪色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为____________________________________________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_______________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | ________ | ________ |
写出其SO2表现还原性的离子反应方程式:______________________________________。
(4) 装置D的作用__________________________________________________________ 。
(5)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是_________________________________________________________________。
-
为了探究铜与浓硫酸的反应,某实验小组同学进行了如下实验,实验装置如图所示。
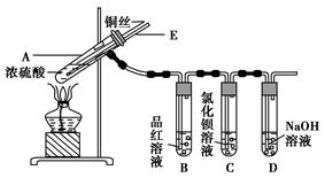
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为 。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是 。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
写出其中涉及的氧化还原反应的离子反应方程式: 。
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是 。
(5)实验完毕后,装置中残留的气体有毒,不能打开导管上的胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 。
-
某实验小组同学为了探究SO2的性质,进行了如下实验(实验前,装置内空气已排尽):

已知:硫酸的沸点是338℃,酒精灯可加热至400℃以上。
主要实验步骤:
①加热试管A直到B、D中均出现大量白色沉淀,熄灭酒精灯;
②将Cu丝上提离开液面;
③从导管F口向装置中通入空气一段时间。
(1)试管A中发生的主要反应的化学方程式为 。
(2)试管B中出现白色沉淀的原因是 。
(3)试管C中溶液褪色,说明SO2具有 (填“漂白性”或“氧化性”或“还原性”),请将该反应的离子方程式补充完整:

(4)试管D中发生反应的离子方程式为 。
(5)下列叙述正确的是 。
a.上下移动铜丝可控制生成SO2的量
b.为确认有CuSO4生成,可向试管A中加水,观察颜色
c.步骤③可使装置中残留气体完全被吸收,避免污染空气
d.熄灭酒精灯后, B中的液体不会倒吸,因为空气可经导管F进入试管A,使压强平衡
-
(题文)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验。实验装置如下图所示,A中盛有浓硫酸,插入一段下端已绕成螺旋状的铜丝,D为玻璃导管。
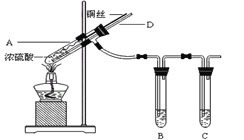
(1)装置A中发生反应的化学方程式为:_________________,该反应中浓硫酸的主要作用有_____________________。
(2)当B中盛有___________时,证明生成的气体产物具氧化性; 当B中盛有___________时,B中溶液颜色褪去,证明生成气体产物具有还原性。
(3)C为尾气处理装置,C中盛放的试剂为________________。
(4)有人建议在A之间B增加一个防倒吸的安全瓶,经该实验小组同学实验后发现,即使不加安全瓶熄灭酒精灯停止反应后,B中的液体也没有发生倒吸,请给出一个合理的解释_______。
(5)实验中,该小组同学取6.4g铜丝和12mL 18mol·L-1H2SO4溶液放在试管中共热充分反应直到反应停止,最后发现烧瓶中还有铜丝剩余;该小组同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的试管中确有剩余的H2SO4的是________ 。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.小苏打粉末
-
(题文)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验。实验装置如下图所示,A中盛有浓硫酸,插入一段下端已绕成螺旋状的铜丝,D为玻璃导管。
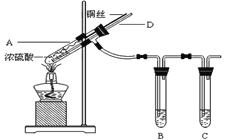
(1)装置A中发生反应的化学方程式为:_________________,该反应中浓硫酸的主要作用有_____________________。
(2)当B中盛有___________时,证明生成的气体产物具氧化性; 当B中盛有___________时,B中溶液颜色褪去,证明生成气体产物具有还原性。
(3)C为尾气处理装置,C中盛放的试剂为________________。
(4)有人建议在A之间B增加一个防倒吸的安全瓶,经该实验小组同学实验后发现,即使不加安全瓶熄灭酒精灯停止反应后,B中的液体也没有发生倒吸,请给出一个合理的解释_______。
(5)实验中,该小组同学取6.4g铜丝和12mL 18mol·L-1H2SO4溶液放在试管中共热充分反应直到反应停止,最后发现烧瓶中还有铜丝剩余;该小组同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的试管中确有剩余的H2SO4的是________ 。
a.BaCl2溶液 b.Ba(NO3)2溶液 c.银粉 d.小苏打粉末
-
为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
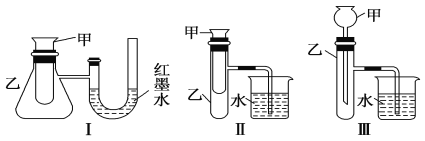
(1)上述装置中,不能证明“锌和稀硫酸反应是吸热反应还是放热反应”的是 _________(填序号)
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡晶体与氯化铵固体搅拌反应,U形管中可观察到的现象是___________________________________________________________________________________________
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若观察到烧杯里的玻璃管内形成一段水柱,则说明M溶于水________________ (填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”或“可能是吸热反应”),理由____________。
②若观察到烧杯里产生气泡,则M可能是__________________(填一种物质的化学式)
-
(14分)某实验小组同学用如下实验装置探究铜与浓硫酸的反应。
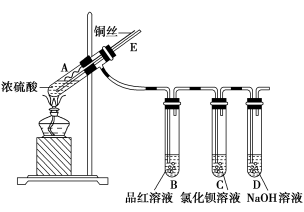
实验步骤:
①先连接好装置,检查气密性,再加入试剂;
②加热A试管,B中品红溶液褪色,熄灭酒精灯;
③将铜丝向上抽动离开液面。
(1)A试管中发生反应的化学方程式为 。
(2)能够证明铜与浓硫酸反应生成气体的现象是 。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其分成两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应的位置。
写出其中SO2显示还原性的反应的离子方程式 。
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,B中的液体不会倒吸入A中,其原因是____________ ____________。
(5)实验完毕后,装置中残留气体有毒,不能打开胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 。











