-
知识的梳理和感悟是有效学习的方法之一。山大附中高二化学兴趣小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(所有电极均为石墨)。电解所用的氯化钠溶液需精制,除去有影响的Ca2+、Mg2+、NH4+、SO42﹣及泥沙,其精制流程如下:
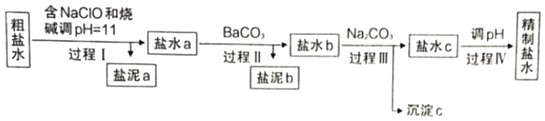
已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如表。
| Ca(OH)2 | Mg(OH)2 |
| pH | ≥11.5 | ≥9.2 |
②Ksp(BaSO4)=1.1×10﹣10,Ksp(BaCO3)=2.6×10﹣9,Ksp(CaCO3)=5.0×10﹣9
(1)盐泥a除泥沙外,还含有___________(填化学式)。
(2)过程I中,NaClO的作用是将NH4+转化为N2,反应的离子方程式为________________。
(3)过程Ⅲ中,沉淀c主要成分的化学式为_____。
(4)过程Ⅳ调pH目的是除去___________(填离子符号)
(5)利用图1装置电解精制氯化钠一段时间后,气球b中的气体是_____(填化学式)
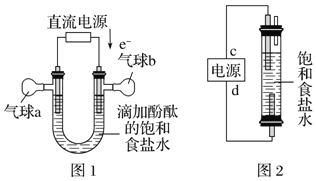
(6)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分NaClO,则c为电源的_____极;该发生器中反应的总离子方程式为_______________。
(7)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。如图是目前已开发出用电解法制取ClO2的新工艺。
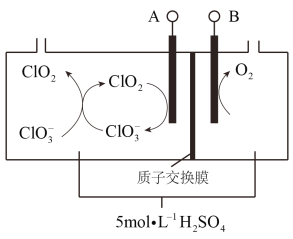
①阴极发生的反应有:_______________、__________________________。
②当阳极产生标准状况下112 mL气体时,通过阳离子交换膜离子的物质的量为_____。
-
知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
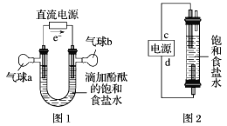
(1)图1中,电解一段时间后,气球b中的气体是__________(填化学式),U形管________(填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的________极;该发生器中反应的总离子方程式为_______________________________。
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出用电解法制取ClO2的新工艺。
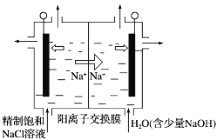
①阳极产生ClO2的电极反应式:__________________________________________________。
②当阴极产生标准状况下112 mL气体时,通过阳离子交换膜的离子物质的量为________。
-
知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
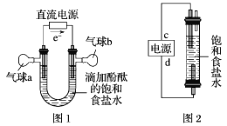
(1)图1中,电解一段时间后,气球b中的气体是__________(填化学式),U形管________(填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则c为电源的________极;该发生器中反应的总离子方程式为_______________________________。
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。下图是目前已开发出用电解法制取ClO2的新工艺。
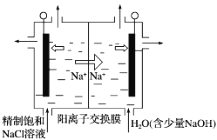
①阳极产生ClO2的电极反应式:__________________________________________________。
②当阴极产生标准状况下112 mL气体时,通过阳离子交换膜的离子物质的量为________。
-
某化学兴趣小组进行有关电解食盐水的探究实验,电解装置如图所示。

实验一:电解饱和食盐水。
(1)配制饱和食盐水所需的玻璃仪器有:烧杯、量筒、 。
(2)电解饱和食盐水的化学方程式为 。
实验二:电解不饱和食盐水及产物分析。
相同条件下,电解1mol·L-1 NaCl溶液并收集两极产生的气体。在X处收集到V1mL气体,同时,在Y处收集到V2mL气体,停止电解。结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
ⅰ.有部分Cl2溶于NaCl溶液中;ⅱ.有O2生成。
(3)设计实验证明有部分Cl2溶于NaCl溶液中。实验方案为:取少量 电极附近溶液。
(4)证明有O2生成并测定O2的体积。按如右图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3mL气体(设V1、V2、V3均在相同条件下测得)。

①装置A的作用是 。
②本实验中,观察到________________的现象,说明石墨电极上有O2生成。
③实验中是否需要预先除尽装置中的空气? (填“是”或“否”)。
(5)实验二中,在石墨电极上产生的Cl2的总体积为 mL(用代数式表示)。
-
某化学兴趣小组进行有关电解食盐水的探究实验,电解装置如图所示。


实验一:电解饱和食盐水。
(1)配制饱和食盐水所需的玻璃仪器有:烧杯、量筒、 。
(2)电解饱和食盐水的化学方程式为 。
实验二:电解不饱和食盐水及产物分析。
相同条件下,电解1mol·L-1 NaCl溶液并收集两极产生的气体。在X处收集到V1mL气体,同时,在Y处收集到V2mL气体,停止电解。结果发现V2<V1,且与电解饱和食盐水相比,Y处收集到的气体颜色明显较浅。经讨论分析,导致上述现象的原因有:
ⅰ.有部分Cl2溶于NaCl溶液中;ⅱ.有O2生成。
(3)设计实验证明有部分Cl2溶于NaCl溶液中。实验方案为:取少量 电极附近溶液, 。
(4)证明有O2生成并测定O2的体积。按如右图所示装置进行实验,通过注射器缓缓地将在Y处收集到V2mL气体全部推入装置A(盛有足量试剂NaOH溶液)中,最终,量气管中收集到V3mL气体(设V1、V2、V3均在相同条件下测得)。
①装置A的作用是 。
②本实验中,观察到________________的现象,说明石墨电极上有O2生成。
③实验中是否需要预先除尽装置中的空气? (填“是”或“否”)。
(5)实验二中,在石墨电极上产生的Cl2的总体积为 mL(用代数式表示)。
-
化学实验小组在学习化学电源和氯碱工业相关知识后,在实验室 进行实验验证,他们设计组装了如下图所示装置,已知为石墨电极;为铁电极;为铝电极(已除去表面氧化膜); 为多孔石墨电极,烧杯中是足量饱和食盐水(滴有酚酞),连好导线后,电流计指针发生明显偏转。下列判断正确的是
为多孔石墨电极,烧杯中是足量饱和食盐水(滴有酚酞),连好导线后,电流计指针发生明显偏转。下列判断正确的是
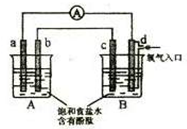
A.为负极, 为阳极
为阳极
B.一段时间后,和 电极附近溶液变红
电极附近溶液变红
C.电极电极反应式为:2Cl—2e-=Cl2↑
D.当电解一段时间,B中出现大量白色沉淀时,停止
实验,再将A中溶液倒入B中混合,充分振荡,
沉淀全部消失
-
电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:
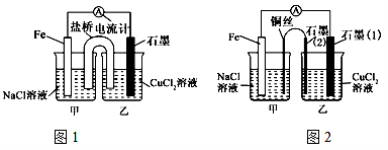
(1)如上图1为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的KNO3溶液和琼胶制成的胶冻,则NO3-移向_____________装置(填写“甲或乙”)。其他条件不变,若将CuCl2溶液换为NH4Cl溶液,发现生成无色无味的单质气体,则石墨上电极反应式______________________。
(2)如上图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲装置是____________(填“原电池或电解池”),乙装置中石墨(2)为 极,乙装置中与铁线相连的石墨(1)电极上发生的反应式为 。
(3)在图2乙装置中改为加入CuSO4溶液,一段时间后,若某一电极质量增重 1.28 g,则另一电极生成______________mL(标况下)气体。
-
电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:
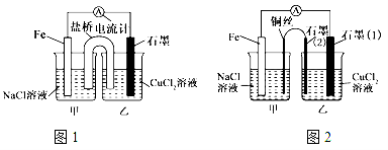
(1)如上图1为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的KNO3溶液和琼胶制成的胶冻,则NO3-移向_____________装置(填写“甲或乙”)。其他条件不变,若将CuCl2溶液换为NH4Cl溶液,发现生成无色无味的单质气体,则石墨上电极反应式______________________。
(2)如上图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲装置是____________(填“原电池或电解池”),乙装置中石墨(2)为 极,乙装置中与铁线相连的石墨(1)电极上发生的反应式为 。
(3)在图2乙装置中改为加入CuSO4溶液,一段时间后,若某一电极质量增重 1.28 g,则另一电极生成______________mL(标况下)气体。
-
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程式为________。
(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)

①理论上,电解后溶液中c(OH—)=________mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是________g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是________g。
b.还可能为________(用离子方程式表示)。
经测定,该实验中溶液实际减少的质量为4.23 g,则所产生的气体及其物质的量之比为________。
-
(12分)某化学研究性小组采用如下装置(夹持和加热仪器已略去)电解饱和食盐水一段时间,并通过实验测定产物的量来判断饱和食盐水的电解率。饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%
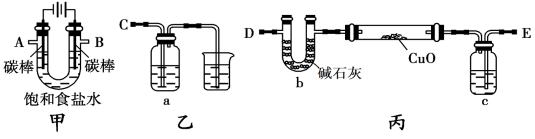
甲方案:利用甲、乙装置测定饱和食盐水的电解率
(1)若饱和食盐水中滴有酚酞,则电解过程中甲装置中的实验现象: 。
(2)若洗气瓶a中盛放的为足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率,则正确的连接顺序为 连________(填A、B、C、D、E等导管口),则洗气瓶a中发生反应的离子方程式为 。
乙方案:利用甲、丙装置测定饱和食盐水的电解率
(3)对于乙方案,有同学提出有两种方法都可测得饱和食盐水的电解率
Ⅰ.通过测定硬质玻璃管中氧化铜固体前后质量差来计算饱和食盐水的电解率
Ⅱ.通过测定丙装置中除硬质玻璃管外的某装置前后质量差来计算饱和食盐水的电解率
①一同学认为可以在乙方案方法Ⅱ中的装置中添加一干燥装置防止外界空气中的水蒸气的干扰,则该干燥装置应与 口连接
a.A b.B c.D d.E
②另一同学认为乙方案的方法Ⅰ、Ⅱ测得的实验结论都不正确,你是否同意?请说明理由 。
丙方案:只利用甲装置测定饱和食盐水的电解率。
(4)若电解150mL饱和食盐水一段时间,测得溶液的为pH为14,求饱和食盐水的电解率 (假设电解前后溶液体积不变,饱和食盐水密度约为1.33 g/mL,溶解度为33.0g)。
(5)若往该电解后所得溶液中通入二氧化碳气体2.24L(标准状况),则所得溶液中各离子浓度大小关系为: 。














