-
元素周期表中第VIIA族元素的单质及其化合物的用途广泛:
己知:H2CO3:Kal=4.3×l0-7 ,Ka2=5.6×l0-ll HC1O,Ka=2.98×l0-8
(1)室温下,0.l mol/L的次氯酸钠溶液和0.l mol/L的碳酸氢钠溶液,碱性较强的是___________;其原因是___________。
(2)己知新制氯水中存在三种分子和四种离子。在500mL l mol.L-l的碳酸钠溶液中,通入11.2L(标准状况)的Cl2,充分反应以后,溶液中离子浓度在前三位的大小顺序为__________;
(3)BrF3具有较强的氧化性,可以和许多还原剂反应。在一定条件下,BrF3和H2O反应生成O2和等物质的量的Br2和HBrO3,写出该反应的化学方程式_____________;
(4)向CuCl2溶液中滴加NaOH溶液,有蓝色沉淀生成,继续滴加一定量的NaHS溶液后,生成CuS黑色沉淀,用溶解平衡和电离平衡原理解释上述现象__________________;
(5)将1.12L(标准状况)CH3F在纯氧中完全燃烧,将产物通入足量的澄清石灰水中,溶液中有白色固体生成,白色沉淀是_____________、_________,再通入过量的CO2沉淀部分消失,继续滴加浓盐酸浊液变澄清,用离子方程式解释上述现象__________________。
高三化学综合题中等难度题查看答案及解析
-
下列说正确的是
【已知:HClO的Ka=3.0×l0-8;H2CO3的Ka1= 4.3×l0-7,Ka2=5.6×l0-11;Ksp(BaSO4)= 1.1 ×10-10;Ksp(BaCO3)= 5.1 ×10-9】
A.相同条件下,pH相同的NaClO和Na2CO3溶液,物质的量浓度前者小于后者
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7时:
c(Na+)>c(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+)=c(OH-)
C.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小
D.氯碱工业使用的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂时,粗盐水中可先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后滤去沉淀,所得滤液中仍含有一定量的SO42-
高三化学选择题中等难度题查看答案及解析
-
根据表提供的数据,下列判断正确的是
弱酸化学式
CH3COOH
HClO
H2CO3
电离平衡常数
1.8×10-6
3.0×10-8
Ka1=4.3×10-7
Ka2=5.6×l0-11
A. 等物质的量的Na2CO3和CH3COOH两种溶液混合,一定有:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(CH3COO-)
B. 常温下,已知酸H2A存在如下平衡:H2A
H++HA-;HA-
H++A2-(Ka1=5.9×10-2,Ka2=6.4×10-6),则NaHA溶液中水的电离程度一定大于纯水中水的电离程度
C. 相同浓度的CH3COONa和NaClO混合溶液中各离子浓度大小关系是:
C(Na+)> c(ClO-)> c(CH3COO-)> c(OH-)>c(H+)
D. 常温下,在0.1mol/LCH3COOH溶液中滴加0.1mol/LNaOH的溶液发生反应,当c(CH3COOH):c(CH3COO-)=5:9时,此时溶液pH=5
高三化学选择题中等难度题查看答案及解析
-
元素周期表中第VIIA族元素的单质及其化合物的用途广泛.完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有___种不同能量的电子.
(2)能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___(填序号).
a.IBr中溴为﹣1价 b.HBr、HI的酸性c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)海水提溴过程中,先向浓缩海水中通入_____,将其中的Br﹣氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收.已知纯碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_____mol,反应中氧化产物为_____.
(4)已知:AlF3的熔点为1040℃,AlCl3在178℃升华.从物质结构的角度解释两者熔点相差较大的原因:__________
(5)HClO有很好的杀菌消毒效果.为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_____________________。
高三化学综合题中等难度题查看答案及解析
-
元素周期表中第VIIA族元素的单质及其化合物的用途广泛.完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有___种不同能量的电子.
(2)能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___(填序号).
a.IBr中溴为﹣1价 b.HBr、HI的酸性c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)海水提溴过程中,先向浓缩海水中通入_____,将其中的Br﹣氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收.已知纯碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_____mol,反应中氧化产物为_____.
(4)已知:AlF3的熔点为1040℃,AlCl3在178℃升华.从物质结构的角度解释两者熔点相差较大的原因:__________
(5)HClO有很好的杀菌消毒效果.为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_____________________。
高三化学综合题中等难度题查看答案及解析
-
元素周期表中第VIIA族元素的单质及其化合物的用途广泛。
(1)氯元素同族的下一周期元素的原子结构示意图为_______,碘是______ (填颜色)固体物质。
(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程___________。此外氰离子还能抑制口腔细菌产生酸,含氟牙膏己经普遍使用。
(3)碘被称为“智力元素”,磺酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与碘化钾生成单质碘。写出该反应的离子方程式_____________。
(4)电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在—定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:

步骤⑤的操作名称____________________。
(5)己知:I2+2S2O32-=S4O62-+2I-。
用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取ag试样溶于水,加入过量KI固体,充分反应,生成白色沉淀,I-被氧化为I2。然后用cmol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O5标准溶液bmL。可选用______作滴定指示剂,滴定终点的现象是_______________。
高三化学简答题困难题查看答案及解析
-
二元弱酸是分步电离的,25时碳酸和草酸的
如下表:
H2CO3
Ka1=4.3×10-7
H2C2O4
Ka1=5.6×10-2
Ka2=5.6×10-11
Ka2=5.42×10-5
(1)设有下列四种溶液:
A.0.1 mol/L的Na2C2O4溶液 B.0.1 mol/L的NaHC2O4溶液
C.0.1 mol/L的Na2CO3溶液 D.0.1 mol/L的NaHCO3溶液
其中,c(H+)最大的是_________,c(OH-)最大的是_________ 。
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插人pH传感器,测得pH变化曲线如图所示。
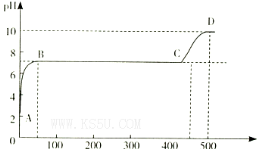
刚开始滴人碳酸钠溶液时发生反应的离子方程式为_________,BC段发生反应的离子方程式为_____,D点时混合溶液中由水电离产生的c(H+)=_________ mol/L。
高三化学填空题困难题查看答案及解析
-
二元弱酸是分步电离的,25时碳酸和草酸的
如下表:
H2CO3
Ka1=4.3×10-7
H2C2O4
Ka1=5.6×10-2
Ka2=5.6×10-11
Ka2=5.42×10-5
(l)设有下列四种溶液:
A.0.1 mol/L的Na2C2O4溶液 B.0.1 mol/L的NaHC2O4溶液
C.0.1 mol/L的Na2CO3溶液 D.0.1 mol/L的NaHCO3溶液
其中,c(H+)最大的是_________,c(OH-)最大的是_________ 。
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示。
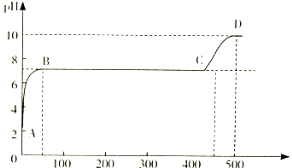
刚开始滴入碳酸钠溶液时发生反应的离子方程式为 ,BC段发生反应的离子方程式为 ,D点时混合溶液中由水电离产生的c(H+)=_________ mol/L。
高三化学填空题困难题查看答案及解析
-
已知,25 ℃时几种弱酸的电离常数如表所示:
弱酸
电离常数
弱酸
电离常数
H2CO3
Ka1=4.3×10-7
Ka2=5.6×10-11
H2C2O4
(草酸)
Ka1=5.9×10-2
Ka2=6.4×10-5
H3PO4
Ka1=7.1×10-3
Ka2=6.3×10-8
Ka3=4.2×10-13
H3C6H5O7
(柠檬酸)
Ka1=7.4×10-4
Ka2=1.7×10-5
Ka3=4.0×10-7
下列有关推断正确的是( )
A. 溶液pH的大小关系为K3PO4>K2HPO4>KH2PO4
B. 在Na2CO3溶液中存在:c(OH-)- c(H+)=c(HCO3-)+ c(H2CO3)
C. 等浓度的NaHCO3、NaHC2O4溶液中前者pH较大
D. H3C6H5O7与Na2CO3溶液反应的产物为Na3C6H5O7、CO2、H2O
高三化学单选题中等难度题查看答案及解析
-
部分弱酸的电离平衡常数如下表:
弱酸
HCOOH
HCN
H2CO3
电离平衡常数
(25℃)
Ka=1.77×10-4
Ka=4.9×10-10
Ka1=4.3×10-7
Ka2=5.6×10-11
下列选项正确的是
A. 2CN-+H2O+CO2=2HCN+CO32-
B. 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C. 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-) < c(K+)-c(CN-)
D. c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,
c(NH4HCO3)>c(NH4CN) >c(HCOONH4)
高三化学选择题中等难度题查看答案及解析