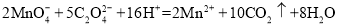-
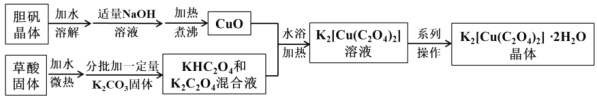
二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]•2H2O}(摩尔质量为354g•mol-1),是一种工业用化工原料。微溶于冷水和酒精,虽可溶于热水但会慢慢分解,干燥时较为稳定,温度高于260℃易分解。实验室以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体的流程如下,请根据相关流程回答:(已知:H2C2O4 CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)
(1)抽滤CuO时若发现滤液中有较多浑浊,应采取的措施是_________。
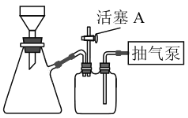
(2)如图装置,经过一系列操作完成CuO的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物; b.关活塞A; c.开活塞A; d.确认抽干; e.加洗涤剂洗涤
(3)KHC2O4和K2C2O4混合溶液制备时K2CO3固体需分批加入的原因是________。
(4)下列说法正确的是________。
A.从K2[Cu(C2O4)2]溶液中结晶时应采用水浴蒸发浓缩、冷却结晶
B.洗涤CuO沉淀和K2[Cu(C2O4)2]•2H2O晶体时可分别用热水和冷水
C.为充分利用滤纸上的CuO,可将滤纸剪碎后加入到热的KHC2O4和K2C2O4混合溶液中,待充分反应后趁热过滤
D.在500℃下烘干K2[Cu(C2O4)2]•2H2O晶体比200℃的效果更好
(5)产品纯度的测定:准确称取制得的晶体试样ag溶于氨水中,并加水定容至250mL,取试样溶液25.00mL,再加入10mL的稀硫酸,用bmol•L-1的KMnO4标准液滴定,消耗KMnO4标准液V mL。
已知: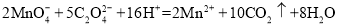
①滴定过程中若不慎将标准液滴在锥形瓶内壁上,用少量蒸馏水冲洗锥形瓶内壁后再继续滴定至终点,实验结果会________。(填“偏大”“偏小”或“无影响”)
②该产品的纯度为________________。(用含字母的最简式表示)
-
(10分)乙二酸( HOOC—COOH)俗称草酸,易溶于水,,电离常数K1=5.4×10-2,K2=5.4×10-5,其盐草酸钙和草酸氢钙均为白色不溶物。无色晶体H2C2O4·2H2O称为草酸晶体,其熔点为101.5℃。草酸晶体失去结晶水得无水草酸,它在157℃升华。根据上述信息,回答下列问题。
(1)向盛有2mL饱和NaHCO3溶液的试管里加入少量乙二酸浓溶液,观察到有大量气泡产生,写出该反应的离子方程式: 。(碳酸:K1=4.4×10-7)
(2)向试管A中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙二酸溶液,按下图Ⅰ组装好装置,加热3—5min。在装有饱和Na2CO3溶液的试管B中有油状且带有香味的液体产生。B中导管口在液面上而不伸入液面下的原因是 。写出乙二酸与少量乙醇反应的化学反应方程式 。

(3)已知草酸分解的化学方程式为:H2C2O4 H2O+CO2↑+CO↑
H2O+CO2↑+CO↑
利用图Ⅱ①和图Ⅱ②加热草酸晶体(夹持仪器忽略),以验证草酸受热是否分解。连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清;
图Ⅱ②:试管里澄清石灰水只变浑浊。
能验证草酸受热分解的装置是 (填图Ⅱ中的编号“①”或“②”)。
(4)图Ⅱ①中冷凝管的作用是: 。
-
草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10﹣2,K2=5.4×10﹣5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解为CO、CO2和H2O。回答下列问题:
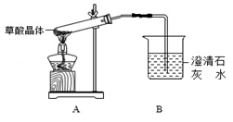
(1)写出草酸晶体分解的化学方程式_________________________________。
(2)甲组同学按照如图所 示的装置,通过实验检验草酸晶体的分解产物。若实验过程中,B中澄清石灰水变浑浊,______(填“能”或“不能”)说明草酸晶体的分解产物中有CO2,原因是______。
示的装置,通过实验检验草酸晶体的分解产物。若实验过程中,B中澄清石灰水变浑浊,______(填“能”或“不能”)说明草酸晶体的分解产物中有CO2,原因是______。
(3)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A和如图所示的部分装置(可以重复选用)进行实验。
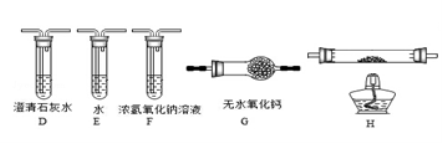
①乙组同学的实验装置中,依次连接的合理顺序为A →___→____→G→ →____。装置H反应管中盛有的物质是  。
。
②F装置的作用是________ ___________________________。
___________________________。
③能证明草酸晶体分解产物中有CO的现象是 。
-
为测定某草酸晶体(H2C2O4•2H2O)样品的纯度,现称取一定质量的该样品,配制成100 mL溶液,取25.00 mL该溶液于锥形瓶中,加适量稀硫酸,用0.100 mol/L的KMnO4溶液滴定(杂质不参与反应)。为省去计算过程,当称取的样品的质量为某数值时,滴定所用KMnO4溶液的毫升数恰好等于样品中草酸晶体的质量分数的100倍。则应称取样品的质量为
A. 2.25 g B. 3.15 g C. 9.00 g D. 12.6 g
-
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上用粗氧化铜(含Fe2O3、FeO、Cu2O以及少量不溶性杂质)为原料制取氯化铜晶体 (CuCl2·2H2O)的为生产流程如下:
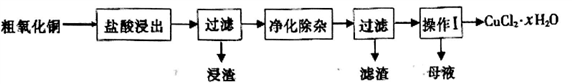
己知:Cu2O在酸性环境中可以生成Cu2+和Cu 回答下列问题:
(1)己知“浸渣”中不含铜单质,写出Cu2O在“盐酸浸出”中发生反应的化学方程式:___________________________________________
(2)“盐酸浸出”中,铜的浸出率与浸出时间的关系如下图所示。由图可得出如下变化规律:

①____________________________
②______________________________。
(3) “净化除杂”需先加入C1O2,其作用是(用离子方程式表示)______________。
然后再调节溶液的pH约为4,可选用的试剂是(填选项字母)______________。
A. CuSO4 B.CuO C.Cu2(OH)2CO3 D.NH3·H2O
(4)“操作I”包含多步实验基本操作,依次是__________、洗涤和风干等。工业上常采用无水乙醇代替水进行洗涤的主要原因是______________。
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,称取ag晶体,加入足量10%的氢氧化钠溶液,过滤、洗涤后,用酒精灯加热至质量不再减轻为止,冷却、称量所得固体质量为bg。计算得x= ______________。(用含a、b的代数式表示)。
-
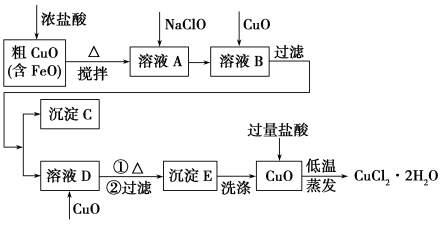
工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产流程如下:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH | ≥9.6 | ≥6.4 | 3~4 |
(1)写出向溶液A中加入NaClO的离子方程式___________________________________。
(2)沉淀C的化学式为________。
(3)实验室如何检验沉淀E已洗涤干净?________。
(4)低温蒸发的目的是______________________________________。
(5)流程中两次加入了CuO,而不是一次性向溶液B中加入过量的CuO,其理由是________________________________________________。
-
草酸亚铁晶体( FeC2O4·2H2O)是一种淡黄色粉末,可用作照相显影剂。某课外小组利用如下实验装置对草酸亚铁品体分解产物进行探究,并设计实验测定草酸亚铁晶体样品纯度。
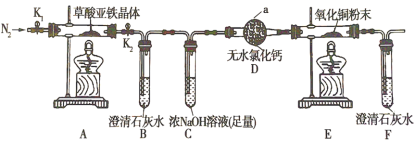
回答下列问题:
(1)仪器a的名称为_____;装置B中澄清石灰水变浑浊,说明气体分解产物中含有_____;
(2)实验前先通一段时间N2目的是________;装置C中浓NaOH溶液的作用是______;
(3)证明草酸亚铁晶体分解产物中含有CO的实验现象是______;
(4)充分反应后,将装置A硬质玻璃管中的残留固体溶于足量的稀硫酸中,无气泡产生,滴加几滴KSCN溶液,溶液不变红,说明固体分解产物是______(填化学式);根据上述实验现象写出草酸亚铁晶体分解的化学方程式_______;
(5)所给实验装置存在明显的设计缺陷,该缺陷是______;
(6)草酸亚铁晶体样品纯度的测定:准确称取12. 000 g某草酸亚铁晶体样品,在一定条件下溶于稍过量的硫酸中,配成250 mL溶液。取25.00 mL上述溶液,用0.100 mol/L KMnO4标准溶液滴定,达到滴定终点时, 消耗35.00 mL KMnO4标准溶液,滴定反应为:FeC2O4·2H2O + KMnO4+ H2SO4→Fe2(SO4)3+CO2↑+ MnSO4 + K2SO4 + H2O(未配平)。则该草酸亚铁晶体样品的纯度为________(已知该草酸亚铁晶体样品中不含其他与高锰酸钾反应的还原性杂质)。
-
草酸晶体的组成可用H2C2O4·2H2O(M=126g/mol)表示,其中混有不参与反应的杂质,为了测定草酸晶体的纯度,进行如下实验:称取m g样品,配成250mL水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为c mol·L-1的KMnO4溶液滴定,所发生的反应: KMnO4+ H2C2O4+ H2SO4 = K2SO4+ CO2↑+ MnSO4+ H2O.试回答:
(1)写出该反应的离子方程式并配平:_________________________________________,该反应发生时产生气体先慢后快的原因是_______________________________________________
(2)实验中,KMnO4溶液应装在_____式滴定管中,因为 ___________________。
(3)滴定过程中需要加入的指示剂为___________(填指示剂的名称或“不需要”),确定反应达到滴定终点时的现象是______________________________________。
(4)在滴定过程中若用c mol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为____________mol·L-1,由此可计算样品中草酸晶体的纯度是________。
-
草酸晶体的组成可用H2C2O4·2H2O(M=126g/mol)表示,其中混有不参与反应的杂质,为了测定草酸晶体的纯度,进行如下实验:称取m g样品,配成250mL水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为c mol·L-1的KMnO4溶液滴定,所发生的反应: KMnO4+ H2C2O4+ H2SO4 = K2SO4+ CO2↑+ MnSO4+ H2O。试回答:
(1)写出该反应的离子方程式并配平:_________________________________________,该反应发生时产生气体先慢后快的原因是_______________________________________________
(2)实验中,KMnO4溶液应装在_____式滴定管中,因为 ___________________。
(3)滴定过程中需要加入的指示剂为___________(填指示剂的名称或“不需要”),确定反应达到滴定终点时的现象是______________________________________。
(4)下列操作会导致测定结果偏低的是_________________________。
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)在滴定过程中若用c mol·L-1的KMnO4溶液V mL,则所配制的草酸溶液的物质的量浓度为___mol·L-1,由此可计算样品中草酸晶体的纯度是________。
-
已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
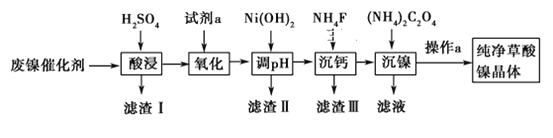
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:_______________________________。
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:_____________。
(3)“调pH”时pH的调控范围为__________________。
(4)写出“沉镍”时发生反应的离子方程式:________________________________,证明Ni2+已经沉淀完全的实验步骤及现象是______________________________,当Ca2+沉淀完全时,溶液中c(F-)>____________mol·L-1(写出计算式即可)。
 CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)