《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法不正确的是 ( )

A.As、S 原子的杂化方式均为 sp3
B.AsH3 的沸点比 NH3 的低
C.As 的价电子排布式为 3d104s24p3
D.已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:1
高二化学单选题简单题
《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法不正确的是 ( )

A.As、S 原子的杂化方式均为 sp3
B.AsH3 的沸点比 NH3 的低
C.As 的价电子排布式为 3d104s24p3
D.已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:1
高二化学单选题简单题
《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法不正确的是 ( )

A.As、S 原子的杂化方式均为 sp3
B.AsH3 的沸点比 NH3 的低
C.As 的价电子排布式为 3d104s24p3
D.已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:1
高二化学单选题简单题查看答案及解析
《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法不正确的是 ( )

A.As、S 原子的杂化方式均为 sp3
B.AsH3 的沸点比 NH3 的低
C.As 的价电子排布式为 3d104s24p3
D.已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:1
高二化学单选题简单题查看答案及解析
《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3)经常用来修改错字,其结构如图所示。下列说法不正确的是( )
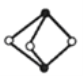
A.As、S原子的杂化方式均为sp3
B.AsH3的沸点比NH3的低
C.与As同周期且基态原子核外未成对电子数目相同的元素只有V
D.已知As2F2分子中各原子均满足8电子结构,分子中σ键和π键的个数比为3:1
高二化学单选题中等难度题查看答案及解析
雌黄 As2S3 和雄黄 As4S4 都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有 抗病毒疗效也用来入药。
(1)砷元素有+2、+3 两种常见价态。雄黄在空气中加热至 300℃时会生成两种氧化物,其 中一种氧化物为剧毒的砒霜(As2O3),则物质 a 是_____,可用双氧水将 As2O3 氧化为 H3AsO4,写出该反应的化学方程式:________。
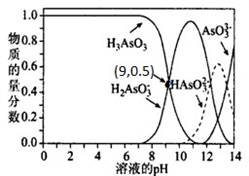
(2)亚砷酸 H3AsO3 可以用于治疗白血病,其在溶液中 存在多种微粒形态,25℃时,各种微粒物质的量分数与 溶液的 pH 关系如图所示。
①人体血液的 pH 在 7.35 ~7.45 之间,用药后人体中 含砷元素的主要微粒是_____。
②下列说法不正确的是_____(填字母序号)。
A.n(H3AsO3):n(H2AsO3-)=1:1 时,溶液显碱性
B.25℃时,H3AsO3 的第一电离平衡常数的值 Ka1=10-5
C.在 K3AsO3 溶液中, c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
③将 KOH 溶液滴人亚砷酸溶液,当 pH 调至 11 时发生反应的离子方程式 是_____。
(3)P 和 As 属于同主族元素,存在亚磷酸(H3PO3),该酸与足量的 NaOH 溶液反应生成Na2HPO3。工业电解 Na2HPO3 溶液可得到亚磷酸,装置示意图如下:
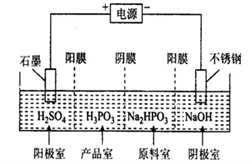
①产品室中反应的离子方程式为_____;
②得到 1mol 亚磷酸的同时,阴极室制得 NaOH 质量为_____g。
高二化学简答题困难题查看答案及解析
(6分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为________。
(2)上述反应中的还原剂是________,反应产生的气体可用________吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为________。若将该反应设计成一原电池,则NO2应该在(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量________(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
高二化学填空题简单题查看答案及解析
高二化学解答题中等难度题查看答案及解析
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。
根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为_______。
(2)上述反应中的氧化剂是_______,反应产生的气体可用_______吸收。
(3)As2S3和HNO3有如下反应:As2S3 + 10H++ 10NO3-→2H3AsO4 + 3S+ 10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为_______。若将该反应设计成原电池,则NO2应该在____(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量____(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5 mol d.无法确定
高二化学填空题中等难度题查看答案及解析
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。
根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为_______。
(2)上述反应中的氧化剂是_______,反应产生的气体可用_______吸收。
(3)As2S3和HNO3有如下反应:As2S3 + 10H+ + 10NO3-→2H3AsO4 + 3S+ 10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为_______。若将该反应设计成原电池,则NO2应该在____(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量____(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5 mol d.无法确定
高二化学填空题简单题查看答案及解析
《日华子本草》中已有关于雄黄的记载“雄黄,通赤亮者为上,验之可以虫死者为真。”雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。 回答下列问题:
(1)基态砷原子的价电子轨道排布图为_______,核外电子占据的最高能级的电子云轮廓图形状为_______。
(2) S、P和N三种元素第一电离能由大到小的顺序是_______。
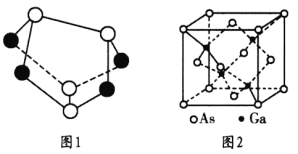
(3) 雄黄(As4S4)的结构如图1所示,S原子的杂化形式为_______。
(4) SO2分子中的键数为______个,分子的空间构型为_______。分子中的大
键可用符号
表示,其中m代表参与形成大
键的原子数,n代表参与形成大
键的电子数(如苯分子中的大
键可表示为
),则SO2中的大
键应表示为______。SO2分子中S—O键的键角_____NO3-中N—O键的键角(填“> ”、“<”、“=”)。
(5)砷化镓是优良的半导体材料,密度为 g • cm-3,其晶胞结构如图2所示。Ga和As 原子半径分别为r1 pm和r2 pm,阿伏加德罗常数值为NA,则砷化镓晶体的空间利用率为________。
高二化学综合题中等难度题查看答案及解析
断肠草(Gelsemium)为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式,下列推断正确的是
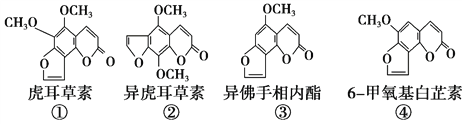
A. ①、②、③、④互为同分异构体
B. ①、③互为同系物
C. 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少
D. ①、②、③、④均能与氢氧化钠溶液反应
高二化学单选题中等难度题查看答案及解析