-
有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:
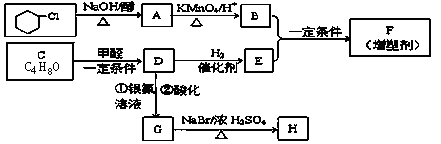
已知: ① (R1、R2代表烃基)
(R1、R2代表烃基)
②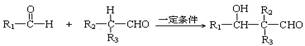
③C能发生银镜反应,且分子中有支链。
请回答:
(1)E中有 种化学环境不同的H原子,原子个数比是 。
(2)D分子中所含官能团的名称是: 。
(3)写出由一氯环己烷到A的化学方程式: 。
(4)写出满足下列条件的D的一种同分异构体的结构简式________。
①与D具有相同的官能团;
②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,则0.1moLH与足量NaOH溶液反应,消耗NaOH
________ moL。
(6)B与E在一定条件下生成F的反应的化学方程式是:________。
-
有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:
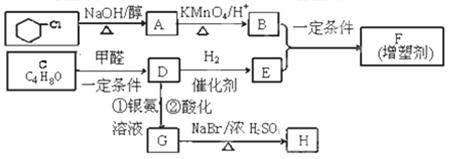
①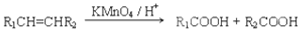 (R1、R2代表烃基)
(R1、R2代表烃基)
② (R1、R2、R3代表烃基或氢原子)
(R1、R2、R3代表烃基或氢原子)
③C能发生银镜反应,且分子中有支链
请回答:
(1)C的结构简式____________,B的结构简式______________ 。
(2)E中有多种化学环境不同的氢原子,原子个数比是______________。
(3)写出由一氯环己烷到A的化学方程式(注明反应条件):______________。
(4)写出满足下列条件的D的一种同分异构体的结构简式_______________。
①与D具有相同的官能团;
②分子中具有两个手性碳原子(连接四个不同原子或基团的碳原子,称为手性碳原子)。
(5)G和H的相对分子质量相差63,H能与NaHCO3溶液反应,H的结构简式是______________。
(6)B与E在一定条件下生成F的反应的化学方程式是:__________________。
-
(16分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,乙酸乙酯的实验室和工业制法常采用如下反应:

请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有________,________。(任写两点只要合理即可)
(2)浓硫酸的作用是:①________、②________。
(3)饱和NaCO3溶液的作用:
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 | 同一反应温度 |
| 反应温度/℃ | 转化率/% | 选择性/% | 反应时间/h | 转化率/% | 选择性/% |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| 选择性100%表示反应无副反应发生 |
根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B. 80 ℃,2 h C. 60 ℃,4 h D.40 ℃,3 h
-
(12分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常用冰醋酸、无水乙醇和浓硫酸混合,在加热条件下反应制得:
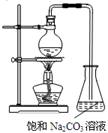
请根据要求回答下列问题:
(1) 写出该反应的化学方程式________
(2)此反应中浓硫酸的作用是 ________
饱和碳酸钠的作用是________
(3)若采用同位素示踪法研究该化学反应,反应物无水乙醇中含有18O,冰醋酸中均为16O,反应后的混合物中,含有18O的物质有________
(4)若用如图所示装置来制备少量的乙酸乙酯,锥形瓶中的现象为________,不过往往产率偏低,其原因可能为(任填2种)
-
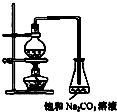
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、妨织等工业。乙酸乙酯的实验室制法常采用如图装置:
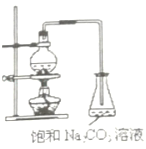
(1)烧瓶中除了乙酸和乙醇之外,还必须加的药品是___,其作用是___。
(2)能不能把饱和Na2CO3溶液换成饱和NaCl溶液?___,为什么?___。
(3)为了乙酸和乙醇回流,减少它们损失,该装置应该改进之处是:___。
(4)分离乙酸乙酯和饱和溶液,所需要的操作是___。
-
琥珀酸二乙酯是良好的增塑剂和特种润滑剂,也是重要的有机合成的中间体。分析下图中物质间的转化关系,回答问题。
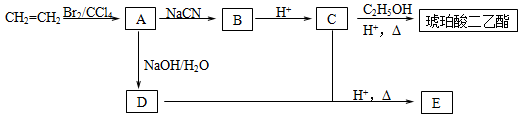
已知:RCN RCOOH
RCOOH
(1)B的结构简式为 。
(2)C的同分异构体中,与C具有相同官能团的是 (写结构简式)。
(3)由C制备琥珀酸二乙酯的化学方程式为: 。
(4)若E为高分子化合物,则由C与D制备E的化学方程式为 。
(5)若E为八元环状化合物,其分子式为 。
-
氨对地球上的生物相当重要,它是许多食物和肥料的重要成分。氨也是制造硝酸、化肥、炸药 的重要原料。氨在国民经济中占有重要地位。回答下列问题:
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
①工业合成氨的热化学方程式是_______________。
②若起始时向容器内放入1 mol N2和3 mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为____________;若在同体积的容器中充人2 mol N2和6 molH2,达平衡后放出的热量为Q2 kJ,则Q2__________(填“>”、“<”或“=”)2Q1。
③已知:

1 mol N-H键断裂吸收的能量约等于__________kJ。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2 (g) 2NH3 (g),其平衡常数K与温度T的关系如下表:
2NH3 (g),其平衡常数K与温度T的关系如下表:
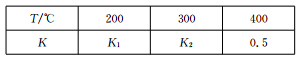
①平衡常数表达式K=_________,K1___________(填“>”、“<”或“一”)K2。
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是__________(填字母)。
a.容器内N2、H2、NH3的浓度之比为1: 3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2 mol、1 mol、2 mol时,则此时该反应_________(填“处于”或“不处于”)平衡状态。
-
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业.乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH
 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)若用右图所示装置来制备少量的乙酸乙酯,其中饱和碳酸钠溶液的作用是______.
(2)此反应以浓硫酸为催化剂,可能会造成______、______等问题.
(3)在图所示的装置中进行50mL 0.50mol/L醋酸与50mL 0.55mol/L NaOH溶液的中和反应.通过测定反应过程中所放出的热量可计算反应热.回答下列问题: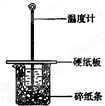
①从实验装置上看,图中尚缺少的一种玻璃用品是______;
②在题述反应条件下,测得反应前醋酸和NaOH溶液的温度均为25.43℃,反应后混合溶液的温度为28.73℃.已知反应前醋酸
和NaOH溶液的密度均为1.0g•cm-3,反应后混合溶液的比热容为c=4.18J/.试写出中和反应的热化学方程式:______.
-
氨在国民生产中占有重要的地位。工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
2NH3(g) △H=-92.4kJ/mol。下表是合成氨反应在某温度下2.0L的密闭容器中进行时,测得的数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
(1)反应进行到2小时时放出的热量为____________kJ。
(2)此条件下该反应的化学平衡常数K=____________(保留两位小数)。
(3)有两个密闭容器A和B,A容器保持恒容,B容器保持恒压,起始时向容积相等的A、B中分别通入等量的NH3气体,均发生反应:2NH3(g) 3H2(g)+N2(g)。则:
3H2(g)+N2(g)。则:
①达到平衡所需的时间:t(A)_____t(B),平衡时,NH3的转化率:a(A)______a(B) (填“>”、“=”或“<”)。
②达到平衡后,在两容器中分别通入等量的氦气。A中平衡向_________移动,B中平衡向_________移动。(填“向正反应方向”、“向逆反应方向”、“不”)。
(4)在三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数[φ(NH3)]随时间变化的曲线如图所示.下列说法中正确的是_____(填字母,下同)。
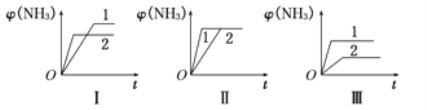
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
-
氨是重要的无机化工产品之一,在国民经济中占有重要地位。我国采用铁触媒(以铁为主的混合物) 做催化剂合成氨。回答下列问题:
(1)Fe基态原子核外电子排布式为____。氮化铁是一种重要的无机化合物,不溶于水,暴露在潮湿环境中可释放出氨气,元素Fe和N中,第一电离能较大的是_____,基态原子核外未成对电子数较多的是_______。
(2)N的氧化物有N2O等,N2O与CO2互为等电子体,N2O的空间构型为__________。
(3)N有多种氢化物,其中肼(N2H4)常用作火箭推进剂的燃料,N2H4中N 原子的杂化形式为____。
(4)N、P、As为同族元素,NH3、PH3、AsH3三种物质的沸点由高到低的顺序为_____。原因是____。
(5)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中存在的化学键类型有_______。
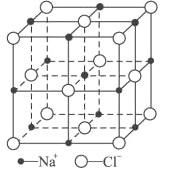
(6)FeO晶体的晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为428pm,则该晶体的密度为____g/cm3(列出计算式即可,用NA表示阿伏加德罗常数的值)。
 。
。

(R1、R2代表烃基)


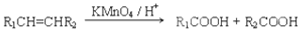 (R1、R2代表烃基)
(R1、R2代表烃基) (R1、R2、R3代表烃基或氢原子)
(R1、R2、R3代表烃基或氢原子)







 。
。