乙酸乙酯广泛用于药物、染料、香料等工业, 某学习小组设计甲、乙两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯。下列说法不正确的是

A.浓硫酸能加快酯化反应速率
B.装置乙中的球形干燥管能防止倒吸
C.振荡a、b 两试管发现油状液体层变薄 ,主要是乙酸乙酯溶于Na2CO3溶液所致
D.可用分液的方法分离出乙酸乙酯
高二化学单选题中等难度题
乙酸乙酯广泛用于药物、染料、香料等工业, 某学习小组设计甲、乙两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯。下列说法不正确的是

A.浓硫酸能加快酯化反应速率
B.装置乙中的球形干燥管能防止倒吸
C.振荡a、b 两试管发现油状液体层变薄 ,主要是乙酸乙酯溶于Na2CO3溶液所致
D.可用分液的方法分离出乙酸乙酯
高二化学单选题中等难度题
乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是
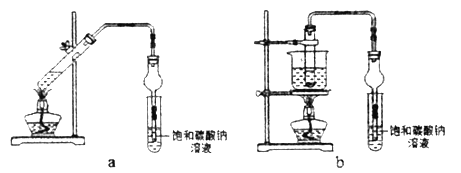
A. 浓硫酸能加快酯化反应速率 B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少 D. 可用分液的方法分离出乙酸乙酯
高二化学单选题中等难度题查看答案及解析
乙酸乙酯广泛用于药物、染料、香料等工业, 某学习小组设计甲、乙两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯。下列说法不正确的是

A.浓硫酸能加快酯化反应速率
B.装置乙中的球形干燥管能防止倒吸
C.振荡a、b 两试管发现油状液体层变薄 ,主要是乙酸乙酯溶于Na2CO3溶液所致
D.可用分液的方法分离出乙酸乙酯
高二化学单选题中等难度题查看答案及解析
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
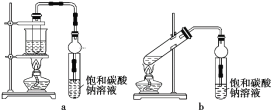
完成下列填空:
(1)实验时,通常加入过量的乙醇,原因是______。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是________;
(2)饱和Na2CO3溶液的作用是________、_______、________。
(3)写出反应原理:________。
(4)若用b装置制备乙酸乙酯,其缺点有_______、________。由b装置制得的乙酸乙酯粗产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是_______,分离乙酸乙酯与该杂质的方法是______。
高二化学实验题中等难度题查看答案及解析
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验可用a装置来制备。完成下列填空:
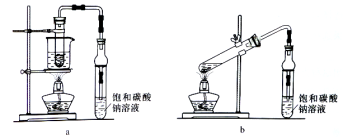
(1)实验时,通常加入过量的乙醇,原因是______________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是_______________;浓硫酸用量又不能过多,原因是____________。
(2)饱和Na2CO3溶液的作用是_______________。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,_________、________,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有__________、__________。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方法是_______________。
高二化学实验题简单题查看答案及解析
乙酸乙酯广泛存在于药物、染料、香料等工业,中学化学实验常用装置来制备:
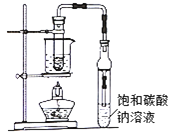
完成下列填空:
(1)写出实验室制备乙酸乙酯的化学方程式:_______通常加入过量乙醇,原因是_______
(2)饱和碳酸钠溶液的作用是①__________②__________
(3)若用装置制备乙酸乙酯,其缺点有_________、_________。边反应边通过分液漏斗边滴加乙酸,边加热蒸出乙酸乙酯。这样操作可以提高酯的产率。其原因是______
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物。下列框图是分离操作步骤流程图:
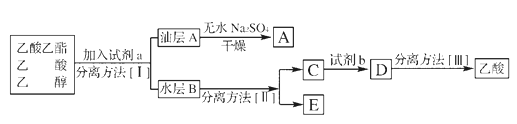
分离方法II是____________试剂b是____________。
高二化学实验题简单题查看答案及解析
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备.
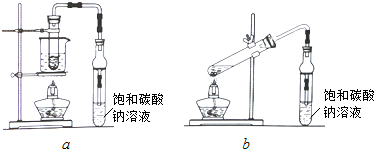
完成下列填空:
(1)用a装置进行实验时,烧杯中的液体是用___________(选填“沸点较高的油”、“水”);装置a, b中均使用了防倒吸装置,产生倒吸的主要原因是___________。加入数滴浓硫酸既能起催化作用,但实际用量多于此量,原因是___________;浓硫酸用量又不能过多,原因是___________。
(2)反应结束后,将试管中收集到的产品倒入分液漏斗中,___________、___________,然后分液。
(3)若用b装置制备乙酸乙酯,其缺点有___________、___________。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是___________,分离乙酸乙酯与该杂质的方法是___________。其中饱和食盐水洗涤的主要作用是___________,饱和氯化钙溶液洗涤是为除去___________杂质。
高二化学实验题困难题查看答案及解析
乙酸乙酯是一种重要的化工原料,广泛用于药物染料、香料等工业。查阅资料得到下列数据:
| 物质 | 沸点/℃ | 密度/ | 相对分子质量 | 水溶性 |
| 乙醇 | 78.0 | 0.8 | 46 | 互溶 |
| 乙酸 | 118.0 | 1.1 | 60 | 可溶 |
| 乙酸乙酯 | 77.5 | 0.9 | 88 | 微溶 |
| 乙醚 | 34.6℃ | 0.7 | 74 | 微溶 |
| 浓硫酸(98%) | 338.0 | 1.8 | 98 | 易溶 |
| 无水氯化钙 | 可与乙醇形成难溶于水的CaCl2·6C2H5OH |
请回答以下问题:
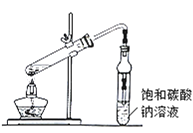
(1)实验室常用下图装置来制备乙酸乙酯。
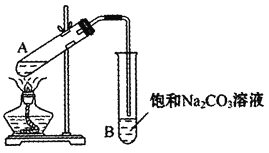
①配制反应混合液时,乙醇、冰醋酸和浓硫酸的混合顺序是________;浓硫酸对反应有催化作用,但加入的浓硫酸不能太多也不能太少,原因是________。
②防止加热时液体暴沸,需要在试管加入碎瓷片,如果加热一段时间后发现忘记了加碎瓷片,应该采取的正确操作是________。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③实验中饱和碳酸钠溶液的作用是________。
(2)产品纯化。分液法从试管B中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,首先向乙酸乙酯中加入无水氯化钙,除去________(填名称);然后再加入无水硫酸钠除去水,最后进行________(填操作名称),得到较纯净的乙酸乙酯。
(3)该实验中用30 g乙酸与46 g乙醇反应,如果实际得到的乙酸乙酯的质量是30.8 g,则该实验中乙酸乙酯的产率是________。(产率指的是某种生成物的实际产量与理论产量的比值)
(4)另一化学小组设计下图所示的装置制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)。此装置和上图装置相比的优点是________(写出一条即可)。
高二化学实验题中等难度题查看答案及解析
乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a制备,b会发生较多的副反应.回答下列问题:
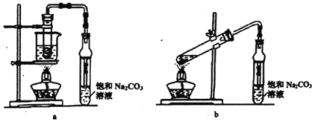
(1)实验时,通常加入过量的乙醇,原因是_____。
(2)饱和Na2CO3溶液的作用是_____。
(3)反应结束后,将盛有饱和Na2CO3溶液的试管中收集到的产品倒入分液漏斗中,_____、_____,然后分液。
高二化学实验题简单题查看答案及解析
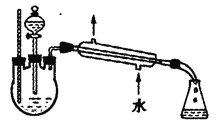
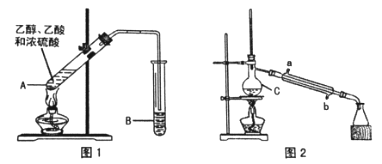
乙酸乙酯广泛用于药物、燃料、香料等工业,在中学化学实验室里常用下图装置来制备乙酸乙酯。(部分夹持仪器已略去)
已知:
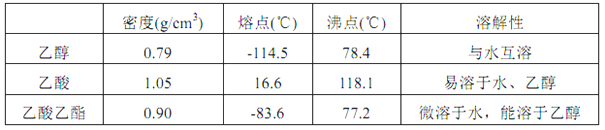
(1)制备粗品(图1)
在A 中加入少量碎瓷片,将三种原料依次加入A 中,用酒精灯缓慢加热,一段时间后在B 中得到乙酸乙酯粗品。
①浓硫酸、乙醇、乙酸的加入顺序是_______________________,A 中发生反应的化学方程式是______________________________。
②A 中碎瓷片的作用是_____________________________________,长导管除了导气外,还具有的作用是_____________________________。
③B 中盛装的液体是_____________________,收集到的乙酸乙酯在 ___________层(填“上”或“下”)。
(2)制备精品(图2)
将B 中的液体分液,对乙酸乙酯粗品进行一系列除杂操作后转移到C 中,利用图2 装置进一步操作即得到乙酸乙酯精品。
①C 的名称是___________________。
②实验过程中,冷却水从_________口进入(填字母);收集产品时,控制的温度应在________℃左右。
高二化学实验题中等难度题查看答案及解析
酯广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯一般通过乙酸和乙醇酯化合成。请根据要求回答下列问题:
(1)将乙酸、乙醇、浓硫酸混合的同时加入碎瓷片的目的是____,在合成过程中控制乙酸过量的作用是____。
(2)向反应后混合液中加入5% Na2CO3溶液洗涤至中性。分液,取上层油状液体,加入无水Na2SO4固体,过滤后蒸馏,收集76~78 ℃馏分。实验中加入少量无水Na2SO4固体的目的是____。
(3)此反应以浓硫酸为催化剂,会造成____等问题,目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
| *选择性100%表示反应生成的产物是乙酸乙酯和水 |
根据表中数据,下列____(填字母)为该反应的最佳条件。
A.40℃,3h B.60℃,4h C.80℃,2h D.120℃,4h
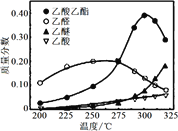
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OHCH3COOC2H5+2H2,在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。当反应温度高于300 ℃时,乙酸乙酯的质量分数迅速下降的原因可能是____。
高二化学实验题简单题查看答案及解析