-
已知 CN- 与 N2互为等电子体,则下列有关 HCN 的说法正确的是
A.HCN 分子的立体构型为 V 形
B.HCN 分子中σ 键与π键个数比为1:2
C.已知 HCN 标况下为液态,与水、乙醇互溶,则其固态时为分子晶体
D.HCN 制备:C2H4+NH3=HCN+CH4+H2,该方程式涉及到的非极性分子有2种
高二化学单选题简单题查看答案及解析
-
CH
、—CH3、CH
都是重要的有机反应中间体,有关它们的说法正确的是( )
A. 它们互为等电子体,碳原子均采取sp2杂化
B. CH
与NH3、H3O+互为等电子体,立体构型均为正四面体形
C. CH
中的碳原子采取sp2杂化,所有原子均共面
D. CH
与OH-形成的化合物中含有离子键
高二化学单选题简单题查看答案及解析
-
下列说法正确的是( )
A. SO2 与 CO2 的分子立体构型均为直线形
B. H2O 和 NH3 中的中心原子杂化方式相同
C. CS2 为空间构型为 V 形的极性分子
D. HCN、SiF4 和 SO32- 的中心原子均为 sp3 杂化
高二化学单选题简单题查看答案及解析
-
下列说法中正确的是( )
A.CH4,C2H2,HCN都是含有极性键的非极性分子
B.CO2与SO2的立体构型相似,都是非极性分子
C.葡萄糖分子(HOCH2—CHOH—CHOH—CHOH—CHOH—CHO)中的手性碳原子数为5
D.酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多
高二化学单选题中等难度题查看答案及解析
-
下列说法中正确的是( )
A. CH4,C2H2,HCN都是含有极性键的非极性分子
B. CO2与SO2的立体构型相似,都是非极性分子
C.
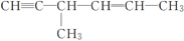 分子中含有1个手性碳原子
分子中含有1个手性碳原子D. 无机含氧酸分子中有几个氢原子,它就属于几元酸
高二化学单选题中等难度题查看答案及解析
-
按顺序填写下列分子或离子中中心原子的孤电子对数,杂化轨道类型,立体构型名称。
(1)HCN__________、__________、__________;
(2)NH2-__________、__________、__________;
(3)NO2+_________、 __________、 __________;
高二化学填空题中等难度题查看答案及解析
-
根据分子结构与性质相关知识,回答下列问题:
(1)NH3分子的VSEPR模型为______________;SO2分子的立体构型为:_______________;
(2)根据等电子原理,写出CN-的电子式_______;SCN-中心原子的杂化方式为 ________;
(3)向CuSO4溶液中逐渐滴加氨水至过量,现象为:__________________________;写出该过程中依次发生的反应离子方程式:_________________________,并写出[Cu(NH3)4]2+的结构简式________。
高二化学综合题中等难度题查看答案及解析
-
若ABn分子的中心原子上没有孤对电子,应用价层电子对互斥模型理论,判断下列说法正确的是
A. n=3时,则分子的立体构型为V形
B. n=2时,则分子的立体构型平面三角形
C. n=4时,则分子的立体构型为正四面体形
D. n=4时,则分子的立体构型为三角锥形
高二化学单选题简单题查看答案及解析
-
若ABn分子的中心原子A上没有未用于形成共价键的孤电子对,根据价层电子对互斥理论,下列说法正确的是( )
A、若n=2,则分子的立体构型为V形
B、若n=3,则分子的立体构型为三角锥形
C、若n=4,则分子的立体构型为正四面体形
D、以上说法都不正确
高二化学选择题简单题查看答案及解析
-
若ABn型分子的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是( )
A.若n=2,则分子的立体构型为V形 B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形 D.以上说法都不正确
高二化学选择题简单题查看答案及解析