-
硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(含2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
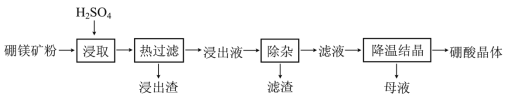
已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0 g、8.7 g、14.8 g、40.2g。Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4。
(1)“浸取”时主要反应的化学方程式为_____________________。
(2)“浸取”后,采用“热过滤”的目的是___________________________。
(3)“浸出液”显酸性,含H3BO3和Mg2+、SO42-,还含有其他杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是__________。H2O2的作用是______(用离子方程式表示)。
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4•H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是_____________。
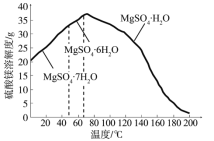
A. 升温结晶 B. 降温结晶 C. 加压升温结晶 D. 降压降温结晶
(5)在实际生产中为了提高原料的综合利用率,可以利用除杂后滤渣作为提炼铝的原料,工艺流程为:
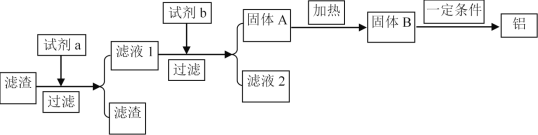
试剂a可选用________(化学式)溶液,若试剂b为AlCl3则由滤液得固体A的离子反应方程式为___________,在实际工业生产中,流程中的一定条件指的是________。
-
I、硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
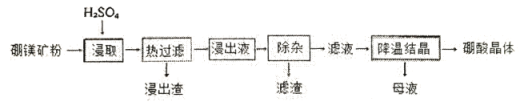
已知: H3BO3在20°C、40°C、60°C、100°C时溶解度依次为5.0g、8.7g、14.8g、40.2 g。
(1)浸出渣除了CaSO4外,还有_____________; (写化学式)
(2)“浸出液”显酸性,含H3BO3和Mg2+、SO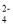 , 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是_____________; H2O2的作用是___________________(用离子方程式表示)。
, 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是_____________; H2O2的作用是___________________(用离子方程式表示)。
(3)“浸取”后,采用“热过滤”的目的是_________________________
(4)以硼酸为原料可制得硼氢化钠(NaBH4)它是有机合成中的重要还原剂,其电子式为____________
II、为了分析矿石中铁元素的含量,先将浸出液处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式:5Fe2+ + MnO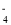 + 8H+= 5Fe3+ + Mn2+ + 4H2O
+ 8H+= 5Fe3+ + Mn2+ + 4H2O
(5)滴定前是否要滴加指示剂?____________(填“是”或“否");
(6)达到滴定终点的标志是_____________________________________
(7)某同学称取4.000g样品,经处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol/L KMnO4标准溶液滴定。达到滴定终点时消耗标准溶液20.00 mL, 则样品中铁元素的质量分数是_________
-
轻质氧化镁和硼酸(H3BO3)都是重要的化工原料,可采用硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸和轻质氧化镁,其工艺流程如图:
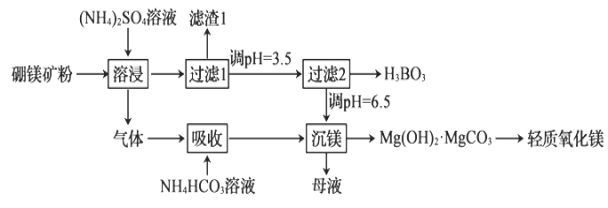
下列叙述错误的是( )
A.Fe2O3、Al2O3都不能溶于(NH4)2SO4溶液
B.进入“吸收”工序中的气体为NH3
C.若“过滤2”时调节溶液的碱性越强得到的硼酸越多
D.“沉镁”中得到的母液经加热后可返回“溶浸”工序循环使用
-
硼酸(H3BO3)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能,提高机械强度,缩短熔融时间。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、Al2O3和SiO2等)为原料制备硼酸的工艺流程如下(部分操作和条件略):
I.向铁硼矿粉中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量双氧水,再调节溶液的pH约为5;
Ⅲ.过滤,将所得滤液蒸发浓缩、冷却结晶、过滤得粗硼酸和含镁盐的母液;
Ⅳ.粗硼酸精制得硼酸。
已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀时 | 3.8 | 5.8 | 2.2 | 10.6 |
| 完全沉淀时 | 4.7 | 8.3 | 4.0 | 12 |
注:金属离子的起始浓度为0.01 mol·L-1
请回答:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式:___________。
(2)为提高步骤I中的反应速率,可采取的措施有_________________(写出两条)。
(3)步骤Ⅱ的目的是_______________________。
(4)“粗硼酸”中的主要杂质是 ___________________。
-
硼酸(H3BO3)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能,提高机械强度,缩短熔融时间。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、Al2O3和SiO2等)为原料制备硼酸的工艺流程如下(部分操作和条件略):
I.向铁硼矿粉中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量双氧水,再调节溶液的pH约为5;
Ⅲ.过滤,将所得滤液蒸发浓缩、冷却结晶、过滤得粗硼酸和含镁盐的母液;
Ⅳ.粗硼酸精制得硼酸。
已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀时 | 3.8 | 5.8 | 2.2 | 10.6 |
| 完全沉淀时 | 4.7 | 8.3 | 4.0 | 12 |
注:金属离子的起始浓度为0.01 mol·L-1
请回答:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式:___________。
(2)为提高步骤I中的反应速率,可采取的措施有_________________(写出两条)。
(3)步骤Ⅱ的目的是_______________________。
(4)“粗硼酸”中的主要杂质是 ___________________。
-
轻质氧化镁和硼酸(H3BO3)都是重要的化工原料,可采用硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸和轻质氧化镁,其工艺流程如图:

下列叙述错误的是( )
A.Fe2O3、Al2O3都不能溶于(NH4)2SO4溶液
B.进入“吸收”工序中的气体为NH3
C.若“过滤2”时调节溶液的碱性越强得到的硼酸越多
D.“沉镁”中得到的母液经加热后可返回“溶浸”工序循环使用
-
以工业生产硼砂所得废渣硼镁泥为原料制取MgSO4·7H2O的过程如图所示:
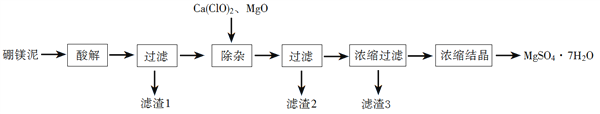
硼镁泥的主要成分如下表:
| MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
| 30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
回答下列问题:
(1)“酸解”时应该加入的酸是_______,“滤渣1”中主要含有_________(写化学式)。
(2)“除杂”时加入次氯酸钙、氧化镁的作用分别是________、_______。
(3)判断“除杂”基本完成的检验方法是____________。
(4)分离滤渣3应趁热过滤的原因是___________。
-
硼镁矿(主要成分为Mg2B2O5·H2O)与硫酸反应可制备硼酸(H3BO3),下列措施能增大该反应速率的是( )
A. 增加反应时间 B. 降低反应温度
C. 减小H2SO4浓度 D. 减小硼镁矿颗粒粒度
-
根据下列实验现象,可以得到相应结论的是
| 实验 | 现象 | 结论 |
| A | 将少量的饱和硼酸溶液滴加到碳酸钠溶液中 | 无气泡 | 酸性:H2CO3>H3BO3 |
| B | 向均盛有2mL5% H2O2溶液的两支试管中分别滴入0.3mol/LFeCl3和0.2mol/LCuCl2溶液各1mL | 前者生成气泡的速率更快 | 催化效果: Fe3+> Cu2+ |
| C | 分别向等物质的量浓度、等体积的KCl和KI的溶液,滴加2滴稀的Ag(NH3)2OH溶液,充分振荡后 | KCl溶液中无白色沉淀,KI溶液中有黄色沉淀 | 微粒结合Ag+的能力:I->NH3>Cl- |
| D | 向1mL2mol/L的NaOH溶液中,滴加1-2滴1mol/ L MgCl2溶液,再滴加2滴1mol/ L FeCl3溶液 | 先有白色沉淀,后有红褐色沉淀 | Ksp:Mg(OH)2>Fe(OH)3 |
A. A B. B C. C D. D
-
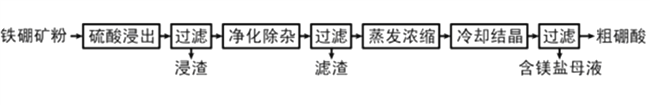
硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应生成硼酸(H3BO3)的化学方程式_____________。为提高浸出速率,除适当增加硫酸的浓度外,还可采取的措施有_________(写出两条)。
(2)利用_______的磁性,可将其从“矿粉”中分离。“浸渣”中的物质是______(写化学式)。
(3) “净化除杂”需先加H2O2溶液,作用是(用离子方程式表示)_______。然后再调节溶液的pH约为5,目的是________。
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为_______。

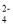 , 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是_____________; H2O2的作用是___________________(用离子方程式表示)。
, 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是_____________; H2O2的作用是___________________(用离子方程式表示)。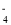 + 8H+= 5Fe3+ + Mn2+ + 4H2O
+ 8H+= 5Fe3+ + Mn2+ + 4H2O





