-
铝及其化合物广泛应用于金属冶炼、有机合成等领域。
(1)铝热反应可以冶炼金属铬,Cr3+基态核外电子排布式为___________。
(2)AlCl3可作下列反应的催化剂。
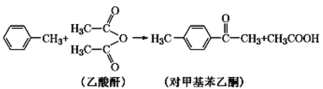
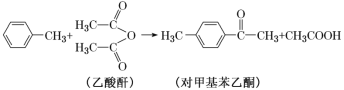
①1mol对甲基苯乙酮分子中含有的σ键数目为__________。
②CH3COOH与H2O可以任意比例互溶的原因是_____________。
(3)用价层电子对互斥理论解释 的键角大于
的键角大于 的原因是__________。
的原因是__________。
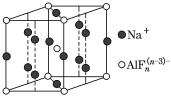
(4)某遮光剂的晶胞如图所示,由晶胞可知n=________。
-
铝及其化合物广泛应用于金属冶炼、有机合成等领域。
(1)铝热反应可以冶炼金属铬,Cr3+基态核外电子排布式为____________________。
(2)AlCl3可作反应的催化剂。

①1 mol对甲基苯乙酮分子中含有的σ键数目为__________。
②CH3COOH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为_______________。
(3)用价层电子对互斥理论解释SO 的键角大于SO
的键角大于SO 的原因是_______________。
的原因是_______________。
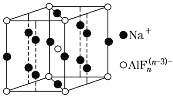
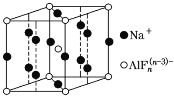
(4)某遮光剂的晶胞如图所示,由晶胞可知n=________。
(5)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体 的中心原子的杂化形式为______, 空间构型为_____。
的中心原子的杂化形式为______, 空间构型为_____。
大π键可用符号 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为 ,则
,则 中大π键应表示为__________。
中大π键应表示为__________。
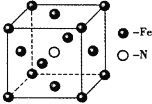
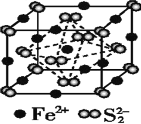
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为______cm。(阿伏加德罗常数用NA表示)
-
铝及其化合物广泛应用于金属冶炼和有机合成等领域。
(1)铝热反应可以冶炼金属铬,基态铬原子的核外电子排布式为:_______________________。
(2)AlCl3可用作下列反应的催化剂
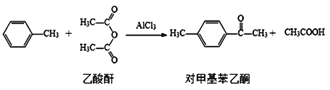
①乙酸酐分子中发生sp3杂化的原子共有______个
②CH3COOH和H2O可以以任意比例互溶,其原因是它们均是极性分子和_________________。
③单个AlCl3分子的空间构型为_______。
(3)在氧化铝的作用下,N4H4(SO4)2可同碱反应生成一种类似白磷的N4分子,1molN4分子中含有的共价键的物质的量为_____mol
(4)某遮光剂的晶胞如图甲(黑球为Na+,白球为AlFn(n-3)-阴离子),由图可推算知,n=________。

(5)由Fe和Y形成的某化合物的晶胞如图乙所示,该晶胞中与亚铁离子距离相等并且最近的亚铁离子有_____个。 另有一种有缺陷的Fe和Y形成的化合物的晶体由Fe2+,Fe3+,Y2-及空隙组成,可表示为Fe0.98Y,则该晶体中,n(Fe2+) : n(Fe3+) =______________。
-
金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有________种能量不同的电子;很多不饱和有机物在Ni催化下可以H2发生加成反应,如①CH2═CH2、②HC≡CH、③  、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
-
金属镍及其化合物在合金材料以及催化剂等方面应用广泛,Ni的基态原子有________种能量不同的电子;很多不饱和有机物在Ni催化下可以H2发生加成反应,如①CH2═CH2、②HC≡CH、③  、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
、④HCHO等,其中碳原子不是采取sp2杂化的分子有________(填物质编号),HCHO分子的立体构型为________
-
(12分)钴(Co)是一种重要的战略金属,钴及其合金广泛应用于电机、机械、化工、航空和航天等领域。钴在化合物中通常以+2、+3的形式存在。
(1)写出基态Co原子的核外电子排布式 ;
(2)Co2+、Co3+都能与CN—形成配位数为6的配离子。CN—中碳原子的杂化方式为 ;1mol HCN分子中σ键的数目为 。
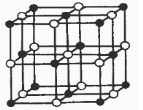
(3)Co的一种氧化物的晶胞如图所示(其中黑球代表Co),则该氧化物的化学式为 在该晶体中与一个氧离子等距离且最近的Co离子所形成的空间构型为 。
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4—,该配离子是一种相当强的还原剂,在加热时能与水反应生成[Co(CN)6]3—,写出该反应的离子方程式 。
-
碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
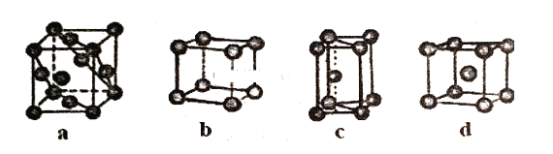
(3)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___ (填字母)。
-
钴(Co)是一种重要的战略金属,钴及其合金广泛应用于电机、机械、化工、航空和航天等领域。钴在化合物中通常以+2、+3的形式存在。
(1)写出基态Co原子的核外电子排布式___________________;
(2)Co2+、Co3+都能与CN-形成配位数为6的配离子。CN-中碳原子的杂化方式为_____;1mol HCN分子中σ键的数目为_________。
(3)Co的一种氧化物的晶胞如图所示(其中黑球代表Co),则该氧化物的化学式为_______,在该晶体中与一个氧离子等距离且最近的Co离子所形成的空间构型为___________。
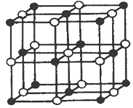
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子是一种相当强的还原剂,在加热时能与水反应生成[Co(CN)6]3-,写出该反应的离子方程式__________________。
-
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________。
(2)NH3是一种很好的配体,NH3的沸点______(填“高于”“等于”或“低于”)AsH3。
(3)科学家通过X射线测得胆矾结构示意图可简单表示如下,图中虚线表示的作用力为________________。
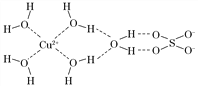
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于________(填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)As 的卤化物的熔点如下:
| AsCl3 | AsBr3 | AsI3 |
| 熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是________________。
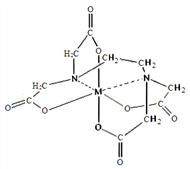
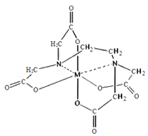
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________。
-
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________。
(2)NH3是一种很好的配体,NH3的沸点______(填“>”“=”或“<”)AsH3。
(3)N原子核外有______种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为___________。
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为________________。

(5)As的卤化物的熔点如下:
| AsCl3 | AsBr3 | AsI3 |
| 熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是________________。
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________。
(7)FeS2晶体的晶胞如图所示。晶胞边长为anm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_________g·cm-3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为_________nm。
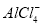 ,与
,与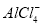 互为等电子体的分子为________。
互为等电子体的分子为________。