-
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出 性质。
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于 (填“酸性”、“碱性”或“两性”,下同)氧化物,Al2O3属于 氧化物。
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是 ;
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是 。
-
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质___________(填序号,下同);
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
②将SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________。
A.S2— B.S C.SO32— D.SO42—
(2)从物质分类的角度可以推测物质的性质。现有由MgO、Al2O3、Fe2O3、SiO2组成的某混合物试样。
①其中Al2O3属于_______氧化物,MgO和Fe2O3属于_________氧化物(填“酸性”、“碱性”或“两性”);
②将试样溶于过量的盐酸中,过滤,滤渣的主要成分是_________;再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是_________;
③若将该试样直接溶于过量的NaOH溶液中,所发生的反应的化学方程式是______________________(可任意写其中一个)。
-
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质___________(填选项,下同);
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
②将SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是______________。
A.S2- B.S C. SO42- D. SO32-
(2)从物质分类的角度可以推测物质的性质。现有由MgO、Al2O3、Fe2O3、SiO2组成的某混合物试样。
①其中Al2O3 属于_____氧化物,MgO 和Fe2O3属于_____氧化物(填“酸性”、“ 碱性”或“两性”);
②将试样溶于过量的盐酸中,过滤,滤渣的主要成分是_____ (写化学式,下同);再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是____________________。
-
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是 。
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是 。
A.S2- B.S C.SO32- D.SO42-
②亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现有试剂:溴水、H2S、稀硫酸。
请选取合适的试剂证明Na2SO3具有还原性, 并写出该反应的离子方程式为: .
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中属于碱性氧化物的是 。
②现取一份蛇纹石试样进行实验:
I.先将其溶于过量的盐酸中、过滤,滤渣的主要成分是 。
II.再向滤液中加入NaOH溶液至过量、过滤,滤渣中的主要成分是 。
-
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
① 的性质___________(填序号,下同)。
的性质___________(填序号,下同)。
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
②将 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________
A. B.
B. C.
C. D.
D.
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由 、
、 、
、 、
、 组成。其中
组成。其中 属于_______氧化物,
属于_______氧化物, 和
和 属于_________氧化物(填“酸性”、“碱性”或“两性”)。
属于_________氧化物(填“酸性”、“碱性”或“两性”)。
②现取一份蛇纹石试样进行实验:
I.先将其溶于过量的盐酸中、过滤,滤渣的主要成分是_________。
II.再向滤液中加入 溶液至过量、过滤,滤渣中的主要成分是_________。
溶液至过量、过滤,滤渣中的主要成分是_________。
③若将少量的蛇纹石试样直接溶于过量的 溶液中,所发生的两个反应的化学方程式是_________________________。
溶液中,所发生的两个反应的化学方程式是_________________________。
-
利用化合价推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质________________(填序号,下同)
A.只有氧化性 B.只有还原性 C.既有还原性又有氧化性
②SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应后,锰元素被还原成Mn2+,写出上述反应的离子方程式_________________________________
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的离子方程式为__________________________________________________为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配置的NaOH溶液反应制备。
①用硫酸亚铁晶体配置上述硫酸亚铁溶液时,还需加入_________来防止Fe2+被氧化
②除去蒸馏水中溶解的O2常采用_______的方法
(3)检验Fe3+的方法:_______________________(写出加入试剂的化学式和现象与结论)
-
利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
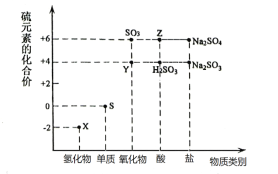
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___(填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为___。
(3)检验物质Y的方法是___。
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为___。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___(填代号)。
a.Na2S+S b.SO2+Na2SO4 c.Na2SO3+S d.Na2SO3+Na2SO4 e.SO2+ Na2S2+Na2CO3
(6)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL0.05 mol·L-1的Na2SO3溶液与20mL0.02mol·L-1的K2Cr2O7溶液恰好完全反应时,Cr元素在还原产物中的化合价为___。
-
利用元素的化合价推测物质的性质是化学研究的重要手段。图是硫元素的常见化合价与部分物质类别的对应关系。
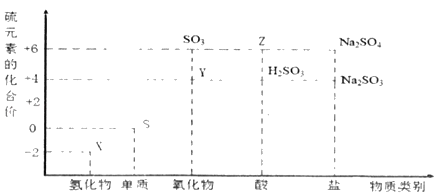
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的氧化物为_____(填化学式)。
(2)将X与Y混合可生成淡黄色固体,该反应的化学方程式为_____。
(3)Z的浓溶液与碳在一定条件下可以发生反应,体现了Z的_____性。
(4)写出硫与浓硫酸在加热条件下反应的化学方程式_____。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方法理论上可行的是_____(填字母)。
a.Na2SO3+S b.Na2S+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
-
利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系:
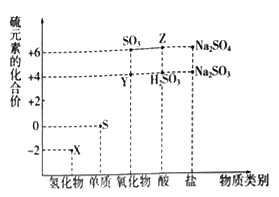
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式).
(2)将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为_______.
(3)检验物质Y的方法是_______________________________.
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______.
(5)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr207氧化为Na2SO4则24mL 0.05mol•L﹣1的Na2SO3溶液与 20mL 0.02mol•L﹣1的溶液恰好反应时,Cr元素在还原产物中的化合价为________.
-
利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系:

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式).
(2)将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为_______.
(3)检验物质Y的方法是_______________________________.
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______.
(5)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr207氧化为Na2SO4则24mL 0.05mol•L﹣1的Na2SO3溶液与 20mL 0.02mol•L﹣1的溶液恰好反应时,Cr元素在还原产物中的化合价为________.
的性质___________(填序号,下同)。
通入酸性
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________
B.
C.
D.
、
、
、
组成。其中
属于_______氧化物,
和
属于_________氧化物(填“酸性”、“碱性”或“两性”)。
溶液至过量、过滤,滤渣中的主要成分是_________。
溶液中,所发生的两个反应的化学方程式是_________________________。



