-
CuSO4和Cu(NO3)2是自然界中重要的铜盐。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子基态核外电子排布式为____________,
(2)SO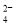 的立体构型是____,与SO
的立体构型是____,与SO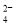 互为等电子体的一种分子为_______(填化学式)。
互为等电子体的一种分子为_______(填化学式)。
(3)利用CuSO4和NaOH制备的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如图所示。
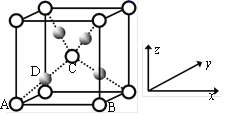
①该晶胞的原子坐标参数A为(0,0,0),B为(1,0,0),C为(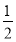 ,
,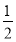 ,
,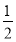 )。则D的坐标参数为________,它代表________原子。
)。则D的坐标参数为________,它代表________原子。
②若Cu2O晶体密度为d g·cm-3,晶胞参数为a pm,则阿伏加德罗常数值NA=_____。
-
含硼、氮、磷、铜、锌的化合物有许多重要用途。回答下列问题:
(1)基态B原子电子占据最高能级的电子云轮廓图为____;基态Cu+的核外电子排布式为___。
(2) 的空间构型是________;HNO3的酸性比HNO2强,试从结构的角度解释其原因_______________。
的空间构型是________;HNO3的酸性比HNO2强,试从结构的角度解释其原因_______________。
(3)亚磷酸(H3PO3)是磷元素的一种含氧酸,与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3分子的结构式为____。
(4)Zn2+可与CN-、二苯硫腙(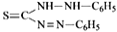 )等形成稳定配合物。
)等形成稳定配合物。
①CN- 的结构式为_____。
②每个二苯硫腙分子中,采取sp2杂化的原子有__个。
-
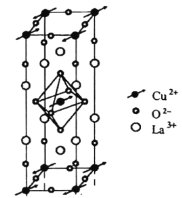
铜酸镧是一种反铁磁绝缘体,可由Cu(NO3)2和La(NO3)3为起始原料、水为溶剂、柠檬酸为络合剂,采用溶胶—凝胶法制备。
(1)Cu2+基态核外电子排布式为___。
(2)与NO 互为等电子体的阴离子为___。
互为等电子体的阴离子为___。
(3)柠檬酸(结构简式为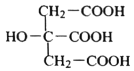 )分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。
)分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。
(4)铜酸镧的晶胞结构如图所示,写出其化学式:___。
-
(14分)铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途。
请回答下列有关问题:
⑴ 铜原子的基态电子排布式是▲ 。比较第一电离能Cu▲ Zn(填 “>”、“=”、“<”),说明理由▲ 。
⑵氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为▲ 。(每个球均表示1个原子)

⑶铜可以形成多种多样的配合物。
① NH3可以和很多过渡金属形成配合物。NH3分子中心原子的杂化类型为▲ 杂化,与NH3互为等电子体的粒子有▲ 。(只写其中一种)
②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。试用离子方程式表示其原因 ▲ 、 ▲ 。
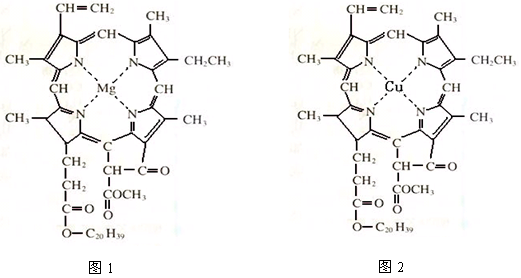
⑷在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键。
-
CuSO4溶液是一种较重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究。
i. 下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。

①该原电池的正极为 ____ ,其外电路中的电子是从____ 极(填“Zn”或“Cu”)流出。
②电解质溶液乙是______溶液,Zn极的电极反应式是_______ 。
③如果盐桥中的成分是K2SO4溶液,则盐桥中向左侧烧杯中移动的离子主要是_____。
ii. 下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。
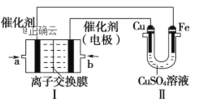
①同学想在Ⅱ中实现铁上镀铜,则Cu作____极,电极反应式为______,当线路中有0.1mol电子通过时,阴极增重_____ g。Ⅰ中消耗氧气体积是_____L(标况下)。
②a处通入的是____(填“CH4”或“O2”),b处电极上发生的电极反应式是___。Ⅰ中的总反应方程式为___。
③该同学若将Ⅱ中的两个电极都换成铂电极,当线路中有0.1mol电子通过时,测得溶液pH=______(100mL的CuSO4溶液),则Ⅱ中的总反应方程式为 _______ 。
-
【化学—选修3:物质结构与性质】CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3)向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,
[Cu(OH)4] 2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。

(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0pm,密度为________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为______________pm(列式表示)。
-
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
(1)写出基态原子或离子的电子排布式:
Fe3+_________________;Cu _______________。
(2)比较 Fe2+与Fe3+的化学稳定性:Fe2+________Fe3+;半径大小:Fe2+________Fe3+(均填“>”或“<”)。
Ⅱ.(1)在第三周期中,第一电离能最小的元素是______,电负性最大的元素是_______(用元素符号表示)。
(2)第三周期原子中p轨道半充满的元素是_______________(用元素符号表示)。
(3)第二周期原子中,未成对电子数等于其周期序数的原子有________(用元素符号表示)。
Ⅲ.酞菁与酞菁铜染料分子结构如下图:酞菁分子中氮原子采用的杂化方式有:________,并在下图相应位置上标出酞菁铜结构中铜原子周围的配位键:
-
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
⑴写出基态原子或离子的电子排布式:
①Fe3+_________________; ②Cr _______________; ③Cu _______________.
⑵比较 Fe2+与Fe3+的化学稳定性:Fe2+________Fe3+,半径大小:Fe2+________Fe3+
Ⅱ⑴在第三周期中,第一电离能最小的元素是________,电负性最大的元素是________(用元素符号表示)。
⑵第二、三、周期原子中p轨道半充满的元素是_______________(用元素符号表示)。
⑶第二周期原子中,未成对电子数等于周期系数的原子有________(用元素符号表示)
Ⅲ. (2010·滁州模拟)ClO、ClO、ClO中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构。
-
金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)①铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是___ (填字母)。
A. 电子从基态跃迁到较高的激发态 B. 电子从较高的激发态跃迁到基态
C. 焰色反应的光谱属于吸收光谱 D. 焰色反应的光谱属于发射光谱
②碘、铜两种元素的电负性如表:
CuI属于_______(填“共价”或“离子”)化合物。
(2)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
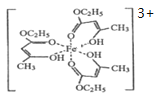
①此配合物中,基态铁离子的价电子排布图为________________。
②此配合物中碳原子的杂化轨道类型有________________。
③此配离子中含有的化学键有____________(填字母)。
A.σ键 B.π键 C.极性键 D.非极性键 E. 配位键 F. 氢键 G.离子键
(3)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_____________。
(4)治疗铅中毒可滴注依地酸(别名EDTA,结构如下面左图)钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_________(填标号)
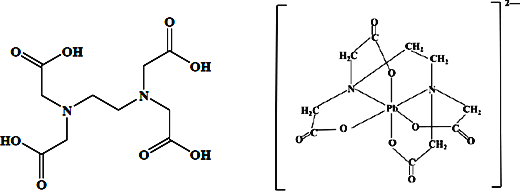
A.形成依地酸铅离子所需n(Pb2+):n(EDTA)=1:4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
(5)AlCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态还是气态,一个分子中的氯原子与另外一个铝原子形成配位键,因此以二聚体Al2Cl6的形式存在,写出Al2Cl6的结构式_______(用→标出配位键)。
-
铜是第四周期重要的过渡元素之一,其单质及化合物具有广泛用途.
请回答下列有关问题:
(1)铜原子的基态电子排布式是______.比较第一电离能Cu______Zn(填“>”、“=”、“<”),说明理由______.
(2)氮和铜形成某种化合物的晶胞结构如图所示,则其化学式为______.(每个球均表示1个原子)
(3)铜可以形成多种多样的配合物.
①NH3可以和很多过渡金属形成配合物.NH3分子中心原子的杂化类型为______杂化,与NH3互为等电子体的粒子有______.(只写其中一种)
②向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.试用离子方程式表示其原因______、______.
(4)在绿色植物标本的制作过程中,将植物材料洗净后浸入5%的硫酸铜溶液中,叶绿素(如图1)中心离子Mg2+被置换成Cu2+(如图2),叶片则永保绿色,请在图2中用箭头表示出配位键.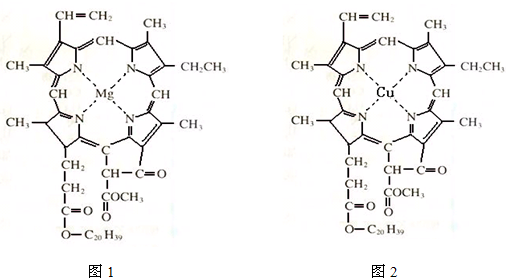

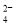 的立体构型是____,与SO
的立体构型是____,与SO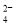 互为等电子体的一种分子为_______(填化学式)。
互为等电子体的一种分子为_______(填化学式)。
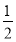 ,
,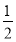 ,
,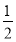 )。则D的坐标参数为________,它代表________原子。
)。则D的坐标参数为________,它代表________原子。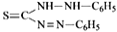 )等形成稳定配合物。
)等形成稳定配合物。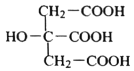 )分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。
)分子中碳原子的轨道杂化类型为___;1mol柠檬酸分子含σ键数目为___mol。







