-
某化学小组欲探究NO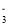 的氧化性及其还原产物。
的氧化性及其还原产物。
(1)提出问题
甲同学认为只有溶液中同时存在H+时,NO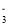 才有氧化性;
才有氧化性;
乙同学不赞成甲同学观点,他认为NO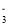 自身就具有氧化性,依据是__________
自身就具有氧化性,依据是__________
(2)实验探究:小组同学为解决上述争论,设计并进行了以下实验
| 实验I | 实验II | 实验III |
| 操作 | 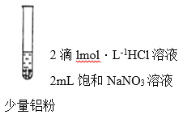
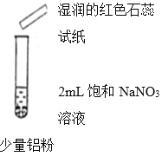
| 
| 
|
| 现象 | 微热,产生无色气泡,至液面上方变为浅红棕色。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 | 微热,产生无色气泡,湿润的红色石蕊试纸变蓝。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 | 微热,产生无色气泡,湿润的红色石蕊试纸变蓝。用拇指堵住试管口片刻,靠近酒精灯火焰,没有爆鸣声。 |
①实验I中反应的离子方程式为_________。
②实验II滴加两滴蒸馏水的目的是__________,产生的无色气泡为___________
③实验III反应后静置,取上层清液,滴加稀盐酸,先产生白色浑浊,后又消失。则实验III中反应的离子方程式为__________。
(3)实验结论:由实验I、II、III可得出的结论是________。
-
某小组同学探究浓硫酸及其部分反应产物的化学性质,装置如下图所示(夹持装置略去)
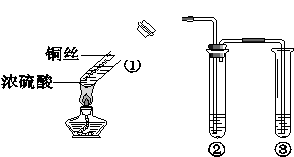
(1)试管①中反应的化学方程式是 。该反应表明浓硫酸具有 (填序号)。
a.酸性 b.强氧化性 c.还原性
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是 ,说明试管①中生成的气体具有 性。
(3)若试管②中的试剂为酸化的Ba(NO3)2溶液,观察到生成不溶于硝酸的白色沉淀,说明试管①中生成的气体具有 性。
(4)试管③中的试剂为NaOH溶液,反应的离子方程式是 。
-
已知,在木炭还原氧化铜的实验中发生的主要反应是C+2CuO 2Cu+CO2↑。某化学实验小组对该实
2Cu+CO2↑。某化学实验小组对该实
验产物(假设已完全反应)进行了如下探究:
探究一:检验产物的成分
【提出问题】实验产物是暗红色固体,很难观察到紫红色固体,那么该暗红色固体物质是什么?
【查阅资料】氧化亚铜(Cu2O)为红色固体,可以和硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O。
【猜想假设】暗红色固体除铜外还可能含有Cu2O。
【设计实验】取少量暗红色固体,加入稀硫酸,如果观察到_______________,说明猜想正确。
探究二:测定产物中Cu2O的含量
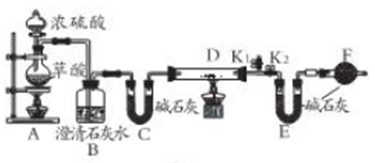
【查阅资料】草酸在浓硫酸的作用下会分解为CO和CO2
【设计实验】称取固体样品6.0g,置于上右图装置D中进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置E的质量达到实验目的。
(1)证明草酸的分解产物中有CO2存在的是_______________。
(2)装置C的作用是__________________。
(3)写出装置D中反应的化学方程式___________________________。
(4)下列为加热装置前所涉及的部分操作,正确的顺序是_________(填序号)。
①检查装置的气密性 ②关闭K2,打开K1,使装置A中的反应先进行一段时间
③连接仪器 ④关闭K1,打开K2
(5)若装置E在反应前后的质量分别为30.1g和31.2g,则该固体样品中Cu2O的质量分数为__________。
指出该装置的不足之处,说明不足的理由并绐出改进方案__________________。
-
某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是 ___________。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | 
| Zn+Fe2+=Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | | Fe+2Fe3+=3 Fe2+ | Fe3+具有氧化性 |
| ④ | | 
| | Fe3+具有氧化性 |
实验结论:_________________________________。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:_____。(填序号)
A、Cl2 B、Na C、Na+ D、Cl- E、SO2 F、盐酸
-
该研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略).已知:Cl2易溶于CCl4而HCl不溶于CCl4
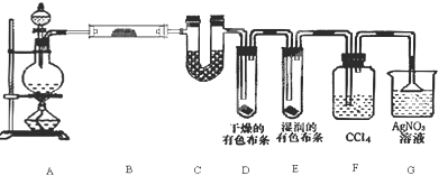
按要求回答问题:
(1)写出装置A制取Cl2的化学方程式_____。
(2)装置B中的试剂是__,现象是________。
(3)装置D和E中出现的不同现象说明的问题是____。
(4)装置F的作用是____。
(5)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在F和D之间再连接一个洗气瓶装置,则装置中应放入_____(填写试剂或用品名称),改正后证明有HCl挥发出来的现象是_______。
-
某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)请帮他们完成以下实验报告:
实验目的:_______________________。
试剂:铁粉、FeCl3溶液、FeCl2溶液、KSCN溶液、氯水、锌片。
实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| Ⅰ | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | ________ | Fe2+具有还原性 |
| Ⅱ | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+=Zn2++Fe | ________ |
| Ⅲ | 在FeCl3溶液中加入足量铁粉 | __________ | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
(2)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:____(填序号)。
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.H2O2
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时可以在溶液中加入____以防止亚铁盐被氧化。
(4)检验亚铁盐溶液是否被氧化的操作步骤和现象是___________________________。
(5)向FeCl2溶液滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________,此过程中发生的氧化还原反应的化学方程式__________________________。
-
某校化学实验兴趣小组为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学根据下列仪器设计实验装置证明上述结论。请按要求回答问题。

(1)U形接管中所盛试剂的化学式为_______________。
(2)检验产物中HCl 的离子方程式:____________________。
(3)乙同学认为甲同学的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在________________之间(填装置序号)瓶中可以放入_________________。
-
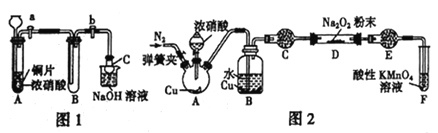
某研究性学习小组学生根据氧化还原反应规律,探究NO2、NO与Na2O2反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析Na2O2和NO2都既有氧化性又有还原性,于是提出如下假设:
假设1:Na2O2氧化NO2;
假设2:NO2氧化Na2O2。
(1)甲同学设计如图1装置进行实验:
①试管A中反应的离子方程式是_________________________________________。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B;向其中加入适量Na2O2粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
③仪器C兼有防倒吸的作用,仪器C的名称为___________________。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是________________________。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设1正确,则NO2和Na2O2反应的化学方程式是_______________________。
Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与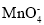 反应生成
反应生成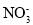 和Mn2+。
和Mn2+。
(3)丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________________。
②B中不能观察到的现象是____________(填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色b.有红棕色气泡产生c.有无色气泡产生
③C、E中所盛装的试剂不能是________(填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④F中发生反应的氧化剂与还原剂的物质的量之比为_____________。
⑤充分反应后,检验D装置中产物的方法是:______________,则产物是NaNO2。
-
某化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
(1) 实验目的:探究铁及其化合物的氧化性和还原性
(2) 实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是____________。
| 序号 | 实验设计 | 实验观察 (主要现象) | 离子方程式 | 解释与 结论 |
| ① | 在铁粉中滴入稀硫酸 | 铁粉溶解,溶液由无色变成浅绿色,生成无色无味气体 | Fe +2H+= H2↑+ Fe2+ | Fe具有还原性 |
| ② | FeCl2溶液中滴入KSCN溶液,再加氯水 | 滴入KSCN溶液无明显变化,加入氯水立即成血红色 | ____________ | ____________ |
| ③ | FeCl2溶液加入锌片 | | Fe2++ Zn = Fe+Zn 2+ | ____________ |
| ④ | ____________ | ____________ | 2Fe3++Cu=2Fe2++Cu2+ | Fe3+具有氧化性 |
(3) 实验记录(在仿照①实验作答,划线部分不必填写)。
(4) 学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是____________。
A. Cl2 B. Na C. Mg2+ D. H2O2
(5) 在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因:____________;
你将对实验员在配制氯化亚铁溶液时,提出的建议是____________。
(6)在配制氯化铁溶液时,含有少量Fe2+,为检验少量Fe2+的存在,请从下列物质中选择合适的试剂____________。
A. KSCN溶液 B. 稀盐酸
C. KMnO4 溶液 D. NaOH溶液
-
某化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是________。
| 序号 | 实验设计 | 实验观察(主要现象) | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴 入稀硫酸 | 铁粉溶解,溶液由无 色变成浅绿色,有无 色无味的的气体生成 | Fe +2H+= H2↑+ Fe2+ | Fe具有还原性 |
| ② | 氯化亚铁溶液中滴入KSCN溶液,再加入氯水 | 滴入KSCN溶液无明 显变化,加入氯水立 即变成血红色 | | |
| ③ | 氯化亚铁溶液加 入锌片 | | Fe2++ Zn = Fe + Zn 2++ | |
| ④ | | | | Fe3+具有氧化性 |
(3)实验记录(在仿照①实验作答,划线部分不必填写)
(4)学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是
A、Cl2 B、Na C、Mg2+ D、H2O2
(5)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因:________;
你将对实验员在配制氯化亚铁溶液时,提出的建议是________ 。
(6)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,为帮助实验员进行检验少量Fe2+的存在,请从下列物质中选择合适的试剂( )
A、KSCN溶液 B、稀盐酸 C、KMnO4 溶液 D、NaOH溶液
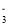 的氧化性及其还原产物。
的氧化性及其还原产物。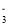 才有氧化性;
才有氧化性;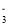 自身就具有氧化性,依据是__________
自身就具有氧化性,依据是__________







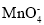 反应生成
反应生成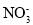 和Mn2+。
和Mn2+。