-
已知,在木炭还原氧化铜的实验中发生的主要反应是C+2CuO 2Cu+CO2↑。某化学实验小组对该实
2Cu+CO2↑。某化学实验小组对该实
验产物(假设已完全反应)进行了如下探究:
探究一:检验产物的成分
【提出问题】实验产物是暗红色固体,很难观察到紫红色固体,那么该暗红色固体物质是什么?
【查阅资料】氧化亚铜(Cu2O)为红色固体,可以和硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O。
【猜想假设】暗红色固体除铜外还可能含有Cu2O。
【设计实验】取少量暗红色固体,加入稀硫酸,如果观察到_______________,说明猜想正确。
探究二:测定产物中Cu2O的含量
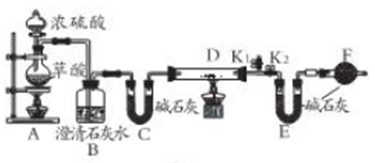
【查阅资料】草酸在浓硫酸的作用下会分解为CO和CO2
【设计实验】称取固体样品6.0g,置于上右图装置D中进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置E的质量达到实验目的。
(1)证明草酸的分解产物中有CO2存在的是_______________。
(2)装置C的作用是__________________。
(3)写出装置D中反应的化学方程式___________________________。
(4)下列为加热装置前所涉及的部分操作,正确的顺序是_________(填序号)。
①检查装置的气密性 ②关闭K2,打开K1,使装置A中的反应先进行一段时间
③连接仪器 ④关闭K1,打开K2
(5)若装置E在反应前后的质量分别为30.1g和31.2g,则该固体样品中Cu2O的质量分数为__________。
指出该装置的不足之处,说明不足的理由并绐出改进方案__________________。
-
古代炼铜,主要矿物原料是孔雀石 [Cu2(OH)2CO3],燃料是木炭,涉及的反应有:
①Cu2(OH)2CO3  2CuO+CO2↑+H2O ②2CuO+C
2CuO+CO2↑+H2O ②2CuO+C  2Cu+CO2↑
2Cu+CO2↑
③CuO+CO  Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C  2CO
2CO
(1)从四种基本反应类型看:反应①、②、④分别属于:______、________、____________ 。
(2)在上述反应中,属于氧化还原反应的是 __________________(填序号)。其中这几个反应的氧化剂分别是:____________、___________、______________。
-
已知酸性条件下有如下反应: 2Cu+=Cu2++Cu↓。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:
| 加入试剂 | 稀硫酸 | 浓硫酸、加热 | 稀硝酸 | 浓硝酸 |
| 实验现象 | 有红色固体剩余和溶液变为蓝色 | 产生无色气体 | 产生无色气体和溶液变为蓝色 | 产生红棕色气体和溶液变为绿色 |
由此推出本次氢气还原氧化铜实验的产物是
A. Cu B. Cu2O C. 一定有Cu,可能有Cu2O D. 一定有Cu2O,可能有Cu
-
下列反应属于氧化还原反应的是
A. CaCO3  CaO + CO2↑ B. Na2CO3 + 2HCl
CaO + CO2↑ B. Na2CO3 + 2HCl  2NaCl + CO2↑+ H2O
2NaCl + CO2↑+ H2O
C. 2Cu + O2  2CuO D. Fe2O3 + 3H2SO4
2CuO D. Fe2O3 + 3H2SO4  Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + 3H2O
-
下列反应属于氧化还原反应的是
A. CaCO3  CaO + CO2↑ B. Na2CO3 + 2HCl
CaO + CO2↑ B. Na2CO3 + 2HCl  2NaCl + CO2↑+ H2O
2NaCl + CO2↑+ H2O
C. 2Cu + O2  2CuO D. Fe2O3 + 3H2SO4
2CuO D. Fe2O3 + 3H2SO4  Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + 3H2O
-
下列反应属于氧化还原反应的是
A. CaCO3  CaO + CO2↑ B. Na2CO3 + 2HCl
CaO + CO2↑ B. Na2CO3 + 2HCl  2NaCl + CO2↑+ H2O
2NaCl + CO2↑+ H2O
C. 2Cu + O2  2CuO D. Fe2O3 + 3H2SO4
2CuO D. Fe2O3 + 3H2SO4  Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + 3H2O
-
某实验小组设计了如下装置对焦炭还原二氧化硅气体产物的成分进行探究。
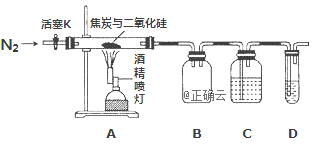
已知:PdCl2溶液可用于检验CO,反应的化学方程式为: CO+PdCl2 + H2O = CO2 +2HCl + Pd↓(产生黑色金属钯粉末,使溶液变浑浊)。
(1)实验时要通入足够长时间的N2,其原因是________
(2)装置B的作用是________
(3)装置C中所盛试剂应为___________
(4)该装置的缺点是________
-
某实验小组设计了如下装置对焦炭还原二氧化硅的气体产物的成分进行探究。
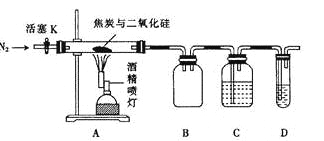
已知:PdCl2溶液可用于检验CO,反应的化学方程式为CO + PdCl2 + H2O = CO2 + 2HCl + Pd↓
(产生黑色金属钯粉末,使溶液变浑浊)。
(1)实验时要通入足够长时间的N2,其原因是_ 。
(2)装置B的作用是_ 。
(3)装置C、D中所盛试剂分别为_ ___ 、_ ___,若装置C、D中溶液均变浑浊,且经检测两气体产物的物质的量相等,则该反应的化学方程式为_ 。
(4)该装置的缺点是_ 。
(5)资料表明,上述反应在焦炭过量时会生成副产物SiC。取18 g SiO2和8.4 g焦炭充分反应后收集到标准状况下的气体13.44 L,假定气体产物只有CO,固体产物只有Si和SiC,则Si和SiC的物质的量之比为_ 。
(6)设计实验证明碳酸的酸性比硅酸的强:_ 。
-
某实验小组设计了如下装置对焦炭还原二氧化硅的气体产物的成分进行探究。已知: PdCl2溶液可用于检验CO,反应的化学方程式为CO + PdCl2 + H2O= CO2+ 2HCl + Pd(产生黑色金属钯粉末,使溶液变浑浊)。
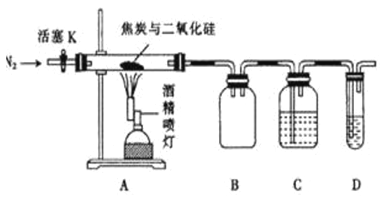
(1)实验时要先通入足够长时间的N2,其原因是_________。
(2) 装置B的作用是__________。
(3)装置C、D所盛试剂分别为______、______,若装置C、D中溶液均变浑浊,且经检测两气体产物的物质的量相等,则该反应的总化学方程式为_________。
(4) 该装置的缺点是_________。
-
下列反应属于氧化还原反应,但不属于四种基本类型反应的是( )
A.H2SO4+2NaOH=Na2SO4+2H2O B.CuO+H2 Cu+H2O
Cu+H2O
C.Cu2(OH)2CO3 =2CuO+ CO2↑+H2O D.3CO+Fe2O3 3CO2+2Fe
3CO2+2Fe
2Cu+CO2↑。某化学实验小组对该实



