-
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g) △H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器中进行以上的反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g) △H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器中进行以上的反应(此条件下为可逆反应),下列叙述正确的是
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C. 反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min
D. 当反应吸热为0.025QkJ时,生成的HCl与100mL1mol·L-1的NaOH溶液恰好反应
-
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g);△H=+QkJ•mol-1 (Q>0)某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
Si(s)+4HCl(g);△H=+QkJ•mol-1 (Q>0)某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强则化学反应速率降低
B.若反应开始时 SiCl4 为 1mol,则达到平衡时,吸收热量为 QkJ
C.反应至 4min 时,若HCl的浓度为 0.12mol•L-1,则 H2 的反应速率为 0.03mol/(L•min)
D.当反应吸收热量为 0.025QkJ 时,生成的 HCl 通入 100mL1mol•L-1 的 NaOH 恰好反应
-
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g) △H=+Q kJ/mol(Q>0),等温、恒压条件下,将一定量反应物通入密闭容器进行上述反应,下列叙述正确的是( )
Si(s)+4HCl(g) △H=+Q kJ/mol(Q>0),等温、恒压条件下,将一定量反应物通入密闭容器进行上述反应,下列叙述正确的是( )
A.反应过程中,若充入与反应无关的气体,由于保持压强不变,则反应速率不变
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C.当反应吸收热量为0.025Q kJ时,生成的HCl通入100mL1mol/L的NaOH溶液恰好完全反应
D.反应至4min时,若HCl浓度为0.12mol/L,则0~4min内H2的反应速率为0.03moL/(L∙min)
-
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g) ΔH=+Q kJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器中进行以上反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ
C.反应至4 min时若HCl浓度为0.12 mol·L-1,则H2反应速率为0.03 mol·L-1·min-1
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液中恰好反应
-
工业上制取纯硅的主要反应:SiCl4 + 2H2  Si + 4HCl。该反应中,被还原的物质是 (填化学式),作为还原剂的物质是 (填化学式);若反应中生成了1molSi,则转移电子 mol,消耗H2 mol。
Si + 4HCl。该反应中,被还原的物质是 (填化学式),作为还原剂的物质是 (填化学式);若反应中生成了1molSi,则转移电子 mol,消耗H2 mol。
-
工业上制备纯硅反应的化学方程式如下:SiCl4(g)+2H2(g) = Si(s)+4HCl(g),将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若通过缩小体积增大压强,则活化分子百分数变大,反应速率加快
B.若Si-Cl、H-H、Si-Si、H-Cl的键能分别为Ea、Eb、 Ec、Ed(单位:),则△H=(4Ea+2Eb-Ec-4Ed )KJ/mol
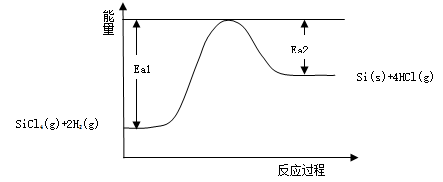
C.该反应能量变化如下图所示,则Ea1、Ea2分别代表该反应正向和逆向的活化能,使用催化剂Ea1、Ea2都减小,△H也变小
D.由下图和题目信息可知该反应△H>0,△S>0,所以在较高温度下可自发进行
-
制备单质硅的主要化学反应如下:①SiO2+2C Si + 2CO↑
Si + 2CO↑
②Si+2Cl2 SiCl4 ③SiCl4+2H2
SiCl4 ③SiCl4+2H2 Si + 4HCl
Si + 4HCl
下列对上述三个反应的叙述中不正确的是( )
A.①③为置换反应 B.①②③均为氧化还原反应
C.③中SiCl4是氧化剂 D. 三个反应的反应物中的硅元素均被还原
-
制备硅单质时,主要化学反应如下:
(1)SiO2 +2C Si +2CO↑
Si +2CO↑
(2) Si + 2Cl2 SiCl4 (3)SiCl4 + 2H2
SiCl4 (3)SiCl4 + 2H2 Si + 4HCl
Si + 4HCl
下列对上述三个反应的叙述中,不正确的是
A.(1)(3)为置换反应 B.三个反应的反应物中硅元素均被还原
C.(2)为化合反应 D.(1)(2)(3)均为氧化还原反应
-
反应SiCl4 + 2H2 =Si(纯) + 4HCl 可用于工业上制取纯硅。该反应属于
A.置换反应 B.复分解反应 C.化合反应 D.分解反应
-
制备硅单质时,主要化学反应如下:
①SiO2 + 2C Si + 2CO↑
Si + 2CO↑
② Si + 2Cl2 SiCl4
SiCl4
③SiCl4 + 2H2 Si + 4HCl
Si + 4HCl
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被还原
Si(s)+4HCl(g);△H=+QkJ•mol-1 (Q>0)某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
