-
反应SiCl4 + 2H2 =Si(纯) + 4HCl 可用于工业上制取纯硅。该反应属于
A.置换反应 B.复分解反应 C.化合反应 D.分解反应
高一化学选择题简单题查看答案及解析
-
工业上制取纯硅的主要反应:SiCl4 + 2H2
Si + 4HCl。该反应中,被还原的物质是 (填化学式),作为还原剂的物质是 (填化学式);若反应中生成了1molSi,则转移电子 mol,消耗H2 mol。
高一化学填空题中等难度题查看答案及解析
-
制备单质硅的主要化学反应如下:①SiO2+2C
Si + 2CO↑
②Si+2Cl2
SiCl4 ③SiCl4+2H2
Si + 4HCl
下列对上述三个反应的叙述中不正确的是( )
A.①③为置换反应 B.①②③均为氧化还原反应
C.③中SiCl4是氧化剂 D. 三个反应的反应物中的硅元素均被还原
高一化学选择题简单题查看答案及解析
-
制备硅单质时,主要化学反应如下:
①SiO2 + 2C
Si + 2CO↑
② Si + 2Cl2
SiCl4
③SiCl4 + 2H2
Si + 4HCl
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被还原
高一化学选择题中等难度题查看答案及解析
-
制备硅单质时,主要化学反应如下:
①SiO2 + 2C
Si + 2CO↑
② Si + 2Cl2
SiCl4
③SiCl4 + 2H2
Si + 4HCl
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被还原
高一化学选择题中等难度题查看答案及解析
-
制备硅单质时,主要化学反应如下:
①SiO2+2C
Si+2CO↑ ②Si+2Cl2
SiCl4 ③SiCl4+2H2
Si+4HCl
下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.②为化合反应
D.三个反应的反应物中硅元素均被还原
高一化学单选题简单题查看答案及解析
-
从石英砂制取并获得高纯硅的主要化学反应如下:
①SiO2+2C
Si(粗)+2CO↑
②Si(粗)+2Cl2
SiCl4
③SiCl4+2H2
Si(纯)+4HCl
关于上述反应的分析不正确的是( )
A. ①、③是置换反应,②是化合反应
B. 任一反应中,每消耗或生成28 g硅,均转移4 mol电子
C. 高温下,焦炭与氢气的还原性均强于硅
D. 高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
高一化学单选题困难题查看答案及解析
-
在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4 SiCl4+2H2=Si(纯)+4HCl。若在25℃101KPa条件下反应生成HCl气体49L(注:25℃101KPa条件下气体摩尔体积为24.5L/mol)则:
(1)反应生成HCl气体的质量为__________,转移电子的个数为_____________。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为 。
(3)“从沙滩到用户”涉及到多个反应,其中制取粗硅的反应方程式为 ,纯净的石英砂与烧碱反应可以制得水玻璃,反应的离子方程式为 。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O 13%,CaO 11.7%,SiO2 75.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需要上述原料的质量是 t(保留两位小数)。
高一化学填空题困难题查看答案及解析
-
在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl。
若在25℃、101kPa条件下反应生成HCl气体49L,(注:25℃、101kPa条件下气体摩尔体积为24.5L•mol-1)则:
(1)反应生成HCl气体的质量为__,转移电子的总数为___。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g•mL-1的盐酸,此盐酸的物质的量浓度为___。
(3)“从沙滩到用户”涉及多个反应,其中制取粗硅的反应方程式为___。纯净的石英与烧碱反应可以制得水玻璃,反应的离子方程式为__。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O13%,CaO11.7%,SiO275.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需耍上述原料的质量是___t。(保留两位小数)
高一化学计算题中等难度题查看答案及解析
-
工业上制备纯硅反应的化学方程式如下:SiCl4(g)+2H2(g) = Si(s)+4HCl(g),将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若通过缩小体积增大压强,则活化分子百分数变大,反应速率加快
B.若Si-Cl、H-H、Si-Si、H-Cl的键能分别为Ea、Eb、 Ec、Ed(单位:),则△H=(4Ea+2Eb-Ec-4Ed )KJ/mol
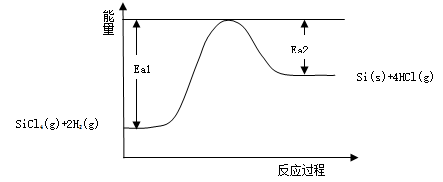
C.该反应能量变化如下图所示,则Ea1、Ea2分别代表该反应正向和逆向的活化能,使用催化剂Ea1、Ea2都减小,△H也变小
D.由下图和题目信息可知该反应△H>0,△S>0,所以在较高温度下可自发进行
高一化学选择题困难题查看答案及解析