-
下列化学方程式中,不能正确表示反应颜色变化的是
A.将盛有NO2的密封玻璃容器放入冷水中,颜色变浅:2NO2 N2O4
N2O4
B.用铝筷摩擦浸泡在NaCl溶液中变黑的银器(黑色物质为Ag2S),银器很快恢复银白色:Ag2S+2NaCl===Na2S+2AgCl
C.氯化亚铁溶液遇铁氰化钾溶液出现蓝色沉淀:3FeCl2+2K3[Fe(CN)6]===Fe3[Fe(CN)6]2↓+6KCl
D.FeCl3溶液中加入铜粉,溶液从黄色变为蓝绿色:2FeCl3+Cu===2FeCl2+CuCl2
-
下列化学方程式中,不能正确表示反应颜色变化的是
A.将盛有NO2的密封玻璃容器放入冷水中,颜色变浅:2NO2 N2O4
N2O4
B.用铝筷摩擦浸泡在NaCl溶液中变黑的银器(黑色物质为Ag2S),银器很快恢复银白色:Ag2S+2NaCl===Na2S+2AgCl
C.氯化亚铁溶液遇铁氰化钾溶液出现蓝色沉淀:3FeCl2+2K3[Fe(CN)6]===Fe3[Fe(CN)6]2↓+6KCl
D.FeCl3溶液中加入铜粉,溶液从黄色变为蓝绿色:2FeCl3+Cu===2FeCl2+CuCl2
-
已知2NO2(红棕色) N2O4(无色)可以同时相互转化,
N2O4(无色)可以同时相互转化,
①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个 热反应。
②在一个恒温恒压容器中,通入稀有气体。颜色 ,平衡 移动。
③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率 ,颜色 ,再通入稀有气体增大压强,平衡 移动,颜色 。
-
在80℃时,某物质在2L的容器中发生化学反应,隔一段时间对该容器内的物质进行分析,得到如表数据:

则下列说法正确的是
A.该反应的方程式为2NO2 N2O4
N2O4
B.80s前该反应一定没有达到平衡状态
C.a的取值为0.56
D.20s到40s内用N2O4表示的反应速率为0.010mol·L-1·S-1
-
下列反应方程式中,能正确表达反应颜色变化的是( )
A.280K时,在一干燥密闭容器中充入NO2和SO2,产生白烟:NO2+SO2═NO+SO3
B.水玻璃敞口放置产生白色浑浊:SiO32-+H2O═SiO2↓+2OH-
C.银器久置空气中表面变黑:4Ag+O2═2Ag2O
D.沸水中滴入FeCl3溶液,液体变为红褐色:Fe3++3OH-═Fe(OH)3↓
-
往恒容密闭容器中通入一定量N2O4,发生反应N2O4(g)  2NO2(g),随温度升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的 规律。X、Y分别是( )
2NO2(g),随温度升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的 规律。X、Y分别是( )

A.温度T,逆反应速率v B.温度T,气体的密度
C.压强P,平衡常数K D.压强P,N2O4转化率
-
往密闭容器中通入一定量N2O4,发生反应N2O4(g)  2NO2(g),随温度升高,气体颜色变深。下图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律。X、Y分别是
2NO2(g),随温度升高,气体颜色变深。下图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律。X、Y分别是

A.温度T,逆反应速率υ逆
B.温度T,气体的密度ρ
C.压强P,平衡常数K
D.压强P,N2O4转化率α
-
在恒温下的密闭容器中,有可逆反应:2NO2 N2O4,下列不能说明反应达到了平衡状态的是 ( )
N2O4,下列不能说明反应达到了平衡状态的是 ( )
A.N2O4生成速率与N2O4分解速率相等时
B.混合气体平均相对分子质量保持不变时
C.NO2的分子数与N2O4分子数比为2∶1时
D.体系颜色不再发生改变时
-
在一定温度下,容积固定的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)  2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
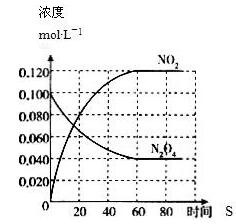
A. 若温度升高,混合气体的颜色变深
B. 在该温度下反应2NO2(g)  N2O4(g)的平衡常K为25/9
N2O4(g)的平衡常K为25/9
C. 反应达平衡后,将反应容器的容积减少一半,平衡向正反应方向移动
D. 反应达平衡后,向此容器中通入NO2气体,则c(NO2)增大
-
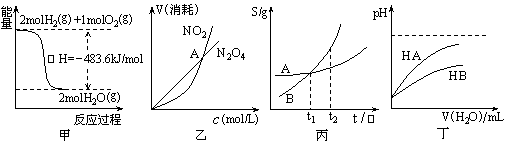
关于下列各图的叙述正确的是 ( )
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
N2O4