-
氨和水都是常用的试剂。请回答下列问题:
(1)氮元素在元素周期表中的位置是 ;基态氮原子的核外电子中,未成对电子数与成对电子数之比为____________。
(2)NH3分子可结合一个H+形成铵根离子(NH)。
①NH3分子中N原子的杂化类型是____________。
②NH3分子与H+结合的过程中未发生改变的是____________(填选项字母)。
A.微粒的空间结构 B.N原子的杂化类型 C.H—N—H的键角
(3)将氨气通入CuSO4溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。[Cu(H2O)6]2+(水合铜离子)和[Cu(NH3)4]2+中共同含有的化学键类型是 。生成蓝色沉淀的离子方程式是 。
【答案】(1)第2周期ⅤA族(2分);3∶4(2分)
(2)①sp3;②B(各1分,共2分)
(3)共价键和配位键(各1分,共2分);Cu2+ +2NH3·H2O =Cu(OH)2↓+2NH4+
(2分,其它合理表示也给分。)
【解析】
(1)氮元素为7号元素,在元素周期表中的位置是第2周期ⅤA族;根据基态氮原子的核外电子轨道表示式判断,未成对电子数与成对电子数之比为3:4。
(2)①NH3分子中N原子的杂化类型是sp3。② A.氨分子的空间构型为三角锥形,铵离子的空间构型为正四面体形,微粒的空间结构发生变化,错误;B、氨分子和铵离子中N原子的杂化方式均为sp3杂化,N原子的杂化类型不变,正确;C、氨分子中的键角107.3。,铵离子中的键角为109.5。,H—N—H的键角发生变化,错误,选B。
(3)[Cu(H2O)6]2+(水合铜离子)和[Cu(NH3)4]2+中Cu2+与H2O、NH3形成配位键,水分子内氢、氧原子间,氨分子中氮、氢原子间形成共价键;将适量氨气通入CuSO4溶液中,二者反应生成氢氧化铜沉淀和硫酸铵,离子方程式是Cu2+ +2NH3·H2O =Cu(OH)2↓+2NH4+。
考点:考查原子结构、分子结构和配合物。
【题型】填空题
【适用】较难
【标题】2015-2016学年四川省雅安市高二上学期期末考试化学试卷(带解析)
【关键字标签】
【结束】某学习小组研究“不同条件对化学反应速率影响的探究”,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液在稀硫酸中进行实验,改变条件如表:
组别
草酸的体积
/mL
温度/℃
其它物质
①
2 mL
20
②
2 mL
20
2滴饱和MnSO4溶液
③
2 mL
30
④
1 mL
20
1 mL蒸馏水
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用 ①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
高二化学实验题困难题查看答案及解析
-
氨和水都是常用的试剂。请回答下列问题:
(1)氮元素基态原子的核外电子中,未成对电子数与成对电子数之比为________________。
(2)NH3分子可结合一个H+形成铵根离子(NH4+)。
①NH3分子中N原子的杂化类型是___________。
②NH3分子中与H+结合的过程中未发生改变的是_____________(填选项字母)。
a.微粒的空间构型 b.N原子的杂化类型 C.H-N-H的键角
(3)将氨气通入CuSO4溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。该过程中微粒的变化是[Cu(H2O)4]2+→Cu(OH)2→[Cu(NH3)4]2+。[Cu(H2O)4]2+和[Cu(NH3)4]2+中共同含有的化学键类型有_________________。
(4)①水变成冰晶体时,密度减小的主要原因是___________。
②N2O4、H2O2分子中电负性最大的元素在周期表中的位置为_______________
(5)NO3-的空间构型是___________。
(6)已知:AlF63-在溶液中可稳定存在,CaF2难溶于水,但可溶于含Al3+的溶液中,原因是________ (用离子方程式表示)。
(7)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为_________,其中氧原子的杂化方式为________。
高二化学综合题中等难度题查看答案及解析
-
原子结构与元素周期表存在着内在联系,根据已学知识请你回答下列问题。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第_______周期______族。
(2)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_____________________________。
(3)写出3p轨道上只有2个未成对电子的元素的符号:________、________,二者电负性________>________。
高二化学综合题中等难度题查看答案及解析
-
原子结构与元素周期表存在着内在联系,根据已学知识请你回答下列问题。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第_______周期______族。
(2)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_____________________________。
(3)写出3p轨道上只有2个未成对电子的元素的符号:________、________,二者电负性________>________。
高二化学综合题中等难度题查看答案及解析
-
第四周期元素Q位于ds区,最外层电子半充满;短周期元素W、X、Y、Z第一电离能与原子序数的关系如图所示,请回答下列问题(用Q、W、X、Y、Z所对应的元素符号作答):
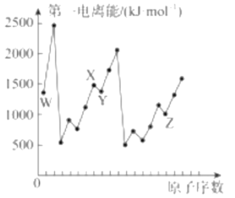
(1)X、W组成的一种二元化合物常用作火箭燃料,该化合物中X原子的杂化方式为___________。
(2)X2Y曾被用作麻醉剂,根据“等电子体原理”预测X2Y的空间构型为______________。
(3)Q与X形成的一种二元化合物的立方晶胞结构如图所示:
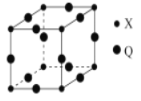
Q原子周围距其距离最近的Q原子的数目为_______(阿拉伯数字表示)。
(4)已知单质Q晶体的堆积方式为面心立方最密堆积,则单质Q晶体的晶胞中原子的空间利用率为_________________(用含π的式子表示)。
高二化学综合题中等难度题查看答案及解析
-
(1)根据原子结构、元素周期表和元素周期律的知识回答下列问题:
①X是1~36号元素原子核外电子排布中未成对电子数最多的元素,X元素的名称是___,在元素周期表中的位置是___,位于周期表___区。。
②C、N、O、F四种元素第一电离能由大到小的顺序为___。
(2)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
①基态铜原子的电子排布式为___。
②CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是___;Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___个铜原子。
高二化学综合题中等难度题查看答案及解析
-
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是____,在元素周期表中的位置是____________________。
(2)C元素基态原子的电子排布图是下图中的_______(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合_______(从A B C中选择)。
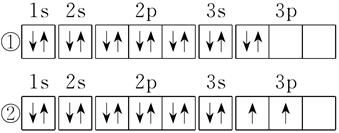
A.能量最低原理 B.泡利原理 C.洪特规则
(3)依据正负化合价代数和等于0,H元素可以放在周期表中的________族
(4)氯化铵的电子式________
高二化学填空题中等难度题查看答案及解析
-
下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置。试回答下列问题:
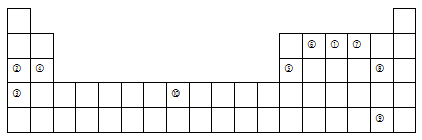
(1)写出表中⑥含有8个中子的原子的化学符号 ,元素⑦的氢化物与⑧的单质反应的离子方程式为 。
(2)元素⑩的核外电子排布式 。
(3) 根据元素周期表来比较④和Cs的金属性,要通过另一种元素作中介或桥梁进行比较, 这种元素是 (填元素符号)。
(4)据报道,美国科学家卡尔·克里斯特于1998年11月根据①合成了一种名为“N5”的物质,由于其极强的爆炸性,又称“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片的电子式为:__________________。
高二化学填空题简单题查看答案及解析
-
(6分)四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
X
Y
Z
W
请回答下列问题:
(1)元素Z位于周期表中第______________周期,___________族;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________(写化学式);
(3)XW2的电子式为_______________;
(4)Y的最高价氧化物的化学式为________________;
(5)W和Y形成的一种二元化合物具有色温效应,请相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________。
高二化学推断题简单题查看答案及解析
-
下表为周期表的一部分,其中的编号代表对应位置的元素。
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
请回答下列问题:
(1)写出上表中元素⑨原子的核外电子排布式________。
(2)元素④、⑤的第一电离能大小顺序是:________>________ ;(用元素符号表示,下同)元素⑥、⑧电负性大小顺序是:________>________
(3)元素③、⑧形成的化合物中心原子杂化轨道类型:________,分子的空间构型________
(4)已知某些不同族元素的性质也有一定的相似性,如元素②与元素⑦的氢
氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的化学方程式________
(5)下图是⑩的某种氧化物的晶胞结构示意图(顶角和体心是氧),可确定该氧化物的化学式为________。
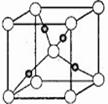
(6)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。
已知NF3与NH3的结构类似,但NF3 不易与Cu2+形成配离子,其主要原因是:________
高二化学填空题简单题查看答案及解析