-
对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
主反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g)
副反应:CO2(g)+H2(g)=CO(g)+H2O(g)
(1)工业上提高甲烷反应选择性的关键因素是____________。
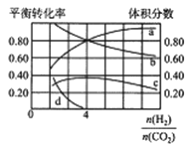
(2)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H2转化率的是____________,c、d分别表示CH4(g)和CO(g)的体积分数,由图可知 =____________时,甲烷产率最高。
=____________时,甲烷产率最高。
Ⅱ.CO2加氢合成低碳烯烃的技术在节能减排等方面具有重要意义,由CO2和H2合成CH3OH的反应如下:CO(g)+3H2(g)=CH3OH(g)+H2O(g) △H,在10L的恒容密闭容器中投入1molCO2和2.75molH2,在不同条件下发生上述反应,测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
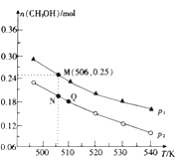
(3)判断P1____________P2 (填“大于”、“小于”或“等于”)
说明理由_____________________________________。
(4)经测定Q点时容器的压强是反应前压强的9/10,若反应从开始到平衡所需的时间为5min,则0〜5min内H2的反应速率v(H2)=____________。
-
对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
主反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1①
副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
已知H2和CH4的燃烧热分别为-285.5kJ·mol-1和-890.0kJ·mol-1
H2O(l)=H2O(g) △H=+44 kJ·mol-1
(1)△H1=______kJ·mo l-1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)_________。工业上提高甲烷反应选择性的关键因素是_____________。
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H2转化率的是______,c、d分别表示CH4(g)和CO(g)的体积分数,由图可知 =______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。
=______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。
II.溶于海水的CO295%以HCO3-形式存在。在海洋中,通过如下左图钙化作用实现碳自净。
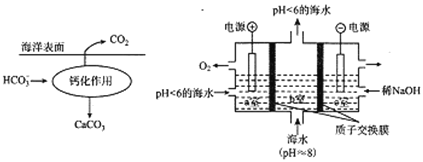
(4)写出写出钙化作用的离子方程式____________。
(5)电解完成后,a室的pH值______(“变大”、“变小”或“几乎不变”);其间b室发生反应的离子方程式为____________。
-
对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:主反应:CO2(g)+4H2(g)  CH4(g)+2H2O(g) △H1①副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol ,己知 H2和CH4 的燃烧热分别为-285.5kJ•mol-1和-890.0kJ•mol-1,H2O(l)= H2O(g) △H=+44 kJ•mol-1
CH4(g)+2H2O(g) △H1①副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol ,己知 H2和CH4 的燃烧热分别为-285.5kJ•mol-1和-890.0kJ•mol-1,H2O(l)= H2O(g) △H=+44 kJ•mol-1
(1)△H3=_____kJ • mol-1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)__________。工业上提高甲烷反应选择性的关键因素是___________。
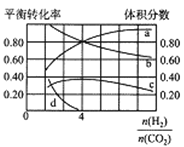
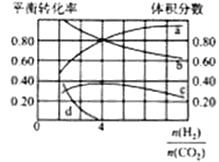
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2 和CO2以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H2转化率是_______,c、d分别表示CH4(g)和CO(g)的休积分数,由图可知n(H2)/ n(CO2)=_____时,甲烷产率最高。若该条件CO的产率趋于0,则T℃时①的平衡常数K=______。
II.溶于海水的CO2 95%以HCO3-形式存在。在海洋中,通过如下左图钙化作用实现碳自净。
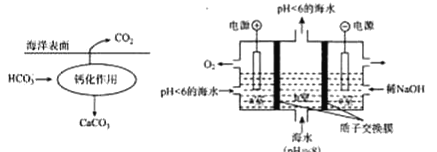
(4)写出写出钙化作用的离子方程式_________________________。
(5)电解完成后,a室的pH值_____(“变大”、“变小”或“几乎不变”);其间b室发生反应的离子方程式为________。
-
对温室气体二氧化碳的研究一直是科技界关注的重点。
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
主反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1①
副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
已知H2和CH4的燃烧热分别为-285.5kJ·mol-1和-890.0kJ·mol-1
H2O(l)=H2O(g) △H=+44 kJ·mol-1
(1)△H1=______kJ·mo l-1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)_________。工业上提高甲烷反应选择性的关键因素是_____________。
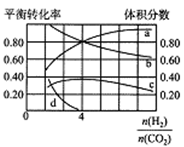
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。若a、b表示反应物的转化率,则表示H2转化率的是______,c、d分别表示CH4(g)和CO(g)的体积分数,由图可知 =______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。
=______时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=________。
II.溶于海水的CO295%以HCO3-形式存在。在海洋中,通过如下左图钙化作用实现碳自净。
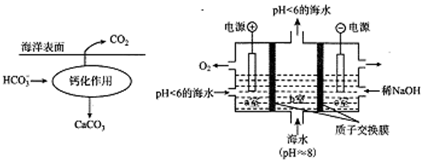
(4)写出写出钙化作用的离子方程式____________。
(5)电解完成后,a室的pH值______(“变大”、“变小”或“几乎不变”);其间b室发生反应的离子方程式为____________。
-
对温室气体二氧化碳的研究一直是科技界关注的重点。
Ⅰ.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如下:
主反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH1①
副反应:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
已知:H2和CH4的燃烧热分别为285.5 kJ·mol-1和890.0 kJ·mol-1,H2O(l)===H2O(g) ΔH=+44 kJ·mol-1。
(1)ΔH1=________ kJ·mol-1。
(2)有利于提高CH4产率的反应条件是(至少写两条)______________________________工业上提高甲烷反应选择性的关键因素是________________________________。
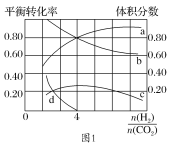
(3)T℃时,若在体积恒为2 L的密闭容器中同时发生上述反应,将物质的量之和为5 mol的H2和CO2以不同的投料比进行反应,结果如图1所示。若a、b表示反应物的平衡转化率,则表示H2平衡转化率的是________,c、d分别表示CH4(g)和CO(g)的体积分数,由图1可知 =________时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=___________________。
=________时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=___________________。
Ⅱ.溶于海水的CO2 95%以HCO3-形式存在。
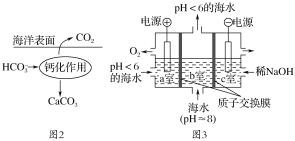
在海洋中,通过图2钙化作用实现碳自净。
(4)写出钙化作用的离子方程式________________。
(5)电解完成后,a室的pH________(填“变大”、“变小”或“几乎不变”);b室发生反应的离子方程式为________________________。
-
减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。合理应用和处理碳、氮及其化合物,在生产生活中有重要意义。
(1)对温室气体二氧化碳的研究一直是科技界关注的重点。在催化剂存在下用H2还原CO2 是解决溫室效应的重要手段之一,相关反应如下:
已知H2 和CH4的燃烧热分别为285.5kJ/mol 和890.0kJ/mol。
H2O(1) =H2O(g) △H= +44 kJ/mol
试写出H2 还原CO2 生成CH4和H2O(g)的热化学方程式_____________。
(2)CO2在Cu-ZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
II.CO2(g) +H2(g) CO(g) + H2O(g) △H2 = +41.2 kJ/mol
CO(g) + H2O(g) △H2 = +41.2 kJ/mol
①某温度时,若反应I的速度v1大于反应II的速度以v2,则下列反应过程的能量变化正确的是_______(填选项)。
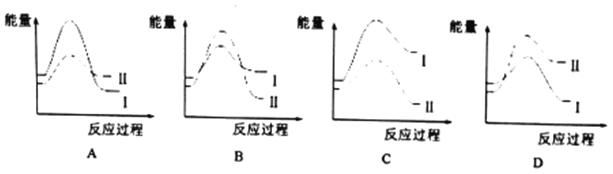
②对于气体参加的反应,,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体物质的量浓度c(B)。
已知:气体各组分的分压p(B),等于总压乘以其体积分数。
在Cu-ZnO存在的条件下,保持温度T时,在容积不变的密闭容器中,充入一定量的CO2 及H2,起始及达平衡时,容器内各气体物质的量如下表:
| CO2 | H2 | CH3OH | CO | H2O(g) | 总压/kPa |
| 起始/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
| 平衡/mol | | | n1 | | n2 | p |
若反应I、II均达平衡时,P0=1.2p,则表中n1=____;若此时n2=3.则反应I的平衡常数Kp=__(无需带单位,用含总压p的式子表示)。
(3)汽车尾气是雾霾形成的原因之一。研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:
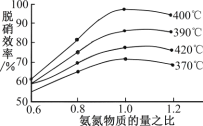
4NO(g) +4NH3(g) +O2(g)  4N2(g) +6H2O(g) △H <0
4N2(g) +6H2O(g) △H <0
根据下图判断提高脱硝效率的最佳条件是________;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是______________。
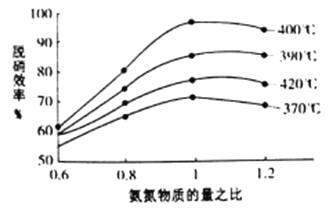
(4)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s) +2NO(g) N2(g) +CO2(g) △H>0
N2(g) +CO2(g) △H>0
在T℃时,反应进行到不同时间测得各物质的量浓度如下:
| 时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_______。
A.通入一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的NO E.加入一定量的活性炭 F.适当升高温度
-
减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。合理应用和处理碳、氮及其化合物,在生产生活中有重要意义。
(1)对温室气体 CO2 的研究一直是科技界关注的重点。在催化剂存在下用 H2 还原 CO2 是解决溫室效应的重要手段之一。
已知:①H2 和 CH4 的燃烧热分别为 285.5 kJ/mol 和 890.0 kJ/mol。
②H2O(1)===H2O(g) ΔH=+44 kJ/mol
试写出H2还原CO2生成CH4和H2O(g)的热化学方程式_____。
(2)CO2在Cu−ZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1=-57.8kJ/mol
CH3OH(g)+H2O(g)ΔH1=-57.8kJ/mol
II.CO2(g)+H2(g) CO(g)+H2O(g)ΔH2=+41.2kJ/mol
CO(g)+H2O(g)ΔH2=+41.2kJ/mol
对于气体参加的反应,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),则反应II的Kp=_____[已知:气体各组分的分压p(B),等于总压乘以其体积分数]。
在Cu−ZnO存在的条件下,保持温度T不变,在一刚性密闭容器中,充入一定量的CO2及H2,起始及达平衡时,容器内各气体物质的量如下表:
| CO2 | H2 | CH3OH | CO | H2O(g) | 总压/kPa |
| 起始/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
| 平衡/mol | | | n1 | | n2 | p |
若反应I、II均达平衡时,p0=1.2p,则表中n1=_____;若此时n2=3.则反应I的平衡常数Kp=_____(无需带单位,用含总压p的式子表示)。
(3)汽车尾气是雾霾形成的原因之一,研究氮氧化物的处理方法可有效减少雾霾的形成。可采用氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g)ΔH<0
4N2(g)+6H2O(g)ΔH<0
(4)根据图示判断提高脱硝效率的最佳条件是_____;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是_____。用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s)+2NO(g) N2(g)+CO2(g)ΔH>0在T℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)ΔH>0在T℃时,反应进行到不同时间测得各物质的量浓度如下:
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(NO)/mol•L−1 | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| c(N2)/mol•L−1 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| c(CO2)/mol•L−1 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是______填字母)。
A.通入一定量的 CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的 NO E.加入一定量的活性炭 F.适当升高温度
-
催化还原CO2 是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2 和H2 可发生两个平行反应,分别生成CH3OH 和CO。反应的热化学方程式如下:
I.CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) △H1=-53.7kJ·mol-1
I.CO2(g)+H2(g)  CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
某实验室控制CO2 和H2 初始投料比为1: 2.2,在相同压强下,经过相同反应时间测得如下实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.l | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.l | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
[备注]XCat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2 中生成甲醇的百分比。
已知:①CO和H2的标准燃烧热分别为-283.0kJ/mol和一285.8kJ/mol;
②H2O(l)==H2O(g) △H3=+44.0kJ·mol-1
请回答下列问题(不考虑温度对△H的影响):
(1)反应I在_________(填“低温”或“高温”)下自发进行;反应II每生成9g水蒸气放出热量为___________。
(2)恒容条件下,有利于提高CO2 转化为CH3OH 的平衡转化率的措施有_____(填字母代号)。
A.延长反应时间 B.使用催化剂Cat.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)由表中实验数据可以得出的结论是_______________________。
(4)553 K,使用催化剂Cat.2,在该时刻H2 的转化率为______(填字母代号)。
A.5.5% B.13.3% C.16.4% D.29.3%
(5)在下图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。________
(6)研究证实,CO2 也可在硫酸溶液中用情性电解生成甲醇,则生成甲醇的电极反应式是_________,另一极的电解产物为______________________。
-
催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1I
CO2(g)+H2(g) CO(g)+H2O(g)ΔH2II
CO(g)+H2O(g)ΔH2II
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
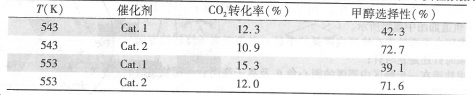
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l) H2O(g)ΔH3=44.0kJ·mol-1
H2O(g)ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=;反应II的ΔH2=kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是。
(4)在图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在极,该电极反应式是。
-
催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,在CO2中通入H2,二者可发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
反应Ⅱ CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
(1)反应Ⅰ的化学平衡常数表达式是K=_______________________________。
(2)一定温度下,在容积可变的密闭容器中进行反应Ⅱ,不能确定上述可逆反应已达到化学平衡状态的是_____________
A.体系的体积不再发生变化 B.生成n mol CO的同时消耗n mol H2O
C.混合气的密度不再改变 D.1 mol H—H键断裂的同时断裂2 mol H—O键
(3)某实验室控制一定的CO2和H2初始投料比,在相同压强下,经过相同的反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
| 反应序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
| ① | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| ② | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
| ③ | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| ④ | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比表中①和③可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_________________________________;
②对比表中①、②可发现,在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因___________________________________________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有____________。
a.使用Cu/ZnO纳米棒做催化剂 b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度 d.投料比不变,增加反应物的浓度
e.增大CO2和H2的初始投料比
(4)反应混合气体经过降温加压可分离出甲醇,剩余气体可再次充入反应器继续反应,经过多次循环往复后混合气体中CO的含量已经很高,可以在另外容器中在合适的催化剂条件下使CO和H2反应合成CH3OH(g),写出该反应的热化学方程式:_______________________________。
=________时,甲烷产率最高。若该条件下CO的产率趋于0,则T℃时①的平衡常数K=___________________。















