0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是
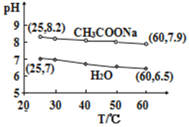
A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
高三化学单选题中等难度题
0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是

A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
高三化学单选题中等难度题
0.5mol·L-1CH3COONa溶液和水的pH随温度的变化如图所示,下列分析错误的是

A.25℃,CH3COONa溶液的pH=8.2,显碱性
B.60℃,H2O中c(H+)=1×10-6.5mol·L-1,呈中性
C.60℃,CH3COONa溶液中c(OH-)=1×10-5.1mol·L-1
D.升高温度,CH3COONa溶液水解程度和pH都减小
高三化学单选题中等难度题查看答案及解析
在25℃时,将1.0L w mol・L-1CH3COOH溶液与0.1molNaOH固体混合,充分反应。然后向混合液中加入CH3COOH或 CH3COONa固体(忽略溶液体积和温度变化),溶液pH变化如图所示。下列叙述正确的是
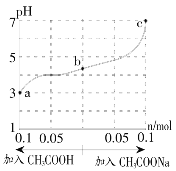
A. a、b、c对应的溶液中,水的电离程度由大到小的顺序是:c>a>b
B. w≥0.1
C. 从b到a的过程中,[c(Na+)·c(OH-)]/c(CH3COO-)增大
D. 25℃时,CH3COOH的电离平衡常数
高三化学单选题中等难度题查看答案及解析
25 ℃时,将1.0L c mol•L-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是
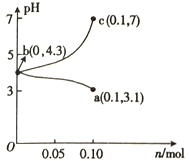
A. 水的电离程度:c>b>a
B. a点对应的混合溶液中,C(CH3COOH)>C(Na+ )>c(OH-)
C. 该温度下,醋酸的电离平衡常数Ka=
D. 当混合溶液呈中性时,c(Na+ )=c(CH3COO-)>c(H+) =c(OH-)
高三化学选择题困难题查看答案及解析
在25 ℃时,将1.0L c mol•L-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入少量CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是
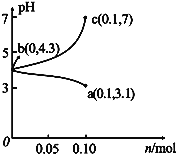
A. 水的电离程度:c>b>a
B. a点对应的混合溶液中,c(CH3COOH)>c(Na+ )>c(OH-)
C. 当混合溶液呈中性时,c(Na+ )=c(CH3COO-)>c(H+) =c(OH-)
D. 该温度下,醋酸的电离平衡常数
高三化学选择题困难题查看答案及解析
实验测得 0.5ml・L-1CH3COONa 溶液和 H2O 的 pH 随温度变化的曲线如图所示。下用说法正确的是
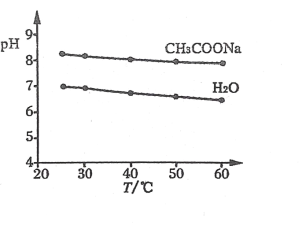
A.随温度升高,CH3COONa 溶液的 c(OH-)增大
B.随温度升高,H2O 的 pH 逐渐减小,是因为水中c(H+)>c(OH-)
C.随温度升高,CH3COONa 溶液的 pH 变化是 Kw 改变不大和水解平衡移动共同作用的结果
D.随温度升高, CH3COONa 溶液的 pH 降低是因为 CH3COO-水解平衡向逆反应方向移动的结果
高三化学多选题简单题查看答案及解析
实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是

A. 随温度升高,纯水中c(H+)>c(OH−)
B. 随温度升高,CH3COONa溶液的c(OH−)减小
C. 随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D. 随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
高三化学单选题简单题查看答案及解析
实验测得0.5 mol·L−1CH3COONa溶液、0.5 mol·L−1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是
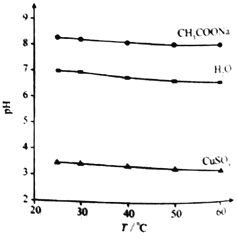
A. 随温度升高,纯水中c(H+)>c(OH−)
B. 随温度升高,CH3COONa溶液的c(OH−)减小
C. 随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D. 随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO−、Cu2+水解平衡移动方向不同
高三化学单选题简单题查看答案及解析
室温下,0.1mol·L-1CH3COONa溶液与 0.1 mol·L-1NaCl溶液等体积混合(忽略溶液体积变化),下列有关叙述正确的是
A.混合前CH3COONa溶液中由水电离出来的c(OH—)>1×10-7 mol·L-1
B.混合前NaCl溶液中:c(Na+) + c(OH—)= c(Cl-)+c(H+)
C.混合溶液中 :c(Cl-) >c(CH3COOH) >c(OH—)
D.混合溶液中:c(Cl-) + c(CH3COO-) =0.1mol·L-1
高三化学选择题中等难度题查看答案及解析
(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中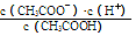 (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为 。
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数随溶液pH变化的情况如下:
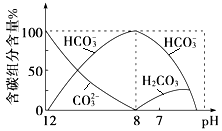
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32- (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有 、 ,溶液中含量最多的三种微粒的物质的量浓度的大小关系为 ;
高三化学简答题极难题查看答案及解析
(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
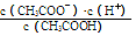 (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为 。
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数随溶液pH变化的情况如下:
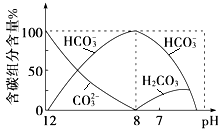
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32- (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有 、 ,溶液中含量最多的三种微粒的物质的量浓度的大小关系为 ;
高三化学填空题极难题查看答案及解析