工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是( )
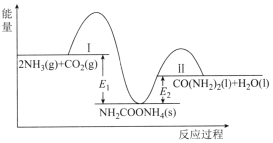
A.NH2COONH4为合成尿素反应的中间产物
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势很大
D.2NH3(g)+CO2(g)CO(NH2)2(1)+H2O(1)的焓变△H=El-E2
高三化学多选题中等难度题
工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是( )

A.NH2COONH4为合成尿素反应的中间产物
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势很大
D.2NH3(g)+CO2(g)CO(NH2)2(1)+H2O(1)的焓变△H=El-E2
高三化学多选题中等难度题
工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。下列说法错误的是( )

A.NH2COONH4为合成尿素反应的中间产物
B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能
C.反应Ⅱ在热力学上进行趋势很大
D.2NH3(g)+CO2(g)CO(NH2)2(1)+H2O(1)的焓变△H=El-E2
高三化学多选题中等难度题查看答案及解析
大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
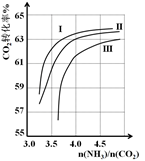
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(g) 在合成塔中进行。下如图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为_______________。
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由_______________。
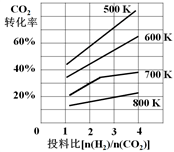
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
①该反应的化学平衡常数的表达式为_____________。
②该反应的∆S__________0,∆H_________0(填“>”或“<”)。
③700K投料比[n(H2)/n(CO2)] = 2时,H2的平衡转化率为___________________。
(3)固体氧化物电解池(SOEC)用于高温电解CO2/H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如下如图。
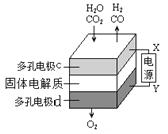
①在c极上反应分两步进行:首先水电解产生氢气,然后氢气与CO2反应产生CO。写出电极c上发生的电极反应式:___________________。
②若电解得到的1:1的合成气(CO+H2),则通入的CO2和H2O物质的量比值为__________。
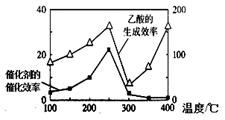
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见如图。如何解释如图中250-400℃时温度升高与乙酸的生成速率变化的关系?______________________。
高三化学简答题困难题查看答案及解析
尿素是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2CO(NH2)2+H2O,当氨碳比
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )

A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率υ逆(CO2)大于B点的正反应速率υ正(CO2)
高三化学选择题中等难度题查看答案及解析
工业上常利用CO2为初始反应物,合成一系列重要的化工原料。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)=NH2COONH4(s)ΔH1
反应Ⅱ:NH2COONH4(s)=CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
请回答下列问题:
①反应Ⅰ的ΔH1=______________。
②在________(填“高温”或“低温”)情况下有利于反应Ⅱ的自发进行。
③一定温度下,在体积固定的密闭容器中按n(NH3)∶n(CO2)=2∶1 进行反应Ⅰ。下列能说明反应Ⅰ达到了平衡状态的是____________(填字母代号)。
A 混合气体的平均相对分子质量不再变化
B 容器内气体总压强不再变化
C NH3与CO2的转化率相等
D 容器内混合气体的密度不再变化
(2)将CO2和H2按质量比25∶3充入一定体积的密闭容器中,在不同温度下发生反应CO2(g)+3H2(g)=CH3OH(g)+H2O(g)。测得CH3OH(g)的物质的量随时间的变化如下图所示。

①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为K(Ⅰ)______(填“>”“<”或“=”)K(Ⅱ)。
②欲提高CH3OH(g)的平衡产率,可采取的措施除改变温度外,还有__________(任写两种)。
③一定温度下,在容积均为2 L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后反应达到平衡。
| 容器 | 甲 | 乙 |
| 反应物起 始投入量 | 1 mol CO2、 3 mol H2 | a mol CO2 b mol H2 c mol CH3OH(g) c mol H2O(g) (a,b,c均不为0) |
若甲容器中反应达平衡后气体的压强为开始时的,则该温度下,反应的平衡常数为______;要使反应达平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_______________。
高三化学综合题困难题查看答案及解析
(15分)二氧化碳的过度排放会引发气候问题,而进行有效利用则会造福人类,如以CO2和 NH3 为原料合成尿素。经研究发现该反应过程为:
① CO2(g) + 2NH3(g) NH2COONH4(s) △H1
② NH2COONH4(s) CO(NH2)2(s) + H2O(g) △H2>0
请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1____0。(选填“>”、“<”或“=”)。
(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g) + 2NH3(g) CO(NH2)2(s) + H2O(g)
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
| CO2的转化率T(℃) | 10min | 20min | 30min | 40min |
| T1 | 30% | 65% | 75% | 75% |
| T2 | 45% | 50% | a1 | a2 |
①T1℃下,l0min内NH3的平均反应速率为__________。
②根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=________,该温度下的化学平衡常数为_________。
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人3molCO2,此时v(正)_____ v (逆)(选填“>”、“<”或“=”),判断的理由是______。
(3)请在下图中补画出合成氨总反应2NH3(g) + CO2(g)CO(NH2)2(s) + H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物CO(NH2)2(s) + H2O(g)〕。
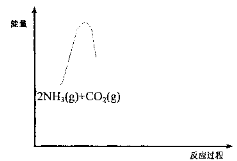
高三化学填空题极难题查看答案及解析

高三化学填空题中等难度题查看答案及解析
氨气在生产、生活和科研中应用十分广泛 。
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47kJ/mol
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+72.49kJ/mol
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH=_____________kJmol。
②液氨可以发生电离:2NH3(l)NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式______________。
(2)氨气易液化,便于储运,可利用NH3作储氢材料已知:2NH3(g)N2(g)+3H2(g) ΔH=+92.4 kJ/mol 。
①氨气自发分解的反应条件是________________(填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度 的变化如图所示。
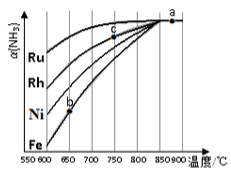
在600℃时催化效果最好的是________________(填催化剂的化学式)。c点氨气的转化率高于b点, 原因是________________。
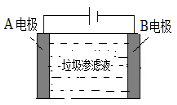
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
①写出电解时A极的电极反应式:________________。
②写出第二步反应的化学方程式:__________________。
高三化学填空题困难题查看答案及解析
氨气在生产、生活和科研中应用十分广泛
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+ 72.49 kJ·mol-1
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH= kJ·mol-1。
②液氨可以发生电离:2NH3(l)NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
(2)氨气易液化,便于储运,可利用NH3作储氢材料
已知:2NH3(g)N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
① 氨气自发分解的反应条件是 (填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如右图所示。
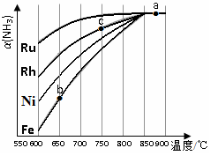
在600℃时催化效果最好的是 (填催化剂的化学式)。c点氨气的转化率高于b点,原因是 。
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
①写出电解时A极的电极反应式: 。
②写出第二步反应的化学方程式: 。
高三化学填空题困难题查看答案及解析
尿素[CO(NH2)2]是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2 CO(NH3)2+H2O,当氨碳比
CO(NH3)2+H2O,当氨碳比,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是
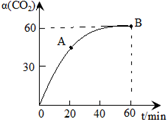
A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率v逆(CO2)大于B点的正反应速率V正(CO2)
高三化学选择题中等难度题查看答案及解析
(14分)(2012•重庆)尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为 .
(2)当氨碳比=4时,CO2的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(CO2) B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”).
②NH3的平衡转化率为 .
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.
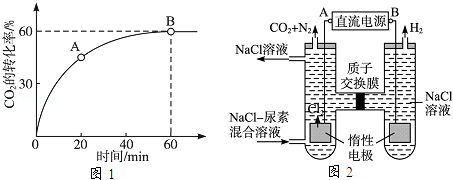
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 .
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
高三化学填空题困难题查看答案及解析