-
(1)H2S的标准燃烧热ΔH=-akJ∙mol−1,H2S燃烧反应的热化学方程式为______
(2)催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在催化剂Cu/ZnO存在下,CO2和H2可发生两个反应,分别生成CH3OH和CO。反应的热化学方程式如下:
Ⅰ.CO2(g)+3H2(g)=CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g)ΔH2
已知:①CO和H2的燃烧热分别为283.0kJ·mol-1和285.8kJ·mol-1
②H2O(l)=H2O(g)ΔH3=+44.0kJ·mol-1
反应Ⅱ的ΔH2=________kJ·mol-1。
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其负极材料为_____,正极电极反应式为________。
高一化学填空题中等难度题查看答案及解析
-
已知H2S的燃烧热 ΔH=-akJ·mol-1,下列热化学方程式正确的是( )
A. 2H2S(g) + O2(g)=2H2O(g) + 2S(s) ΔH=-akJ·mol-1
B. 2H2S(g) + O2(g)=2H2O(l) + 2S(s) ΔH=-akJ·mol-1
C. 2H2S(g) + 3O2(g)=2H2O(l) + 2SO2(g) ΔH=-akJ·mol-1
D. 2H2S(g) + 3O2(g)=2H2O(l) + 2SO2(g) ΔH=-2akJ·mol-1
高一化学单选题简单题查看答案及解析
-
催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH
和CO。反应的热化学方程式如下:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2
(g)+H2(g)
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K)
催化剂
CO2转化率(%)
甲醇选择性(%)
543
Cat.1
12.3
42.3
543
Cat.2
10.9
72.7
553
Cat.1
15.3
39.1
553
Cat.2
12.0
71.6
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)
H2O(g)ΔH3=
+ 44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的逆反应平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施
有 。
A.使用催化剂Cat.1 B.使用催化剂Cat.
2 C.降低反应温度
D.增大CO2和H2的初始投料比 E.投料比不变,增加反应物的浓度
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 。
(4)在图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图。
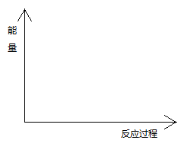
高一化学填空题困难题查看答案及解析
-
蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g)
CO2(g)+4H2(g)ΔH3=+akJ·mol-1
化学键
C—H
H—H
H—O
键能kJ/mol
b
c
d
(1)写出甲烷的结构式___________
(2)C=O的键能为_______________kJ/mol(用含a、b、c、d的式子表示)
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=_____________
时间/min
0
10
20
40
50
60
n(CH4)/mol
0.50
0.35
0.25
0.10
0.10
0.10
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是_______________。
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式______
高一化学填空题中等难度题查看答案及解析
-
某烃A不能使溴水褪色,0.5molA完全燃烧时,得到1.5mol水和67.2L二氧化碳(标准状况)。
(1)A的结构简式为___。
(2)根据下列条件写出有关反应的化学方程式:
①在催化剂FeCl3的作用下,A与液氯反应:___;
②在催化剂作用下A与H2反应:___。
高一化学推断题简单题查看答案及解析
-
(4分)(1)某烃A燃烧的化学方程式为:CxHy+(x+
)O2 → xCO2+
H2O,该反应为 反应(填“吸热”或“放热”);将0.2 mol A完全燃烧生成4.48 L(标准状况下)CO2和7.2 g H2O,则烃A的结构式 。
(2)试分析下列情况下微粒间作用力的变化情况(填“离子键”、“极性键”、“非极性键”或“分子间作用力”)
①MgCl2溶于水时破环 ;
②碘升华破坏 。
高一化学填空题困难题查看答案及解析
-
催化还原CO2是解决温室效应及能源问题的重要手段之一。在恒容密闭容器中,CO2和H2在催化剂作用下发生反应:CO2(g) + 3H2(g)
CH3OH(g) + H2O(g)。CO2、H2、CH3OH、H2O的浓度均不再改变时,下列说法正确的是
A. CO2、H2、CH3OH、H2O的浓度一定相等
B. 该反应已经达到化学平衡状态
C. CO2和H2完全转化为CH3OH和H2O
D. CO2、H2的反应速率等于CH3OH、H2O的反应速率且为零
高一化学单选题中等难度题查看答案及解析
-
催化还原CO2是解决温室效应及能源问题的重要手段之一。在恒容密闭容器中,CO2和H2在催化剂作用下发生反应:CO2(g) + 3H2(g)
CH3OH(g) + H2O(g)。CO2、H2、CH3OH、H2O的浓度均不再改变时,下列说法正确的是
A. CO2、H2、CH3OH、H2O的浓度一定相等
B. 该反应已经达到化学平衡状态
C. CO2和H2完全转化为CH3OH和H2O
D. CO2、H2的反应速率等于CH3OH、H2O的反应速率且为零
高一化学单选题中等难度题查看答案及解析
-
在一固定体积的密闭容器中,进行下列反应:CO2(g)+H2(g)
CO(g)+H2O(g) ΔH=akJ·mol-1其化学平衡常数K和温度T的关系如右表所示:则下列有关叙述正确的是( )
T/℃
700
800
830
1 000
1 200
K
0.6
0.9
1.0
1.7
2.6
A. a<0
B. 可测量容器总压强变化来判定化学反应是否达到平衡
C. 温度为830 ℃时,若c(CO2)·c(H2)>c(CO)·c(H2O),此时v(正)>v(逆)
D. 温度不变,增大c(CO2),平衡右移,K增大
高一化学选择题中等难度题查看答案及解析
-
H2S在O2中不完全燃烧生成S和H2O。下列说法正确的是
A. 氧元素的单质存在周位素 B. 微粒半径:O2->S2-
C. 还原性:H2S>H2O D. 该反应中化学能全部转化为热能
高一化学选择题中等难度题查看答案及解析