-
溴元素主要以Br-形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程示意如图。已知:常温下溴呈液态,深红棕色,易挥发。
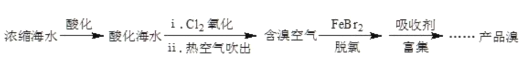
(1)氧化:请写出i中的化学方程式_____。
(2)脱氯:除去含溴空气中残留的Cl2。
①具有脱氯作用的离子是_____。
②溶液失去脱氯作用后,补加FeBr2或加入_____,脱氯作用恢复。
(3)富集、制取Br2:
用Na2CO3溶液吸收溴,Br2歧化为BrO 和Br-。再用H2SO4酸化后可以得到Br2。写出加入H2SO4酸化生成Br2的离子方程式_____。
和Br-。再用H2SO4酸化后可以得到Br2。写出加入H2SO4酸化生成Br2的离子方程式_____。
(4)探究NaBr溶液与H2SO4溶液反应时H2SO4浓度对生成Br2的影响,实验如下:
| 序号 | A | B | C |
| 试剂组成 | 1mol/LNaBr 20%H2SO4 | 1mol/LNaBr 98%H2SO4 | 将B中反应后溶液用水 稀释 |
| 实验现象 | 无明显现象 | 溶液呈棕红色,放热 | 溶液颜色变得很浅 |
①B中溶液呈棕红色说明产生了_____。
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由。若认为乙同学的分析合理,请进一步设计实验方案证明。请从甲乙同学的说法中任选一个作答。
认为甲合理的理由_____(具体反应)。
认为乙合理的实验方案_____。
-
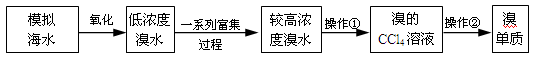
溴被称为“海洋元素”,海水中的溴主要以NaBr的形式存在。查阅资料得知:Br2的沸点为59℃,微溶于水,易溶于有机溶剂。实验室简单模拟从海水(此处以低浓度的NaBr溶液代替)中提取溴单质的流程如图:


(1)写出实验操作的名称,操作① 、操作② ;
(2)在富集过程中,有反应 5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
A.2NaBr+Cl2 = 2NaCl+Br2
B.2H2S+SO2 = 2H2O+3S↓
C.AlCl3+3NaAlO2+6H2O = 4Al(OH)3↓+3NaCl
D.Cl2 + 2NaOH = NaCl +NaClO + H2O
(3)实验前检测分液漏斗没有问题,但在操作①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因可能是 ;
(4)下列说法正确的是 。
A.操作①中,可以用酒精代替CCl4
B.操作②中,若发现忘了加碎瓷片,应该趁热补加
C.操作②中,温度计水银球应浸没在蒸馏烧瓶中液体的液面以下,但不能接触瓶底
D.操作②中,冷凝水流向应该是下进上出
-
溴被称为“海洋元素”,海水中的溴主要以NaBr的形式存在。查阅资料得知:Br2的沸点为59℃,微溶于水,易溶于有机溶剂。实验室简单模拟从海水(此处以低浓度的NaBr溶液代替)中提取溴单质的流程如图:
(1)写出实验操作的名称,操作① 、操作② ;
(2)在富集过程中,有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是
A.2NaBr+Cl2 = 2NaCl+Br2
B.2H2S+SO2 = 2H2O+3S↓
C.AlCl3+3NaAlO2+6H2O = 4Al(OH)3↓+3NaCl
D.Cl2 + 2NaOH = NaCl +NaClO + H2O
(3)实验前检测分液漏斗没有问题,但在操作①的步骤中,旋开分液漏斗下端的旋塞,却发现分液漏斗中的液体很难滴下,其原因是 ;
(4)下列说法正确的是 。
A.操作①中,可以用酒精代替CCl4
B.操作②中,若发现忘了加碎瓷片,应该趁热补加
C.操作②中,温度计水银球应浸没在蒸馏烧瓶中液体的液面以下,但不能接触瓶底
D.操作②中,冷凝水流向应该是下进上出
-
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
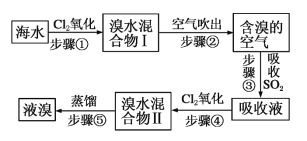
(1)步骤①反应的离子方程式是___________________。
(2)步骤③反应的化学方程式是___________________,从理论上考虑,下列也能吸收Br2的是___________________。
A.FeCl2 B.Na2SO3 C.H2O
(3)步骤①中已获得Br2,步骤③中又将Br2还原为Br-,步骤④又生成Br2,这样做的目的为___________________。
(4)已知海水中Br-含量为64mg/L,依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为___________________L(忽略Cl2的溶解)。
-
海水中溴元素以Br−形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图所示:
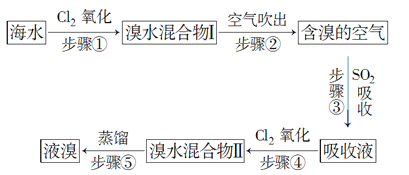
(1)步骤①反应的离子方程式是____________________,步骤③反应的化学方程式是___________________。
(2)从理论上考虑,下列物质也能吸收Br2的是___________(填字母)。
A.NaOH B.FeCl2
C.Na2SO3 D.H2O
(3)步骤③中氧化剂是________,若反应中生成2 mol HBr,则消耗________mol SO2。
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是________________。
-
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
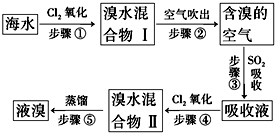
(1)步骤①反应的离子方程式是_______________________________________,
步骤③反应的化学方程式是_______________________________________。
(2)从理论上考虑,下列物质也能吸收Br2的是________________。
A.NaOH B.FeCl2
C.Na2SO3 D.H2O
(3)步骤③中氧化剂是____________,若反应中生成2 mol HBr,则消耗________mol SO2。
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是_______________。
-
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
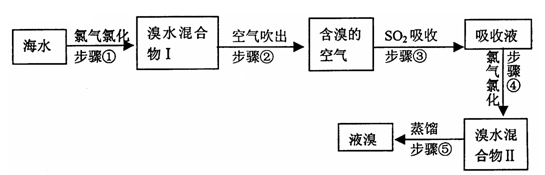
(1)步骤①反应的离子方程式是
(2)步骤③反应的化学方程式是________
(3)Br的原子序数是________ ,在周期表中位于________周期________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因。________
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
________
-
将海水淡化与浓缩海水资源化结合起来是综合利用海水的重要途径之一。浓缩海水中的Br-、Mg2+可通过一系列工艺流程提取出来。
(1)如图是采用膜分离技术淡化海水的示意图,淡化膜可让水分子通过,而海水中其他离子不能通过。加压后,左侧海水中增加的是 (填字母)
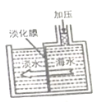
A.溶质质量
B.溶剂质量
C.溶质的质量分数
(2)在浓缩海水中通入氯气,生成Br2,有关的离子方程式是________ _____,该反应中的氧化剂是_____________,生成的Br2可用热空气法吹出的原因_____________。
(3)从海水中提取镁的主要步骤如下:
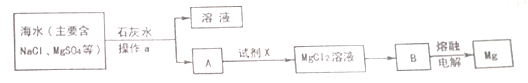
①操作a是
②试剂X是 ,A与X反应的离子方程式 。
③为检验MgCl2溶液中是否含有NaCl残留,实验操作是 。
④生产出的镁在运输途中应防雨淋,原因是 (用化学方程式表示)。
-
空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如图所示。
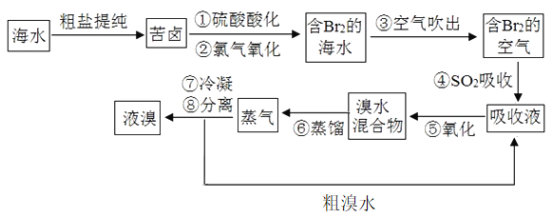
(1)“苦卤”到“含Br2的海水”过程____(填“是”或“不是”)氧化还原反应。
(2)步骤④利用了S02的还原性,反应的离子方程式为____。
(3)步骤⑥的蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,其原因是____。
(4)若处理1 m3海水需要消耗0.45 molSO2,不考虑转化过程中溴的损耗,则海水中溴离子的物质的量浓度为____。
-
海水中化学资源的综合开发利用,已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,如图为提取它们的主要步骤:
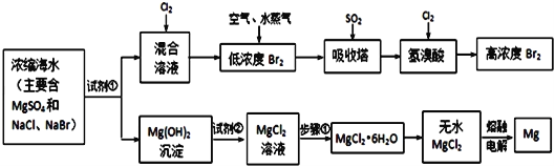
请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是_________。
(2)吸收塔中反应的离子方程式是_______,工业生产1mol Br2,理论上需要Cl2的物质的量为______ 。
(3)取10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100 mol/L AgNO3溶液8.0 mL恰好完全反应,则海水中含溴的含量为______ mg/L(不考虑提纯过程中溴的损失)。
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用__________ (写化学式)。
(2)步骤①包括加热、蒸发、冷却、结晶、____________。
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是_______________。

和Br-。再用H2SO4酸化后可以得到Br2。写出加入H2SO4酸化生成Br2的离子方程式_____。








