如表是ⅥA族部分元素的相关性质。
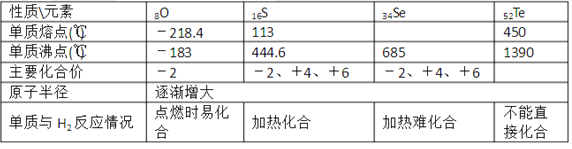
请回答下列问题:
(l)硒的熔点范围可能是____。
(2)碲的化合价可能有____。
(3)氢硒酸有较强的 ____填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生反应的化学方程式为____。
(4)工业上Al2Te可用来制备H2Te,完成下列化学方程式:___ Al2Te3+___ =2Al(OH)3↓+____H2Te↑
高一化学综合题中等难度题
如表是ⅥA族部分元素的相关性质。

请回答下列问题:
(l)硒的熔点范围可能是____。
(2)碲的化合价可能有____。
(3)氢硒酸有较强的 ____填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生反应的化学方程式为____。
(4)工业上Al2Te可用来制备H2Te,完成下列化学方程式:___ Al2Te3+___ =2Al(OH)3↓+____H2Te↑
高一化学综合题中等难度题
如表是ⅥA族部分元素的相关性质。

请回答下列问题:
(l)硒的熔点范围可能是____。
(2)碲的化合价可能有____。
(3)氢硒酸有较强的 ____填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生反应的化学方程式为____。
(4)工业上Al2Te可用来制备H2Te,完成下列化学方程式:___ Al2Te3+___ =2Al(OH)3↓+____H2Te↑
高一化学综合题中等难度题查看答案及解析
下列物质存在如下图所示的转化关系(反应条件、部分产物未标出),已知某物质X是一种正盐,E是强酸

试回答下列问题:
(1)若Y为强酸,且B为黄色固体单质
①从组成物质的元素化合价变化角度预测C可能具有的性质_______________
②一定条件下E转化为C有多种途径,写出其中一种转化的化学反应方程式_______________________。
(2) 若Y为强碱,且B为空气中含量最高的气态单质
①写出实验室制取A的化学方程式______________________________________。
②若A→B的转化常用来检验Z气体管道的是否漏气,用该方法检验的现象是____________________,
其化学反应方程式_________________________________________。
③C、D都是大气污染物,它们对环境造成的危害表现在_______。
A 引起酸雨 B 引起温室效应
C形成光化学烟雾 D引起水体富营养化
④将x mL C、y mL D混合于同一试管中,将试管倒置于水中,同时通入z mL O2充分反应后,试管内气体全部消失,则x:y:z不可能是 _______________
A 1:1:1 B 2:1:1
C 3:7:4 D 1:5:2
(3)无论Y为强酸或强碱均符合上述转化,则物质X的化学式_______________
高一化学简答题困难题查看答案及解析
下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
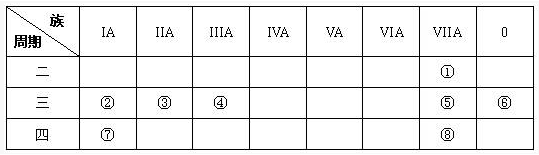
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
高一化学推断题中等难度题查看答案及解析
下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
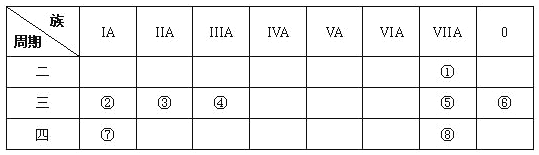
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
高一化学推断题中等难度题查看答案及解析
下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
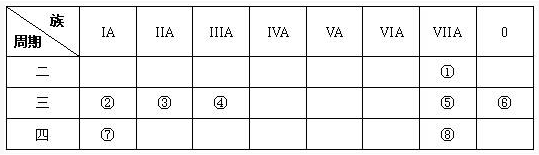
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为______.
(2)用电子式表示①与③形成化合物的过程______.:
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是______. ,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:______.
(4)①②③④四种元素的简单离子半径由大到小的顺序是______.(用离子符号和“>”表示)。
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是______.(用化学式和“>”表示)。
高一化学推断题中等难度题查看答案及解析
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_________。
(2)用于微电子器件生产的锡粉纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是_________________;此锡粉样品中锡的质量分数:_____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
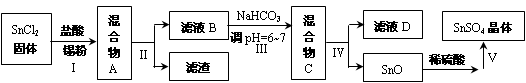
①步骤Ⅰ加入Sn粉的作用: ________________________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、_______________、_______________。
③步骤Ⅲ生成SnO的离子方程式:________________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是___________________,证明已洗净。
⑤步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________。实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是_____________。
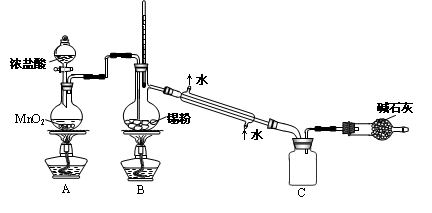
利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是__________________________。
高一化学实验题极难题查看答案及解析
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是_______。
a.单质的熔点降低
b.原子半径和简单离子半径均减小
c.元素的金属性减弱,非金属性增强
d.氧化物对应的水化物碱性减弱,酸性增强
(2)氧化性最弱的简单阳离子是_______;热稳定性:H2O____H2S(填>、<、=)。
(3)写出SiCl4的电子式:________。
(4)已知化合物M由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成谈黄色沉淀A和两种无色有刺意性气味气体B、C,相应物质的转化关系如图:
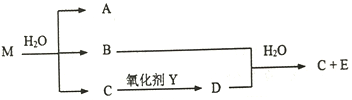
①已知M的摩尔质量为135g/mol,写出M的化学式_____。
②任选一种合适的氧化剂Y,写出C的浓溶液与Y反应生成D的离子反应方程式_______。
③M中的一种元素可形成化合物KXO3,可用于实验室制O2。若不加催化剂,400 ℃时KXO3分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:____________。
高一化学综合题中等难度题查看答案及解析
物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:

(1)类比CO2的性质,学习SO2的性质,写出下列反应的离子方程式。
①少量的SO2通入澄清石灰水中:__________________。
②SO2通入Na2SO3溶液中: ________________________。
(2)Y的分子式:___________________。
(3)Z的稀溶液与铁反应的离子方程式为______________________。
(4)检验CO2是否混有SO2,可以使混合气体通过盛有品红溶液的洗气瓶,这是利用了SO2的_____________性,也可以使混合气体通过盛有酸性高锰酸钾稀溶液的洗气瓶,这是利用了SO2的_____________性。
(5)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原角度分析,合理的是__________(填字母选项)
A.Na2S+S B.Na2SO3+S C.Na2SO3+ Na2SO4 D.SO2+Na2SO4
(6)将X与SO2的水溶液混合后产生淡黄色沉淀,该反应的氧化产物与还原产物的质量之比为__________________
高一化学综合题中等难度题查看答案及解析
物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:

(1)Y是 (化学式)。
(2)将X与Y混合,可生成淡黄色固体,书写相关化学方程式 。
(3)将X的水溶液久置于空气中会变浑浊,说明X具有 性质。
(4)烧杯中加一些蔗糖,滴几滴水,并倒入一些W的浓溶液,用玻璃棒搅拌,观察到的所有现象为 ,说明W的浓溶液具有 、 和 性质。
(5)欲制备Na2S2O3,从氧化还原角度分析,合理的是 (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
高一化学填空题极难题查看答案及解析
类推法是科学学习的重要方法之一。在学习了卤族元素的各种性质后,如下表所示,表格提供的是氧族元素的部分性质。请结合元素周期律完成下列问题:
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | x | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2 反应情况 | 点燃时 易化合 | 加热化合 | 加热难 化合 | 不能直 接化合 |
(1)硒的熔点(x)范围可能是________。
(2)碲的主要化合价可能是________。
(3)在H2O、H2S、H2Se、H2Te四种氢化物中,沸点最低的物质是________;沸点最高的物质是________。
高一化学填空题简单题查看答案及解析