-
汽车发动机稀燃控制系统主要工作原理是发动机在稀燃和富燃条件下交替进行,尾气中的NOx在催化剂上反应脱除。其工作原理示意图如下:
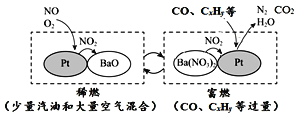
下列说法不正确的是
A. 稀燃过程中,NO发生的主要反应为:2NO + O2 === 2NO2
B. 稀燃过程中,NO2被吸收的反应为:BaO + 2NO2 === Ba(NO3)2
C. 富燃过程中,NO2被CO还原的反应为:2NO2 + 4CO === N2 + 4CO2
D. 富燃过程中,CxHy被O2氧化的反应为:CxHy + (x+y/4)O2 == xCO2 + y/2H2O
-
(1)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)

(2)工业上也常用NaOH溶液吸收法处理NOx  ,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)
,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)
2NO2 + 2NaOH =NaNO2 + NaNO3 + H2O(II)
现有2 240 mL(标准状况)NO 和NO2的混合气体溶于200 mL NaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是 。

(3)NO直接催化分解(生成N2与O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40 ℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示。写出Y和Z的化学式:__________________________。
-
SO2和NOx是主要的大气污染物。某小组认为一定条件下,用NH3与NO2反应转化为无污染物质可进行汽车尾气无害化处理。
(1)氨气的制备
①实验室制氨气的化学方程式为_________。
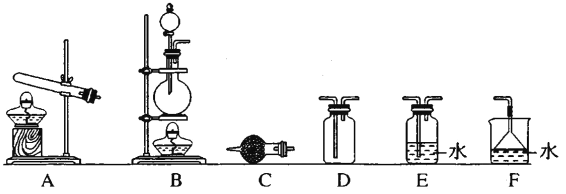
②制备和收集纯净、干燥的氨气,可以选择下图装置______(填序号),C 中试剂为______。
(2)氨气与二氧化氮的反应(已知: 2NO2+2NaOH=NaNO3+ NaNO2+ H2O。)
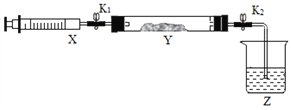
①在硬质玻璃管Y中加入少量催化剂,将NO2气体注入Y管中,Z 中应盛装______。
②打开K1,将注射器X 中的NH3缓慢注入Y中,发生反应的方程式为_______。
③将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Y 中出现倒吸现象,原因是_________。
(3)该小组进一步研究SO2的性质,探究SO2能否与Na2O2发生氧化还原反应。实验室用铜丝和浓硫酸反应生成SO2的化学方程式为____________。利用(2)中装置,将Y中的药品更换为少量Na2O2,将注射器X中SO2缓慢推入Y中,Y 装置中淡黄色粉末变成白色。设计方案检验生成的白色物质中含有SO42-_________。
-
工业生产硝酸的尾气中含有氮氧化物NOx(假设仅为NO和NO2的混合物),影响生态环境。
Ⅰ.氮氧化物NOx 对环境主要影响有两点____、____。
Ⅱ.工业上可用氨催化吸收法处理NOx ,反应原理为:NH3 + NOx N2 + H2O
N2 + H2O
某化学兴趣小组模拟该处理过程的实验装置如下:

(1)装置A中发生反应的化学方程式为________。
(2)装置C的作用有两个:一个作用是通过气泡产生的速率来控制反应物的比例,另一个作用是______。装置F的作用是_______。
(3)反应6 NO2+8 NH3 7 N2+12 H2O可用于处理NO2。当转移3.6 mol电子时,消耗NO2的物质的量为_______mol。
7 N2+12 H2O可用于处理NO2。当转移3.6 mol电子时,消耗NO2的物质的量为_______mol。
Ⅲ.工业上也常用NaOH溶液吸收法处理NOx :
NO + NO2 + 2NaOH= 2NaNO2 + H2O (I)
2NO2 + 2NaOH =NaNO2 + NaNO3 + H2O (II)
(1)当NOx被NaOH溶液完全吸收时,转化为盐。x的值可能是_____(填字母)。
A.1.0 B.1.3 C.1.5 D.2.0
(2)2240 mL(标准状况)NO 和NO2的混合气体溶于200 mL NaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是__________。
Ⅳ.除能防止有毒气体的污染外,NaOH溶液吸收法还具有的优点是_____,其缺点是_____。
-
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务。在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物进行相互反应,生成无毒物质;或者使用新型燃料电池作汽车动力,减少汽车尾气污染。
(1)H2或CO可以催化还原NO以达到消除污染的目的。
已知:N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ·mol-1
2H2(g) + O2(g) = 2H2O(l) △H =-571.6 kJ·mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是 。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2CO(g)+2NO(g)  2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
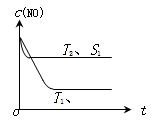
① 该反应的△H 0 (填“>”或“<”)。
② 若催化剂的表面积S1>S2 ,在右图中画出c (NO) 在T1、S2 条件下达到平衡过程中的变化曲线。
(3)在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:

| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c (NO)(×10-3 mol·L-1) | 1.00 | 0.50 | 0.20 | 0.10 | 0.10 |
| c (CO)(×10-3 mol·L-1) | 3.00 | 2.50 | 2.20 | 2.10 | 2.10 |
不考虑温度变化对催化剂催化效率的影响,按要求完成以下计算(写出计算过程,只写出计算结果的不给分):
①计算前2s内的△c (CO2) ;
②计算前2s内的平均反应速率v (N2) ;
③计算达到平衡时NO的转化率。
-
大气污染物NOx、SO2和可吸入颗粒物(PM2.5)等会危害人体健康,影响动植物生长,因此应加强对其监测和治理。请回答:
⑴为降低NOx的排放,在汽车尾气系统中装置催化转化器,可将NOx还原成N2排出。写出NO被CO还原的化学方程式:______________。
⑵某研究小组对PM2.5进行监测时,取其样本用蒸馏水处理制成待测试样,测得有关数据如下:
| 离子 | H+ | Na+ | 
| 
| 
|
| 浓度(mol/L) | | 1×10-5 | 2×10-5 | 3×10-5 | 4×10-5 |
试样中c(H+)=______mol/L。
-
如图是氮氧化物(NOx)的储存还原的工作原理:NOx的储存过程与还原过程在不同时刻是交替进行的。下列有关说法不正确的是( )
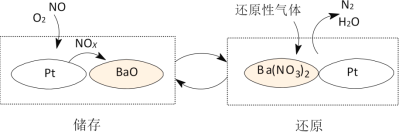
A.“还原”过程中,BaO转化为Ba(NO3)2
B.在储存还原过程中,Pt作催化剂
C.在储存还原过程中,参加反应的NO和O2的物质的量之比为2:1
D.若还原性气体为H2,则参加反应的H2与生成的N2的物质的量之比是5:1
-
汽车尾气催化转化装置的工作原理如图所示:

下列说法不正确的是
A.汽车尾气中含有CO、NO,是雾霾成因之一
B.该过程中NO2既是生成物又是反应物
C.该过程中氧元素被还原,氮元素只被氧化
D.该过程中会发生反应:2NO2 + 4CO 4CO2 + N2
4CO2 + N2
-
工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx (2x+3)N2+6xH2O
(2x+3)N2+6xH2O
某化学兴趣小组模拟该处理过程的实验装置如下:
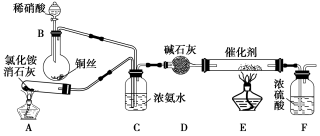
①装置A中发生反应的化学方程式为_____________________。
②装置D中碱石灰的作用是_____________________________。
(2)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3===2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3===NaNO2+NaNO3+CO2(Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是________(填字母)。
A.1.9 B.1.7 C. 1.2
②将1 mol NOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO、NO两种离子的物质的量随x变化关系如图所示:

图中线段a表示____________的物质的量随x值变化的关系;若用溶质质量分数为42.4%的 Na2CO3溶液吸收,则需要Na2CO3溶液至少________g。
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则NOx中的x值为____________。
-
工业尾气中氮氧化物通常采用氨催化吸收法,其原理是NH 3 与NOx在催化剂作用下反应生成无毒的物质。某校活动小组同学采用以下装置和步骤模拟工业上氮氧化物 的处理过程。
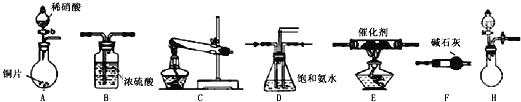
I.探究制取NH 3 的方法
(1)B装置的名称:______________
(2)在上述装置中,H能快速、简便制取,装置中需要添加的反应试剂为_________ 。
(3)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
分析表中数据,你认为哪种方案制取氨气的效果最好________(填序号),从该方案选择的原料分析制气效果好的可能原因是________,__________。
| 试剂组合序号 | 固体试剂 | NH 3 体积(mL) |
| a | 6.0gCa(OH) 2 过量 | 5.4gNH 4 Cl | 1344 |
| b | 5.4g(NH 4 ) 2 SO 4 | 1364 |
| c | 6.0gNaOH过量 | 5.4gNH 4 Cl | 1568 |
| d | 5.4g(NH 4 ) 2 SO 4 | 1559 |
| e | 6.0gCaO过量 | 5.4gNH 4 Cl | 1753 |
| f | 5.4g(NH 4 ) 2 SO 4 | 1792 |
II.模拟尾气处理
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)_______。
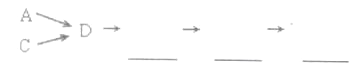
(2)A中反应的离子方程式为__________________________
(3)D装置的作用有:_____________、____________、_____________。
(4)D装置中的液体还可换成(填序号)。
A.H 2 O B.CCl 4 C.浓H 2 SO 4 D.CuSO 4 溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是___________.












