-
(1)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)

(2)工业上也常用NaOH溶液吸收法处理NOx  ,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)
,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)
2NO2 + 2NaOH =NaNO2 + NaNO3 + H2O(II)
现有2 240 mL(标准状况)NO 和NO2的混合气体溶于200 mL NaOH溶液中,恰好完全反应,并无气体放出,则NaOH溶液物质的量浓度是 。

(3)NO直接催化分解(生成N2与O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40 ℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示。写出Y和Z的化学式:__________________________。
-
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务。在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物进行相互反应,生成无毒物质;或者使用新型燃料电池作汽车动力,减少汽车尾气污染。
(1)H2或CO可以催化还原NO以达到消除污染的目的。
已知:N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ·mol-1
2H2(g) + O2(g) = 2H2O(l) △H =-571.6 kJ·mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是 。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2CO(g)+2NO(g)  2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
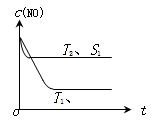
① 该反应的△H 0 (填“>”或“<”)。
② 若催化剂的表面积S1>S2 ,在右图中画出c (NO) 在T1、S2 条件下达到平衡过程中的变化曲线。
(3)在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:

| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c (NO)(×10-3 mol·L-1) | 1.00 | 0.50 | 0.20 | 0.10 | 0.10 |
| c (CO)(×10-3 mol·L-1) | 3.00 | 2.50 | 2.20 | 2.10 | 2.10 |
不考虑温度变化对催化剂催化效率的影响,按要求完成以下计算(写出计算过程,只写出计算结果的不给分):
①计算前2s内的△c (CO2) ;
②计算前2s内的平均反应速率v (N2) ;
③计算达到平衡时NO的转化率。
-
三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图所示,化合物X通过红外光谱仪测定其含有NO3-,下列说法不正确的是 ( )
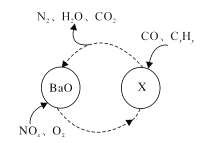
A. X的化学式为Ba(NO3)2 B. 图示的转化中,被还原的元素是N、O
C. 图示生成X的转化中NOx做氧化剂 D. 图示中的所有转化均为氧化还原反应
-
汽车尾气已成为城市空气的主要污染源.
(1)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管内装一个催化转化装置,使NO与CO反应,生成无毒的N2和CO2.反应的化学方程式是 .
(2)下列措施中,能减少或控制汽车尾气污染有效且可行的是 .
A.制定严格的汽车尾气排放标准,并严格执行.
B.开发清洁能源汽车,如氢能汽车、太阳能汽车等.
C.市民出行戴防毒面具.
D.市民大量移居城市郊区.
-
汽车尾气(含CO、SO2、NO等)是城市空气的污染源之一,治理方法之一是在汽车的排气管上装一个“催化转化器”(用铂、钯合金作催化剂),它能使一氧化碳跟一氧化氮反应生成可参与大气循环的无毒气体。
(1)汽车尾气中导致酸雨形成的主要物质是________(填化学式)。
(2)在汽车排气管上加装“催化转化器”,可使CO和NO反应产生可参与大气循环的无毒气体,请写出该反应的化学方程式:__________。该反应的还原剂为:______氮元素的化合价_______(填“升高”或“降低”)。
(3)请写出汽车尾气形成硝酸型酸雨的主要反应的化学方程式:__________
-
汽车尾气(含CO、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气
生态循环的无毒气体,并促进二氧化硫的转化.
(1)汽车尾气中导致酸雨形成的主要物质是______.
(2)写出在催化剂的作用下CO跟NO反应的化学方程式______ 2CO2+N2
-
大气污染物主要成分是SO2、NO2、NO、CO及可吸入颗粒等,主要来自于燃煤、机动车尾气和工业废气,会导致雾霾、酸雨等。
(1)汽车的三元催化转化器中,在催化剂作用下NO和CO转化为无毒气体,反应的化学方程式是: 2CO+2NO  2CO2+N2,该反应中,氧化剂是____________(填化学式),氧化产物是______________(填化学式),当生成2mol N2时,转移电子的物质的量是____________________。
2CO2+N2,该反应中,氧化剂是____________(填化学式),氧化产物是______________(填化学式),当生成2mol N2时,转移电子的物质的量是____________________。
(2)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2转化为SO42―。已知0.1mol/L 100mLNaClO溶液,可以恰好吸收0.01moL SO2,则反应的离子方程式是______________________。
(3)SO2通过如图过程既能制得H2SO4又能制得H2。图中可循环利用的物质X是_________(填化学式),制得H2SO4的化学方程式是__________________________。
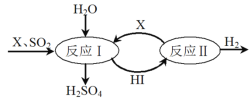
(4)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:NO2+NO+2NaOH===2NaNO2+H2O 2NO2+2NaOH===NaNO2+NaNO3+H2O
现有V L某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。所用烧碱溶液的物质的量浓度至少为________ mol·L−1。若所得溶液中c( )∶c(
)∶c( )=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=____________________。
)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=____________________。
-
SO2和NOx是主要的大气污染物。某小组认为一定条件下,用NH3与NO2反应转化为无污染物质可进行汽车尾气无害化处理。
(1)氨气的制备
①实验室制氨气的化学方程式为_________。
②制备和收集纯净、干燥的氨气,可以选择下图装置______(填序号),C 中试剂为______。
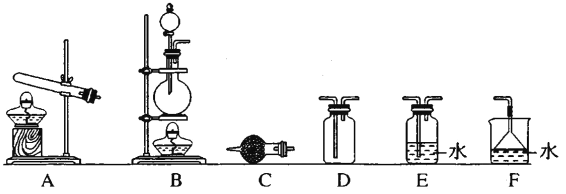
(2)氨气与二氧化氮的反应(已知: 2NO2+2NaOH=NaNO3+ NaNO2+ H2O。)
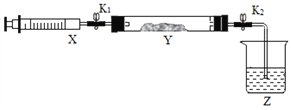
①在硬质玻璃管Y中加入少量催化剂,将NO2气体注入Y管中,Z 中应盛装______。
②打开K1,将注射器X 中的NH3缓慢注入Y中,发生反应的方程式为_______。
③将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Y 中出现倒吸现象,原因是_________。
(3)该小组进一步研究SO2的性质,探究SO2能否与Na2O2发生氧化还原反应。实验室用铜丝和浓硫酸反应生成SO2的化学方程式为____________。利用(2)中装置,将Y中的药品更换为少量Na2O2,将注射器X中SO2缓慢推入Y中,Y 装置中淡黄色粉末变成白色。设计方案检验生成的白色物质中含有SO42-_________。
-
汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源.冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气循环的无毒气体,并促使烃类充分燃烧及SO2的转化.
(1)写出一氧化碳与一氧化氮反应的化学方程式:________.
(2)“催化转化器”的缺点是一定程度上提高了空气的酸度,其原因是________.
A.CO转化为CO2,产生了碳酸酸雾
B.SO2转化为SO3,产生了硫酸酸雾
C.NO转化为NO2,产生了硝酸酸雾
(3)“绿色化学”的最大特点在于从源头上实现污染预防.为控制汽车尾气污染,下列措施符合绿色化学思想的有________(多选扣分).
A.开发氢能源 B.使用电动汽车 C.植树造林 D.戴上呼吸面具.
-
在宏观—微观—符号之间建立联系,是化学学科特有的思维方式。汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”便可以使汽车的尾气转换成无毒气体。如用●表示碳原子,用○表示氧原子,用 表示氮原子,下图为气体转换的微观过程。请根据图示回答下列问题:
表示氮原子,下图为气体转换的微观过程。请根据图示回答下列问题:
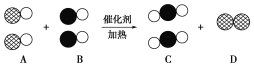
(1)A、B、C三种物质可以归为一类的依据是_________________________________
(2)将C归为化合物,将D归为单质的理由是_______________。
(3)图示反应用化学反应方程式表示为_________化学变化过程中消耗的A物质和生成的C物质的质量比为________。

,已知:NO + NO2 + 2NaOH= 2NaNO2 + H2O(I)






