已知N2(g)+3H2(g)2NH3(g) ΔH=-92.4kJ/mol,一定条件下体系中各物质浓度随时间变化的曲线如图所示。下列说法正确的是( )
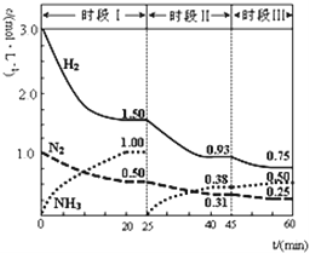
A.前20分钟内反应放出的热量为46.2kJ
B.时段Ⅰ,若仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
C.第25分钟改变的条件可以是将NH3从反应体系中分离出去
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件一定是增大压强
高三化学多选题中等难度题
已知N2(g)+3H2(g)2NH3(g) ΔH=-92.4kJ/mol,一定条件下体系中各物质浓度随时间变化的曲线如图所示。下列说法正确的是( )

A.前20分钟内反应放出的热量为46.2kJ
B.时段Ⅰ,若仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
C.第25分钟改变的条件可以是将NH3从反应体系中分离出去
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件一定是增大压强
高三化学多选题中等难度题
已知N2(g)+3H2(g)2NH3(g) ΔH=-92.4kJ/mol,一定条件下体系中各物质浓度随时间变化的曲线如图所示。下列说法正确的是( )

A.前20分钟内反应放出的热量为46.2kJ
B.时段Ⅰ,若仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
C.第25分钟改变的条件可以是将NH3从反应体系中分离出去
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件一定是增大压强
高三化学多选题中等难度题查看答案及解析
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时, 体系中各物质浓度随时间变化的曲线如图示。下列说法不正确的是( )
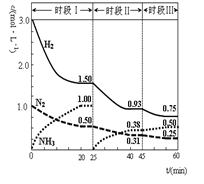
A.前20分钟反应内放出的热量为46.2kJ
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
高三化学选择题困难题查看答案及解析
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
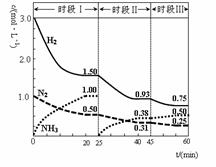
A.前20分钟反应内放出的热量为46.2kJ
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
高三化学选择题简单题查看答案及解析
N2 (g)+3H2 (g) 2NH3(g) ΔH=-92.4 kJ/mol。1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是( )
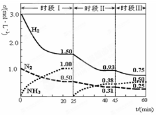
A.前20分钟反应物的转化率为50%
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
高三化学选择题中等难度题查看答案及解析
N2(g)+3H2(g) 2NH3(g) +92.4 kJ。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
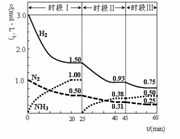
A.前20分钟反应内放出的热量为46.2kJ
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是增大压强
D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
高三化学选择题困难题查看答案及解析
N2 (g)+3H2 (g) 2NH3(g) ΔH=-92.4 kJ·mol-1。 1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示。
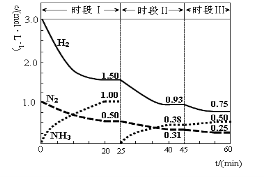
下列说法错误的是:
A.前20分钟反应物的转化率为50%
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大
D.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
高三化学选择题中等难度题查看答案及解析
(1)N2(g)+3H2(g)2NH3(g) △H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。

①在1L容器中发生反应,前20min内,v(NH3)=________,放出的热量为________;
②25min时采取的措施是________;
③时段III条件下,反应的平衡常数表达式为(用具体数据表示)。
(2)电厂烟气脱氮的主反应①:4NH3(g)+6NO(g)5N2(g)+6H2O(g) △H<0,副反应②:2NH3(g)+8NO(g)
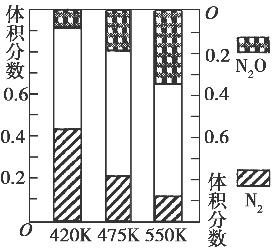
5N2O(g)+3H2O(g) △H>0。平衡混合气中N2与N2O含量与温度的关系如右图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是________,导致这种规律的原因是(任答合理的一条原因)。
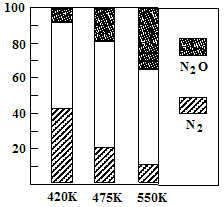
(3)直接供氨式燃料电池是以NaOH溶液为电解质的。电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为________。
高三化学计算题极难题查看答案及解析
(1)N2(g)+3H2(g) 2NH3(g) ΔH=-94.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图所示。
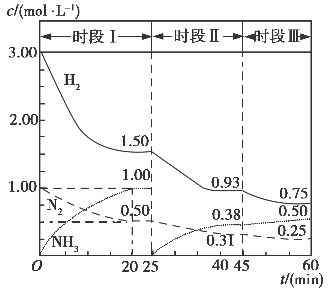
①在1 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②25 min时采取的措施是_______________________;
③时段Ⅲ条件下反应的平衡常数表达式为________(用具体数据表示)。
(2)电厂烟气脱离氮的主反应①:4NH3(g)+6NO(g)5N2(g)+6H2O(g),副反应②:2NH3(g)+8NO (g)
5N2O(g)+3H2O(g) ΔH>0。测得平衡混合气中N2和N2O含量与温度的关系如图。在400~600 K时,平衡混合气中N2含量随温度的变化规律是________,导致这种变化规律的原因是________(任答合理的一条原因)。
(3)直接供氨式燃料电池是以NaOH溶液为电解质的。电池反应为4NH3+3O2=2N2+6H2O,则负极电极反应式为________。
高三化学填空题困难题查看答案及解析
科学家一直致力于“人工固氮”的方法研究。
(1)合成氨的原理为:N2(g)+3H2(g)2NH3(g)ΔH=-92.4 kJ/mol,该反应的能量变化如图所示。
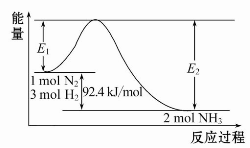
①在反应体系中加入催化剂,反应速率增大,E2的变化是 (填“增大”、“减小”或“不变”)。
②将0.3 mol N2和0.5 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的,此时H2的转化率为 ;欲提高该容器中H2的转化率,下列措施可行的是 (填选项字母)。
A.向容器中按原比例再充入原料气
B.向容器中再充入一定量H2
C.改变反应的催化剂
D.液化生成物分离出氨
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g)
ΔH=+1 530 kJ/mol
又知:H2O(l)H2O(g) ΔH=+44.0 kJ/mol
则2N2(g)+6H2O(g)4NH3(g)+3O2(g) ΔH= kJ/mol,该反应的化学平衡常数表达式为K ,控制其他条件不变,增大压强,K值 (填“增大”、“减小”或“不变”)。
高三化学填空题中等难度题查看答案及解析
N2(g)+3H2(g)≒2NH3(g) △H=-92.2KJ/mol。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是
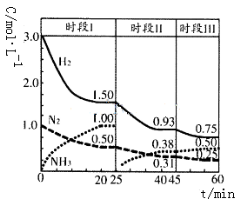
A.若时段I中投入物质的浓度为原来的2倍,则反应物的转化率增大,平衡常数不变
B.第25min改变的条件是将NH3从反应体系中分离出去
C.若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
D.前25min内反应放出的热量为46.lkJ
高三化学选择题困难题查看答案及解析