-
雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。回答下列问题:
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol -1
2SO3(g) ΔH=-196.6 kJ·mol -1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) 的ΔH= kJ·mol-1。
SO3(g)+NO(g) 的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说反应达到平衡状态的有 。(填字母)
a.体系密度保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
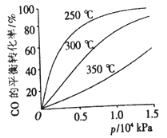
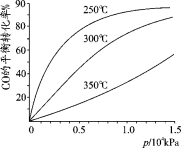
(2)CO可用于合成甲醇,反应的化学方程式为 CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)一种用NH3脱除烟气中NO的原理如下图:
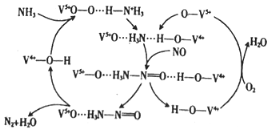
①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为 。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,反应物与生成物三者的物质的量之比比3:1:1,则该反应的化学方程式为 。
-
雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。回答下列问题:
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol -1
2SO3(g) ΔH=-196.6 kJ·mol -1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) 的ΔH= kJ·mol-1。
SO3(g)+NO(g) 的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说反应达到平衡状态的有 。(填字母)
a.体系密度保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
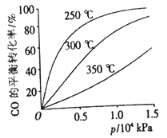
(2)CO可用于合成甲醇,反应的化学方程式为 CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)一种用NH3脱除烟气中NO的原理如下图:
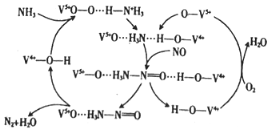
①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为 。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,反应物与生成物三者的物质的量之比比3:1:1,则该反应的化学方程式为 。
-
雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染问题中有着重要的作用。
(1)已知:①2CO(g)+O2(g)=2CO2(g)△H1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g)△H2=+64kJ·mol-1
反应2NO2(g)+4CO(g=N2(g)+4CO2(g)在__________(填“高温”或“低温”)条件下能自发进行。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1:2、1:1.5、3:1时,NO脱除率随温度变化的曲线如图1所示。
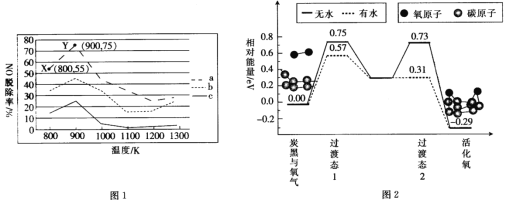
①曲线a中,NO的起始浓度为6×10-4mg·m-3,若从X点到Y点经过20s,则该时间段内NO的脱除速率为_________mg·m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是________,其理由是__________
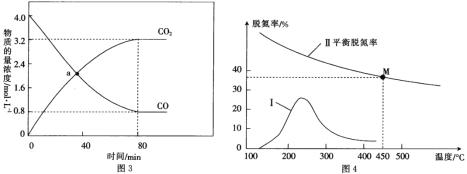
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程中的能量变化模拟计算结果如图2所示。无水情况下,一个氧分子的活化能为__________,容易活化氧分子的条件是_________(填“有水”或“无水”)。
(4)若反应2NO(g)+2CO(g) N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。
N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。
①a点时,v逆:v正=_____________。
②测得平衡时体系压强为p,KP为用气体分压表示的平衡常数,分压=总压×物质的量分数,则平衡常数KP=____________(用含p的式子表示)。
(5)某研究小组探究该反应中催化剂对脱氮率(NO的转化率)的影响。将等物质的量的NO和CO以一定的流速分别通过催化剂a、b,发生反应2NO(g)+2CO(g) N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________
-
雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:① ΔH1=-566.0 kJ·mol-1②
ΔH1=-566.0 kJ·mol-1② ΔH2=-116.5 kJ·mol-1③
ΔH2=-116.5 kJ·mol-1③ ΔH3=+180.5 kJ·mol-1,废气中NO2 与CO 转化成无污染气体的热化学方程式为____。
ΔH3=+180.5 kJ·mol-1,废气中NO2 与CO 转化成无污染气体的热化学方程式为____。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。
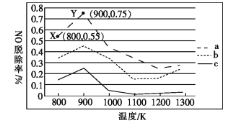
①曲线a中,NO的起始浓度为6×10-4mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为___________mg· m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是___,其理由是___。
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程的能量变化模拟计算结果如图所示。
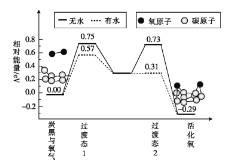
无水情况下,一个氧分子的活化能为__ ,容易活化氧分子的条件是___(填“有水”或“无水”)。
(4)利用反应 构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
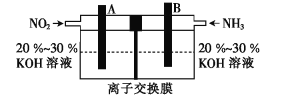
①B极的电极反应式为___。
②若反应转移1.2 mol电子,A极生成N2的体积为___L(标准状况)。
-
雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:① ΔH1=-566.0 kJ·mol-1②
ΔH1=-566.0 kJ·mol-1② ΔH2=-116.5 kJ·mol-1③
ΔH2=-116.5 kJ·mol-1③ ΔH3=+180.5 kJ·mol-1,废气中NO2 与CO 转化成无污染气体的热化学方程式为____。
ΔH3=+180.5 kJ·mol-1,废气中NO2 与CO 转化成无污染气体的热化学方程式为____。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。
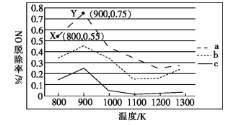
①曲线a中,NO的起始浓度为6×10-4mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为___________mg· m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是___,其理由是___。
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程的能量变化模拟计算结果如图所示。
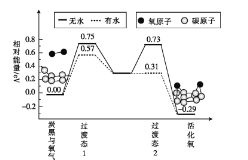
无水情况下,一个氧分子的活化能为__ ,容易活化氧分子的条件是___(填“有水”或“无水”)。
(4)利用反应 构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
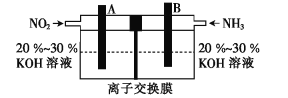
①B极的电极反应式为___。
②若反应转移1.2 mol电子,A极生成N2的体积为___L(标准状况)。
-
雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=−196.6 kJ·mol−1
2SO3(g) ΔH=−196.6 kJ·mol−1
2NO(g)+O2(g) 2NO2(g) ΔH=−113.0 kJ·mol−1
2NO2(g) ΔH=−113.0 kJ·mol−1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)ΔH= kJ·mol−1。
SO3(g)+NO(g)ΔH= kJ·mol−1。
一定条件下,将NO2与SO2以体积比1∶2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有 。
A.体系密度保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)如图是一种用NH3脱除烟气中NO的原理。
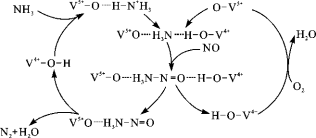
①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 mol O2时,除去的NO在标准状况下的体积为 L。
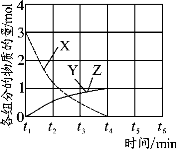
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示,写出NO分解的化学方程式 。
-
化学在解决雾霾污染中有着重要的作用,雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5)、氮氧化物(NOx)、CO、SO2等。
(1)已知:NO(g)+1/2O2(g) NO2(g) ΔH=-56.5 kJ·mol-1
NO2(g) ΔH=-56.5 kJ·mol-1
2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=________kJ·mol-1。
SO3(g)+NO(g) ΔH=________kJ·mol-1。
一定条件下,将NO2与SO2以体积比1︰2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有______________。
a.混合气体的平均相对分子质量 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1︰3,则平衡常数K=___________(用分数表示)
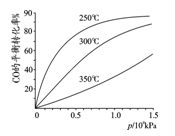
(2)CO综合利用。①CO用于合成甲醇反应方程式为:CO(g)+2H2(g) CH3OH(g)若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如右图所示。得知该反应的∆H 0,该反应的实际生产条件控制在 ℃、1.3×104kPa左右最为适宜。反应达平衡后,下列操作既能加快反应速率,又能使平衡混合物中CH3OH物质的量分数增大的是_____________
CH3OH(g)若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如右图所示。得知该反应的∆H 0,该反应的实际生产条件控制在 ℃、1.3×104kPa左右最为适宜。反应达平衡后,下列操作既能加快反应速率,又能使平衡混合物中CH3OH物质的量分数增大的是_____________
a.升温
b.恒容条件下充入H2
c.加入合适的正催化剂
d.恒容条件下再充入1molCO,2mol H2
e.压缩体积
f.移走一部分CH3OH
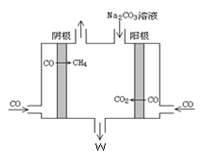
②电解CO制备CH4,电解质为碳酸钠溶液,工作原理如下图所示,写出阴极区电极反应式___________________
-
化学在解决雾霾污染中有着重要的作用,雾霾由多种污染物形成,其中包含颗粒物PM2.5)、
氮氧化物(NOx)、CO、SO2等.
(1)已知:NO(g)+ O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)△H=_________kJ•mol﹣1.
一定条件下,将NO2与SO2以物质的量比1:2置于恒温恒容的密闭容器中发生上述反应,
下列能说明反应达到平衡状态的有____________
a.混合气体的平均相对分子质量
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2物质的量比为1:3,则平衡常数K=________(用分数表示)
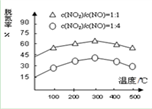
NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请解释300℃之后脱氮率逐渐减小的原因:__________________________
(2)CO综合利用.
①CO用于合成甲醇反应方程式为:CO(g)+2H2(g)═CH3OH(g)
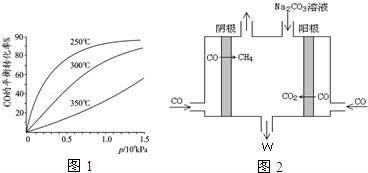
若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如图所示.得知该反应的△H_________0,该反应的实际生产条件控制在 250 ℃、1.3×104kPa左右最为适宜.反应达平衡后,下列操作既能加快反应速率,又能使平衡混合物中CH3OH物质的量分数增大的是____________
a. 升温 b.恒容条件下充入H2
c.加入合适的正催化剂 d.恒容条件下再充入1molCO,2mol H2
e.压缩体积 f.移走一部分CH3OH
②电解CO制备CH4,电解质为碳酸钠溶液,工作原理如图2所示,写出阴极区电极
反应式_______________
(3)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,具体步骤如下:
SO2(g)+H2O(l)  H2SO3(l)
H2SO3(l)  H+(aq)+HSO
H+(aq)+HSO (aq) Ⅰ
(aq) Ⅰ
HSO (aq)
(aq)  H+(aq)+SO
H+(aq)+SO (aq) Ⅱ
(aq) Ⅱ
Ca(OH)2(s)  Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+SO (aq)
(aq)  CaSO3(s) Ⅳ
CaSO3(s) Ⅳ
该温度下,测定吸收后液体中c(Ca2+)一直保持为0.70 mol/L,已知Ksp(CaSO3)=1.4×10-7,则吸收后溶液中的SO 的浓度为_________________
的浓度为_________________
-
(15分)雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=_________kJ·mol-1。
SO3(g)+NO(g) ΔH=_________kJ·mol-1。
一定条件下,将NO2与SO2以体积比1︰2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有_______________。
a.体系密度保持不变
b.混合气体颜色保持不变
c.SO2和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1︰5,则平衡常数K=_______。
(2)CO、CO2都可用于合成甲醇。
①CO用于合成甲醇反应方程式为:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
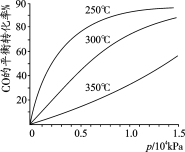
CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_________________________________________。
②CO2用于合成甲醇反应方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
下图是科学家现正研发的,以实现上述反应在常温常压下进行的装置。写出甲槽的电极反应____________。
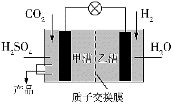
(3)下图是一种用NH3脱除烟气中NO的原理。
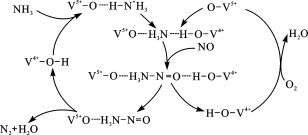
①该脱硝原理中,NO最终转化为H2O和_________(填化学式)。
②当消耗2 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为__________L。
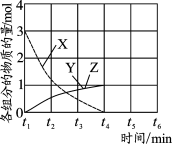
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示,写出NO分解的化学方程式_______________________________。
-
(14分)雾霾由多种污染物形成,其中包含颗粒物(包括PM2.5在内)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol -1
2SO3(g) ΔH=-196.6 kJ·mol -1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有 。
a.体系密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
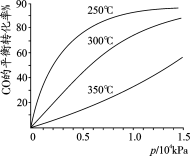
CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
(3)下图是一种用NH3脱除烟气中NO的原理。
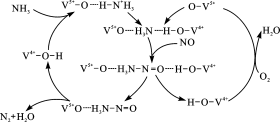
①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1 mol NH3和0.5 molO2时,除去的NO在标准状况下的体积为 L。
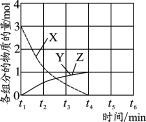
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示,写出NO分解的化学方程式 。

N2(g)+2CO2(g)的正、逆反应速率分别可表示为v正=k正c2(NO)·c2(CO);v逆=k逆c(N2)·c2(CO2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。一定温度下,在体积为1L的恒容密闭容器中加入4molNO和4molCO发生上述反应,测得CO和CO2的物质的量浓度随时间的变化如图3所示。

N2(g)+2CO2(g)。相同时间、不同温度下测得使用催化剂a时脱氮率与温度的关系如图4中曲线Ⅰ所示。已知催化效率b>a,催化剂b的活性在450℃时最大(未达平衡)。请在图4中画出使用催化剂b时所对应的曲线(从300℃开始画)。_______________























