-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
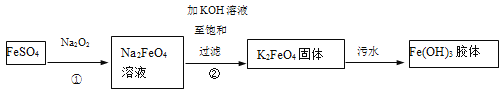
以下说法不正确的是
A.①中一定发生了氧化还原反应
B.污水处理中产生Fe(OH)3胶体,使悬浮物聚沉,利用了胶体具有较强吸附能力的特点
C.另一种在碱性条件下制备K2FeO4的反应可能是:2Fe(OH)3+3ClO-=2FeO42-+3Cl-+4H+ +H2O
D.K2FeO4还可以用于处理废水,例如可以把废水中的CN-转化为两种无毒气体,反应过程中,CN-做还原剂,被K2FeO4氧化
高一化学单选题中等难度题查看答案及解析
-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
回答下列问题:
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中还原剂是___。每生成1molO2,该反应转移___mol电子。
②K2FeO4在水处理过程中所起的作用是___。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:___。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),其原因是___。
高一化学综合题中等难度题查看答案及解析
-
高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。制备K2FeO4如下图:查阅资料:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
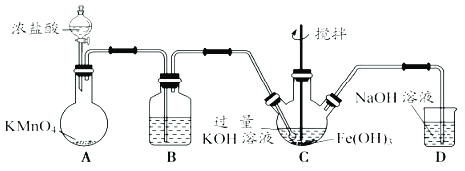
(1)A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为______,A中化学反应的还原剂是______。
(2)装置B的作用是除杂,所用试剂为___________。
(3)C为制备K2FeO4装置,KOH溶液过量的原因是_________________________。
(4)D为尾气处理装置,发生反应的离子方程式为___________________________。
高一化学实验题中等难度题查看答案及解析
-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + aNa2O2 =2Na2FeO4 + bX + 2Na2SO4 + c O2↑
①该反应中物质 X 应是___________,a与c的关系是____________。
②简要说明 K2FeO4 作为水处理剂时,在水处理过程中所起的作用_______________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:__________________________ 。
②若反应过程中转移了0.3mo1电子,则还原产物的物质的量为______mo1。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题____________。
高一化学填空题困难题查看答案及解析
-
.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂是__。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:___。
②每生成2molFeO42-转移_______mol电子,若反应过程中转移了0.5mol电子,则还原产物的物质的量为___mol。
高一化学填空题中等难度题查看答案及解析
-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑该反应中氧化剂是__________(填化学式),过氧化钠(Na2O2)中氧元素化合价为__________。(填数字)
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________。
②每生成1mol FeO42-转移__________mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为__________mol。
高一化学综合题中等难度题查看答案及解析
-
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2 Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中还原剂是_________,每生成1mol O2转移_______mol电子。
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用_________________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:____________________________。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),其原因是________________________________________________。
高一化学填空题困难题查看答案及解析
-
Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中氧化剂是________________(填化学式),过氧化钠(Na2O2)中氧元素化合价为____________。(填数字)
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:___________________________________________________________。
②每生成1mol FeO42-转移________mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为______________mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是________________________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为________________________(用含a、b的代数式表示)。
高一化学综合题困难题查看答案及解析
-
Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是________(填氧化剂、还原剂),与CO2反应的化学反应方程式_________________________。
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:___________________________________________________________。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为____mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=_______(用含a、b的代数式表示)。
高一化学填空题困难题查看答案及解析
-
高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。结合所学知识回答相关问题:
(1)K2FeO4中铁元素的化合价是______价。
(2)制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2= 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑(已知Na2O2中氧元素化合价为-1价)。该反应中还原剂是________________(填化学式),若有1 mol O2生成,转移电子的物质的量为_____ mol。
(3)某反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O,写出在碱性条件下,制高铁酸钾的离子反应方程式________________________________。
(4)在水处理过程中,K 2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉。胶体区别于其他分散系的本质特征是________________________________________。
高一化学综合题困难题查看答案及解析