-
电化学的应用十分广泛,是现代生产、生活、国防,乃至整个人类生活不可缺的物质条件。请根据所给材料回答下列问题:
(1)请结合组成原电池的条件,将氧化还原反应:2Fe3++Cu=2Fe2++Cu2+设计成一个原电池。
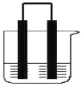
①电解液:___,
②正极材料:___;
③负极反应式:___。
(2)用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:NiO(OH)+MH Ni(OH)2+M
Ni(OH)2+M
①电池放电时,负极的电极反应式为___。
②当该电池充电时,与外电源正极连接的电极上发生的反应是___。
A.H2O的还原 B.NiO(OH)的还原 C.H2的氧化 D.Ni(OH)2的氧化
(3)按如图电解饱和食盐水溶液,写出该电解池中发生反应的总反应式:___;将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是:___。

-
PHEMA材料、树脂Q在生产、生活中有着十分广泛的应用,其中PHEMA的结构是: ,它们的合成路线如图:
,它们的合成路线如图:

已知: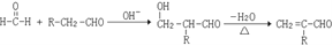
回答下列问题:
(1)C中所含的官能团是____;
(2)G可使Br2的CCl4溶液褪色,F→G的反应类型是____;
(3)写出以下反应的化学方程式:
①A→B____;
②D→E____;
③ →Q____。
→Q____。
(4)D有多种同分异构体,属于酯且含有碳碳双键的共有____种,写出满足以下条件D的同分异构体的结构简式____(不包含立体异构):
①属于酯;②含有碳碳双键;③能发生银镜反应;④含有甲基;
(5)K的核磁共振氢谱有两种峰,峰值面积比为2:9,K的结构简式是:____。
-
化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
A.离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜
B.钢铁制品和铜制品均既能发生吸氧腐蚀又能发生析氢腐蚀
C.现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
D.开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径
-
(12分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素在元素周期表中的位置为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4 反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
(5)下图是一个电化学过程示意图。
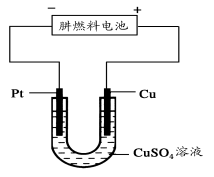
①写出铂片上发生的电极反应式____ ____。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼-空气燃料电池理论上消耗标准状况下的空气_____ ___L(假设空气中氧气体积含量为20%)。
-
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为________;
(2)写出中学化学教材中常见的氮元素的氢化物的化学式________;
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为________;
(4)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
已知:①N2(g)+2O2(g)=N2O4 (1)△H1=-195kJ•mol-1②N2H4 (1)+O2(g)=N2(g)+2H2O(1)△H2=-534.2kJ•mol-1
写出肼和N2O4反应的热化学方程式________.
-
(4分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
写出肼和N2O4 反应的热化学方程式________;
-
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为___________;肼中的化学键类型为 。
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l);ΔH1=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g);ΔH2=-534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式___________________;
(3)已知H2O(l)=H2O(g);ΔH3=+44 kJ·mol-1,则表示肼燃烧热的热化学方程式为_____________
-
醇和酚在人类生产和生活中扮演着重要的角色,根据醇和酚的概念和性质回答下列问题。
(1)下列物质属于酚类的是__________。写出⑤发生消去反应的化学方程式(注明反应条件)____。
①CH3CH2CH2OH②CH3CH(OH)CH3③CH2=CH-CH2OH④CH2OH-CH2OH⑤ ⑥
⑥ ⑦
⑦
(2)司机酒后驾车时可检测他呼出的气体,所利用的化学反应如下:2CrO3(红色)+3C2H5OH+3H2SO4===Cr2(SO4)3(绿色)+3CH3CHO+6H2O被检测的气体成分是__________,上述反应中的氧化剂是____________,还原剂是____________。
(3)300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构简式如图,写出没食子酸中含有的官能团名称_____________用没食子酸制造墨水主要利用了__________类化合物的性质(填代号)。

A.醇 B.酚 C.油脂 D.羧酸
-
铝是当前应用最广泛的金属材料之一,铝制品及其化合物在日常生活和工农业生产中也有着重要的用途。回答下列问题:
(1)基态铝原子的核外电子排布式为____________。
(2)根据元素周期律等知识判断,第一电离能Al____________Mg(填写“大于”或“小于”)。
(3)Al2O3是常用的耐火材料,工业上也是用电解Al2O3方法制取金属Al,据此判断Al2O3的晶体类型是____________。
(4)LiAlH4是一种重要的有机合成试剂,AlH4-的立体构型为____________,LiAlH4中Al原子的杂化轨道类型为____________。
(5)金属铝的晶胞结构如图1所示,原子之间相对位置关系的平面图如图2所示。
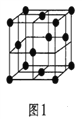
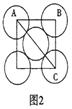
①晶体铝中原子的堆积方式为____________。
②已知铝原子半径为a cm,摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则晶体铝的密度ρ=_______g·cm-3(用含 a、M、NA的代数式来表示)。
-
氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在一定条件下通过以下反应制得:2NO+Cl2=2ClNO,已知几种化学键的键能数据如下表所示:
| 化学键 | Cl-Cl | Cl-N | N=O | N=O(NO) |
| 键能(kJ·mol-1) | 243 | a | 607 | 630 |
请根据表中数据计算:2NO(g)+Cl2(g)=2ClNO(g)△H=___kJ•mol-1。
(2)温度一定时,在一个体积为1L的密闭容器中通入2molNO和1molCl2,10min时ClNO体积占气体总体积40%(气体的“体积分数”即“物质的量分数”),则反应开始到10min内NO的平均反应速率:v(NO)=___mol·L-1·min-1
(3)以NH3为还原剂在脱硝装置中消除烟气中的氮氧化物,
主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H1
副反应:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1267.1kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3=-907.3kJ/mol
①△H1=___。
②将烟气按一定的流速通过脱硝装置,测得出口NO的浓度与温度的关系如图1,试分析脱硝的适宜温度是___(填序号)
a.<850℃ b.900~1000℃ c.>1050 ℃

(4)以连二亚硫酸盐(S2O42-)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2。阴极的电极反应式为___。

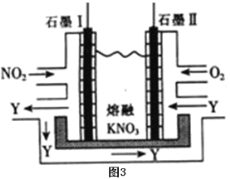
(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图3所示,电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅰ附近发生的电极反应式为:___。

Ni(OH)2+M

 ,它们的合成路线如图:
,它们的合成路线如图:


 ⑥
⑥ ⑦
⑦





