已知A(g)+2B(g)C(g)+4D(g) ΔH=+Q kJ·mol-1(Q>0)。某温度压强下,在密闭容器进行上述反应,下列叙述正确的是( )
A.反应过程中,若压缩体积增大压强能提高A的转化率
B.若反应开始时A为1 mol,则达到平衡时吸收的热量为Q kJ
C.反应至4 min时,若D浓度为0.12 mol·L-1,则B的反应速率为0.03 mol·L-1·min-1
D.反应吸收0.025Q kJ热量时,生成的D的物质的量为0.1 mol
高二化学单选题中等难度题
已知A(g)+2B(g)C(g)+4D(g) ΔH=+Q kJ·mol-1(Q>0)。某温度压强下,在密闭容器进行上述反应,下列叙述正确的是( )
A.反应过程中,若压缩体积增大压强能提高A的转化率
B.若反应开始时A为1 mol,则达到平衡时吸收的热量为Q kJ
C.反应至4 min时,若D浓度为0.12 mol·L-1,则B的反应速率为0.03 mol·L-1·min-1
D.反应吸收0.025Q kJ热量时,生成的D的物质的量为0.1 mol
高二化学单选题中等难度题
已知A(g)+2B(g)C(g)+4D(g) ΔH=+Q kJ·mol-1(Q>0)。某温度压强下,在密闭容器进行上述反应,下列叙述正确的是( )
A.反应过程中,若压缩体积增大压强能提高A的转化率
B.若反应开始时A为1 mol,则达到平衡时吸收的热量为Q kJ
C.反应至4 min时,若D浓度为0.12 mol·L-1,则B的反应速率为0.03 mol·L-1·min-1
D.反应吸收0.025Q kJ热量时,生成的D的物质的量为0.1 mol
高二化学单选题中等难度题查看答案及解析
(10分)在 1.0L恒容密闭容器中放入0.10 mol A (g),在一定温度进行如下反应。A(g)2B(g)+ C(g)+ D(s)△H= + 85.1 kJ / mol
容器内气体总压强(P)与起始压强P。的比值随反应时间(t)变化数据见下表(提示:密闭容器中的压强比等 于气体物质的量之比)。
| 时间t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| P/P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
回答下列问题:
(1)下列能提高 A 的转化率的是 。
A.升高温度 B.向体系中通人A气体
C.减少D的物质的量 D.向体系中通人稀有气体He
(2)反应进行1小时,容器中剩余A的物质的量为 mol。
(3)平衡时A的转化率为
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则 D 的取值范围n(D)mol。
(5)将容器改为恒压容器,改变条件,使反应达到相同的限度,则达到平衡时B的浓度为 。
高二化学填空题困难题查看答案及解析
在 1.0 L 密闭容器中放入 0.10molA(g),在一定温度进行如下反应:A(g)2B(g)+C(g)+D(s) △H= +85.1kJ·mol-1。容器内气体总压强(P)与起始压强 P0 的比值随反应时间(t)数据见下表:
| 时间 t/ h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| P /P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
回答下列问题:
(1)该平衡常数的表达式为_____________。
(2)下列能提高 A 的转化率的是________。
A.升高温度 B.体系中通入 A 气体 C.将 D 的浓度减小
D.通入稀有气体 He,使体系压强增大到原来的 5 倍
E.若体系中的 C 为 HCl,其它物质均难溶于水,滴入少许水
(3)前 2小时 C 的反应速率是___________ mol.L-1.h-1;
(4)平衡时 A 的转化率___________ C 的体积分数_________(均保留两位有效数字)
高二化学综合题中等难度题查看答案及解析
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A. 该反应的化学平衡常数表达式是
B. 此时,B的平衡转化率是35%
C. 增大该体系的压强,平衡向右移动,化学平衡常数增大
D. 增大C,B的平衡转化率不变
高二化学单选题困难题查看答案及解析
某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行反应3A(g)+2B(g)4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6 mol,且反应前后的压强之比为5:4(相同的温度下测量),则下列说法正确的是
A. 该反应的化学平衡常数表达式是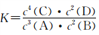
B. 此时B的平衡转化率是40%
C. 增大该体系的压强,平衡向右移动,化学平衡常数增大
D. 其他条件不变时,增大B的浓度,B的平衡转化率不变
高二化学单选题中等难度题查看答案及解析
在恒温恒容的密闭容器中,充入2mol气体A和1mol气体B发生反应:
3A(g)+2B(g)2C(?)+4D(?)。反应一段时间后达到平衡,测得生成1.6molD,反应前后体系压强之比为5:3。则下列说法正确的是 ( )
A. 物质D一定是气体
B. 气体A的平衡转化率大于气体B的平衡转化率
C. 平衡后若减小该体系的压强,平衡向左移动,化学平衡常数减小
D. 平衡后升高温度,若平衡向右进行,则正反应的ΔH>0
高二化学单选题中等难度题查看答案及解析
在恒温恒容的密闭容器中,充入2mol气体A和1mol气体B发生反应:
3A(g)+2B(g)2C(?)+4D(?)。反应一段时间后达到平衡,测得生成1.6molD,反应前后体系压强之比为5:3。则下列说法正确的是 ( )
A. 物质D一定是气体
B. 气体A的平衡转化率大于气体B的平衡转化率
C. 平衡后若减小该体系的压强,平衡向左移动,化学平衡常数减小
D. 平衡后升高温度,若平衡向右进行,则正反应的ΔH>0
高二化学单选题中等难度题查看答案及解析
(14分)Ⅰ、已知:C(s)+H2O(g)CO(g)+H2(g); ΔH一定温度下,在1.0 L密闭容器中放入1 mol C(s)、1 mol H2O(g)进行反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100 kPa | 4.56 | 5.14 | 5.87 | 6.30 | 7.24 | 8.16 | 8.18 | 8.20 | 8.20 |
回答下列问题:
(1)下列哪些选项可以说明该可逆反应已达平衡状态 。
A.混合气体的密度不再发生改变
B.消耗1 mol H2O(g)的同时生成1 mol H2
C.混合气体的总体积
D.v正(CO) = v逆(H2)
(2)由总压强P和起始压强P0表示反应体系的总物质的量n总,n总= mol;
Ⅱ、根据最新“人工固氮”的报道,在常温、常压、光照条件下,N2在催化剂表面可与水发生反应生成NH3,反应方程式:2N2(g)+ 6H2O(l)4NH3(g)+ 3O2(g),进一步研究生成量与温度的关系,常压下测得部分数据如下表:
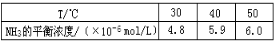
(1)该反应的△H_____O, △S____0(填“>,<,=”)
(2)该反应在30℃、40℃时化学平衡常数分别为K1、K2,则K1_______K2(选填“>,<,=”)
(3)与目前广泛应用的工业合氨相比,该方法的固氮速率慢,氨的生成浓度低,有人提出在常压、450℃下进行该反应,效率将更高,科学家认为该方案不可行,理由是__________.
Ⅲ、向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS−、S2−的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出)。
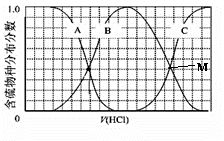
试分析:
①B曲线代表 (用微粒符号表示)分数变化;滴加过程中,溶液中一定成立:c(Na+)= 。
②M点,溶液中主要涉及的离子方程式: 。
高二化学填空题困难题查看答案及解析
在一个盛有催化剂的容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2(g)+3H2(g)2NH3(g),已知加入1mol N2和4mol H2时,达到平衡后生成amol NH3,在相同温度、压强下,保持平衡时各组分的体积分数不变,对①~③的状态,填写表中空白。
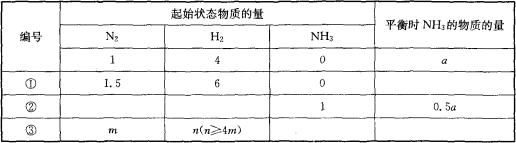
高二化学填空题困难题查看答案及解析
已知一定温度和压强下,合成氨反应:N2(g)+3H2(g)=2NH3(g) ΔH=-92.0 kJ/mol,将1 mol N2和3 mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时向该容器中充入2 mol NH3,反应达到平衡时的热量变化是( )
A.吸收18.4 kJ热量 B.吸收73.6 kJ热量
C.放出18.4 kJ热量 D.放出73.6 kJ热量
高二化学单选题困难题查看答案及解析