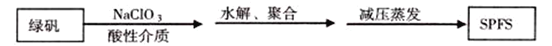-
聚合氯化铝晶体是介于AlCl3和A1(OH)3之间的一种水溶性无机高分子聚合物,其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产工艺流程如图:
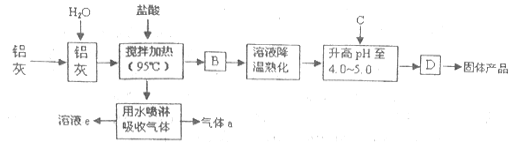
(1)反应中副产品a是___(用化学式表示);
(2)升高pH至4.0~4.5的目的是__;
(3)生产过程中可循环使用的物质是__(用化学式表示);
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用___(填编号);
a.NaOH b.Al c.氨水 d.A12O3 e.NaAlO2
-
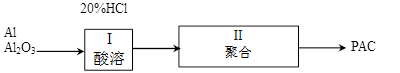
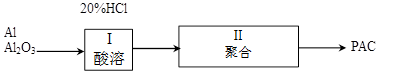
聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

聚合铝(PAC)的分子式为[Al2(OH)aCl b]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b =________(填入合适数字)。
-
黄色固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用。SPFS可表示成Fex(OH)y(SO4)z·nH2O。工业上常用的一种制备流程为:(绿矾化学式为FeSO4·7H2O)
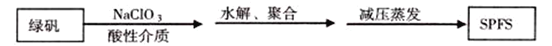
在SPFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=n(OH-)/3n( Fe) ×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH一和Fe的物质的量。试回答下列问题。
(1)在绿矾中加人酸性介质的NaClO3目的是__________ 。
(2)SPFS溶于水后并与水反应生成__________ 能吸附水中的悬浮物来净化水。
(3)取15.05g某固体聚合硫酸铁溶解于水,向其中加人过量的BaCI2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀20.97g.向上述滤液中加人NH3•H2O,调节溶液pH= 6,经过滤、洗涤、干燥得Fe2O3固体5.60g。该固体聚合硫酸铁的盐基度为_________ 。
(4)计算出该固体聚合硫酸铁样品的化学式______________(写出计算过程)。
-
聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:
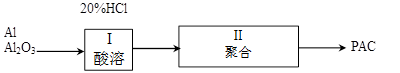
聚合过程主要利用了Al3+的性质是________。
-
聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:
要测定1mol聚合铝中a的值。
①测定时所需的试剂是________(填代号)。
(a) NaOH (b)AgNO3 (c) pH试纸 (d) HNO3
②需要直接测定的物理量是 (用文字表示)。
若该物理量的数值用β表示,试写出聚合铝中a值的表达式。
③测定过程中所需的基本操作是 (按操作先后顺序的代号列出,可重复选择)。
(a) 洗涤 (b) 过滤 (c) 称量 (d) 干燥 (e) 冷却
-
聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:
用36.5%的盐酸配制20%的盐酸,操作步骤是 (依次写出),配制过程中所需的定量仪器是 。
-
(15分)聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

写出铝、氧化铝分别与盐酸反应的离子方程式:
, ,
-
聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝.实验步骤如图:

(1)写出铝、氧化铝分别与盐酸反应的离子方程式:______,______,
(2)用36.5%的盐酸配制20%的盐酸,操作步骤是______(依次写出),配制过程中所需的定量仪器是______.
(3)聚合铝(PAC)的分子式为[Al2(OH)aClb]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=n(OH-)/3n(Al3+),当B=2/3时,b=______(填入合适数字).
(4)聚合过程主要利用了Al3+的性质是______.
(5)要测定1mol聚合铝中a的值.
①测定时所需的试剂是______(填代号).
(a) NaOH(b)AgNO3(c) pH试纸(d) HNO3
②需要直接测定的物理量是______(用文字表示).若该物理量的数值用β表示,试写出聚合铝中a值的表达式______.
③测定过程中所需的基本操作是______(按操作先后顺序的代号列出,可重复选择).
(a) 洗涤(b) 过滤(c) 称量 (d) 干燥(e) 冷却.
-
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途。完成下列填空:
(1) 实验室配制氯化铝溶液时加入盐酸的目的是____________。
(2)往AlCl3溶液中加入过量下列溶液,最终得到无色澄清溶液的是______(填编号)。
a Na2CO3 b NaOH c NaAlO2 d H2SO4
取AlCl3溶液,用小火持续加热至水刚好蒸干,生成白色固体的组成可表示为:Al2(OH)nCl(6-n),为确定n的值,取3.490g白色固体,全部溶解在0.1120 mol的HNO3(足量)中,并加水稀释成100 mL,将溶液分成两等价,进行如下实验:
(3)一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得Al2O3的质量为1.020g。判断加入氨水已足量的操作是________。过滤、洗涤后至少要灼烧_______次(填写数字);测定样品中铝元素含量时不选择测定干燥Al(OH)3的质量,而是测定A12O3的质量的原因可能是____(选填编号)。
a 干燥Al(OH)3固体时易失水 b Al2O3的质量比Al(OH)3大,误差小
c 沉淀Al(OH)3时不完全 d 灼烧氧化铝时不分解
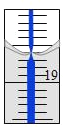
(4)从另一份溶液中取出20.00 mL,用0.1290 mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00 mL,终点时滴定管液面(局部)如图所示(背景为白底蓝线的滴定管)。则滴定管的读数__________mL,Al2(OH)nCl(6-n)中n的值为__________。
-
NiSO4 6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
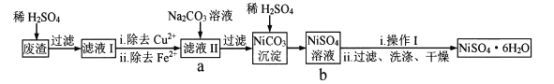
A.溶解废渣时不能用稀盐酸代替稀H2SO4 B.除去Cu2+可采用FeS
C.流程中a-b的目的是富集NiSO4 D.“操作I”为蒸发浓缩、冷却结晶